1 строение электронных оболочек атомов. Строение атомов химических элементов. Состав атомного ядра. Строение электронных оболочек атомов. Электронные формулы атомов
Лекция: Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы
Строение атома
 XX столетие является временем изобретения "модели строения атома". Исходя из предоставленного строения, удалось выработать следующую гипотезу: вокруг достаточно маленького по объему и размеру ядра, электроны совершают перемещения, схожие с перемещением планет вокруг Солнца. Последующее изучение атома показало, что сам атом и его строение гораздо сложнее, чем было установлено раньше. И в настоящее время, при огромных возможностях в научной сфере, атом исследован не до конца. Такие составляющие, как атом и молекулы, считаются предметами микромира. Поэтому данные части человек не способен рассмотреть самостоятельно. В этом мире установлены совершенно иные законы и правила, отличающиеся от макромира. Исходя из этого, исследование атома ведется на его модели.
XX столетие является временем изобретения "модели строения атома". Исходя из предоставленного строения, удалось выработать следующую гипотезу: вокруг достаточно маленького по объему и размеру ядра, электроны совершают перемещения, схожие с перемещением планет вокруг Солнца. Последующее изучение атома показало, что сам атом и его строение гораздо сложнее, чем было установлено раньше. И в настоящее время, при огромных возможностях в научной сфере, атом исследован не до конца. Такие составляющие, как атом и молекулы, считаются предметами микромира. Поэтому данные части человек не способен рассмотреть самостоятельно. В этом мире установлены совершенно иные законы и правила, отличающиеся от макромира. Исходя из этого, исследование атома ведется на его модели.
 Любому атому присвоен порядковый номер, закрепленный в Периодической таблице Менделеева Д.И. К примеру, порядковый номер атома фосфора (Р) - 15.
Любому атому присвоен порядковый номер, закрепленный в Периодической таблице Менделеева Д.И. К примеру, порядковый номер атома фосфора (Р) - 15.
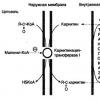
Итак, атом состоит из протонов (p + ) , нейтронов (n 0 ) и электронов (e - ). Протоны и нейтроны образуют ядро атома, оно имеет положительный заряд. А электроны, совершающие перемещения вокруг ядра, «конструируют» электронную оболочку атома, имеющую отрицательный заряд.

Сколько электронов в атоме? Это легко узнать. Достаточно посмотреть порядковый номер элемента в таблице.

Так, число электронов фосфора равно 15 . Количество электронов, содержащихся в оболочке атома, строго равно числу протонов, содержащихся в ядре. Значит и протонов в ядре атома фосфора 15 .
Масса протонов и нейтронов, составляющих массу ядра атома, одинакова. А электроны меньше в 2000 раз. Это означает что вся масса атома сосредоточена в ядре, массой электронов пренебрегают. Массу ядра атома мы также можем узнать из таблицы. Посмотрите изображение фосфора в таблице. Внизу мы видим обозначение 30, 974 – это и есть масса ядра фосфора, его атомная масса. При записи мы округляем эту цифру. Исходя из сказанного, запишем строение атома фосфора следующим образом:
(внизу слева написали заряд ядра – 15, вверху слева округленное значение массы атома – 31).
Ядро атома фосфора:

(внизу слева пишем заряд: протоны имеют заряд равный +1, а нейтроны не заряжены, то есть заряд 0; вверху слева масса протона и нейтрона, равная 1 – условная единица массы атома; заряд ядра атома равен числу протонов в ядре, значит р=15, а число нейтронов нужно посчитать: из атомной массы вычесть заряд, т.е. 31 – 15 = 16).
Электронная оболочка атома фосфора включает в себя 15 отрицательно заряженных электронов, уравновешивающих положительно заряженные протоны. Поэтому, атом – электронейтральная частица.
Энергетические уровни
Рис.1
 Далее нам необходимо подробно разобрать как распределяются электроны в атоме. Их движение не хаотично, а подчинено конкретному порядку. Какие - то из имеющихся электронов, притягиваются к ядру с достаточно большой силой, а другие наоборот, притягиваются слабо. Первопричина такого поведения электронов скрывается в разной степени удаленности электронов от ядра. То есть, ближе находящийся к ядру электрон, станет прочнее с ним взаимосвязан. Эти электроны просто нельзя отсоединить от электронной оболочки. Чем электрон дальше от ядра, тем проще «вытащить» его из оболочки. Так же, запас энергии электрона возрастает, по мере удаления от ядра атома. Энергия электрона определяется главным квантовым числом n, равняющимся любому натуральному числу (1,2,3,4…). Электроны, имеющие одинаковое значение n, образуют один электронный слой, как бы отгораживаясь от иных электронов, передвигающихся на удаленном расстоянии. На рисунке 1 изображены электронные слои, содержащиеся в электронной оболочке, в центре ядро атома.
Далее нам необходимо подробно разобрать как распределяются электроны в атоме. Их движение не хаотично, а подчинено конкретному порядку. Какие - то из имеющихся электронов, притягиваются к ядру с достаточно большой силой, а другие наоборот, притягиваются слабо. Первопричина такого поведения электронов скрывается в разной степени удаленности электронов от ядра. То есть, ближе находящийся к ядру электрон, станет прочнее с ним взаимосвязан. Эти электроны просто нельзя отсоединить от электронной оболочки. Чем электрон дальше от ядра, тем проще «вытащить» его из оболочки. Так же, запас энергии электрона возрастает, по мере удаления от ядра атома. Энергия электрона определяется главным квантовым числом n, равняющимся любому натуральному числу (1,2,3,4…). Электроны, имеющие одинаковое значение n, образуют один электронный слой, как бы отгораживаясь от иных электронов, передвигающихся на удаленном расстоянии. На рисунке 1 изображены электронные слои, содержащиеся в электронной оболочке, в центре ядро атома.
Вы можете заметить, как по мере удаления от ядра увеличивается объем слоя. Следовательно, чем дальше слой от ядра, тем больше в нем электронов.
Электронный слой, содержит в себе электроны, сходные по показателям энергии. Из – за этого, такие слои нередко именуют энергетическими уровнями. Сколько же уровней может содержать атом? Количество энергетических уровней равно номеру периода в таблице Менделеева Д.И. в котором находится элемент. К примеру, фосфор (Р) находится в третьем периоде, значит атом фосфора имеет три энергетических уровня.
Рис. 2
 Как узнать максимальное количество электронов, располагающихся на одном электронном слое? Для этого используем формулу N max = 2n
2
, где n – это номер уровня.
Как узнать максимальное количество электронов, располагающихся на одном электронном слое? Для этого используем формулу N max = 2n
2
, где n – это номер уровня. Получим, что первый уровень содержит всего 2 электрона, второй – 8, третий – 18, четвертый – 32.
Каждый энергетический уровень содержит в себе подуровни. Их буквенные обозначения: s-, p-, d-
и f-
. Посмотрите на рис. 2:
Разным цветом обозначены энергетические уровни, а полосками разной толщины подуровни.
Самый тонкий подуровень обозначается буквой s . 1s – это s-подуровень первого уровня, 2s – это s-подуровень второго уровня и так далее.
На втором энергетическом уровне появился p-подуровень, на третьем – d-подуровень, а на четвертом f-подуровень.
Запомните увиденную закономерность: первый энергетический уровень включает одну s-подуровень, второй два s- и p- подуровня, третий три s-, p- и d-подуровня, а четвертый уровень четыре s-, p-, d- и f-подуровня.
На s-подуровне могут находится только 2 электрона, на p-подуровне- максимум 6 электронов, на d-подуровне - 10 электронов, а на f-подуровне до 14 электронов.
Электронные орбитали
Область (место) где может находится электрон называется электронным облаком или орбиталью. Имейте ввиду, что говорится о вероятной области нахождении электрона, поскольку скорость его движения в сотни тысяч раз больше скорости движения иглы швейной машинки. Графически эта область изображается в виде ячейки:
В одной ячейке может находится два электрона. Судя по рисунку 2 можно сделать вывод о том, что s-подуровень, включающий не более двух электронов может содержать только одну s-орбиталь, обозначается одной ячейкой; p-подуровень имеет три р-орбитали (3 ячейки), d-подуровень пять d-орбиталей (5 ячеек), а f-подуровень семь f-орбиталей (7 ячеек).
Форма орбитали зависит от орбитального квантового числа (l - эль) атома. Атомный энергетический уровень, берет начало с s – орбитали, имеющей l = 0. Представленная орбиталь имеет сферическую форму. На уровнях, идущих после s - орбитали, образуются p – орбитали с l = 1. P - орбитали напоминают форму гантели. Орбиталей, имеющих данную форму, всего три. Каждая возможная орбиталь содержит в себе не больше 2 – ух электронов. Далее располагаются более сложного строения d -орбитали (l = 2), а за ними f -орбитали (l = 3).
Рис. 3 Форма орбиталей Электроны в орбиталях изображаются в виде стрелочек. Если орбитали содержат по одному электрону, то они однонаправленны – стрелкой вверх:
Электроны в орбиталях изображаются в виде стрелочек. Если орбитали содержат по одному электрону, то они однонаправленны – стрелкой вверх:
Если же в орбитали два электрона, то они имеют два направления: стрелкой вверх и стрелкой вниз, т.е. электроны разнонаправленны:
Такое строение электронов называется валентным.
Существуют три условия наполнения атомных орбиталей электронами:
1 условие: Принцип минимального количества энергии. Заполнение орбиталей начинается с подуровня, имеющего минимальную энергию. Согласно данному принципу подуровни заполняются в таком порядке: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5р 6 6s 2 5d 1 4f 14 ... Как мы видим, в некоторых случаях электрону энергетически выгоднее занять место в подуровне вышележащего уровня, хотя подуровень нижележащего уровня не заполнен. Например, валентная конфигурация атома фосфора выглядит так:
Рис. 4

2 условие: Принцип Паули. Одна орбиталь включает 2 электрона (электронную пару) и не больше. Но возможно и содержание всего одного электрона. Его именуют неспаренным.
3 условие: Правило Хунда. Каждую орбиталь одного подуровня сначала заполняют по одному электрону, затем в них добавляются по второму электрону. В жизни мы видели аналогичную ситуацию, когда незнакомые пассажиры автобуса сначала занимают по одному все свободные сидения, а потом рассаживаются по два.
Электронная конфигурация атома в основном и возбужденном состоянии
Энергия атома, находящегося в основном состоянии, наименьшая. Если атомы начинают получать энергию из вне, к примеру, когда вещество нагревается, то они из основного состояния переходят в возбужденное. Этот переход возможен при наличии свободных орбиталей, на которые могут переместиться электроны. Но это временно, отдавая энергию, возбужденный атом возвращается в своё основное состояние.
Закрепим полученные знания на примере. Рассмотрим электронную конфигурацию, т.е. сосредоточение электронов по орбиталям атома фосфора в основном (невозбужденном состоянии). Еще раз обратимся к рис. 4. Итак, вспомним, что атом фосфора имеет три энергетических уровня, которые изображаются полудугами: +15)))
Распределим, имеющиеся 15 электронов на эти три энергетических уровня:

Такие формулы называются электронными конфигурациями. Есть еще электронно – графические, они иллюстрируют размещение электронов внутри энергетических уровней. Электронно – графическая конфигурация фосфора выглядит так: 1s 2 2s 2 2p 6 3s 2 3p 3 (здесь большие цифры – это номера энергетических уровней, буквы – это подуровни, а маленькие цифры – количество электронов подуровня, если их сложить, получится число 15).
В возбужденном состоянии атома фосфора 1 электрон переходит с 3s-орбитали на 3d-орбиталь, а конфигурация выглядит так: 1s 2 2s 2 2p 6 3s 1 3p 3 3d
1
.
| |
Атом - это мельчайшая частица химического вещества, которая способна сохранять его свойства. Слово «атом» происходит от древнегреческого «atomos», что означает «неделимый». В зависимости о того, сколько и каких частиц находится в атоме, можно определить химический элемент .
Кратко о строении атома
Как можно вкратце перечислить основные сведения о является частицей с одним ядром, которое заряжено положительно. Вокруг этого ядра расположено отрицательно заряженное облако из электронов. Каждый атом в своем обычном состоянии является нейтральным. Размер этой частицы полностью может быть определен размером электронного облака, которое окружает ядро.
Само ядро, в свою очередь, тоже состоит из более мелких частиц - протонов и нейтронов. Протоны являются положительно заряженными. Нейтроны не несут в себе никакого заряда. Однако протоны вместе с нейтронами объединяются в одну категорию и носят название нуклонов. Если необходимы основные сведения о строении атома кратко, то эта информация может быть ограничена перечисленными данными .

Первые сведения об атоме
О том же, что материя может состоять из мелких частиц, подозревали еще древние греки. Они полагали, что все существующее и состоит из атомов. Однако такое воззрение носило чисто философский характер и не может быть трактовано научно.
Первым основные сведения о строении атома получил английский ученый Именно этот исследователь сумел обнаружить, что два химических элемента могут вступать в различные соотношения, и при этом каждая такая комбинация будет представлять собой новое вещество. Например, восемь частей элемента кислорода порождают собой углекислый газ. Четыре части кислорода - угарный газ.
В 1803 году Дальтон открыл так называемый закон кратных отношений в химии. При помощи косвенных измерений (так как ни один атом тогда не мог быть рассмотрен под тогдашними микроскопами) Дальтон сделал вывод об относительном весе атомов .

Исследования Резерфорда
Почти столетие спустя основные сведения о строении атомов были подтверждены еще одним английским химиком - Ученый предложил модель электронной оболочки мельчайших частиц.
На тот момент названная Резерфордом «Планетарная модель атома» была одним из важнейших шагов, которые могла сделать химия. Основные сведения о строении атома свидетельствовали о том, что он похож на Солнечную систему: вокруг ядра по строго определенным орбитам вращаются частицы-электроны, подобно тому, как это делают планеты.
Электронная оболочка атомов и формулы атомов химических элементов
Электронная оболочка каждого из атомов содержит ровно столько электронов, сколько находится в его ядре протонов. Именно поэтому атом является нейтральным. В 1913 году еще один ученый получил основные сведения о строении атома. Формула Нильса Бора была похожа на ту, что получил Резерфорд. Согласно его концепции, электроны также вращаются вокруг ядра, расположенного в центре. Бор доработал теорию Резерфорда, внес стройность в ее факты.
Уже тогда были составлены формулы некоторых химических веществ. Например, схематически строение атома азота обозначается как 1s 2 2s 2 2p 3 , строение атома натрия выражается формулой 1s 2 2s 2 2p 6 3s 1 . Через эти формулы можно увидеть, какое количество электронов движется по каждой из орбиталей того или иного химического вещества.

Модель Шредингера
Однако затем и эта атомная модель устарела. Основные сведения о строении атома, известные науке сегодня, во многом стали доступны благодаря исследованиям австрийского физика
Он предложил новую модель его строения - волновую. К этому времени ученые уже доказали, что электрон наделен не только природой частицы, но обладает свойствами волны.
Однако у модели Шредингера и Резерфорда имеются и общие положения. Их теории сходны в том, что электроны существуют на определенных уровнях.
Такие уровни также называются электронными слоями. При помощи номера уровня может быть охарактеризована энергия электрона. Чем выше слой, тем большей энергией он обладает. Все уровни считаются снизу вверх, таким образом, номер уровня соответствует его энергии. Каждый из слоев в электронной оболочке атома имеет свои подуровни. При этом у первого уровня может быть один подуровень, у второго - два, у третьего - три и так далее (см. приведенные выше электронные формулы азота и натрия).

Еще более мелкие частицы
На данный момент, конечно, открыты еще более мелкие частицы, нежели электрон, протон и нейтрон. Известно, что протон состоит из кварков. Существуют и еще более мелкие частицы мироздания - например, нейтрино, который по своим размерам в сто раз меньше кварка и в миллиард раз меньше протона.
Нейтрино - это настолько мелкая частица, что она в 10 септиллионов раз меньше, чем, к примеру, тираннозавр. Сам тираннозавр во столько же раз меньших размеров, чем вся обозримая Вселенная.
Основные сведения о строении атома: радиоактивность
Всегда было известно, что ни одна химическая реакция не может превратить один элемент в другой. Но в процессе радиоактивного излучения это происходит самопроизвольно.
Радиоактивностью называют способность ядер атомов превращаться в другие ядра - более устойчивые. Когда люди получили основные сведения о строении атомов, изотопы в определенной мере могли служить воплощением мечтаний средневековых алхимиков.
В процессе распада изотопов испускается радиоактивное излучение. Впервые такое явление было обнаружено Беккерелем. Главный вид радиоактивного излучения - это альфа-распад. При нем происходит выброс альфа-частицы. Также существует бета-распад, при котором из ядра атома выбрасывается, соответственно, бета-частица.
Природные и искусственные изотопы
В настоящее время известно порядка 40 природных изотопов. Их большая часть расположена в трех категориях: урана-радия, тория и актиния. Все эти изотопы можно встретить в природе - в горных породах, почве, воздухе. Но помимо них, известно также порядка тысячи искусственно выведенных изотопов, которые получают в ядерных реакторах. Многие их таких изотопов используются в медицине, особенно в диагностике .

Пропорции внутри атома
Если представить себе атом, размеры которого будут сопоставимы с размерами международного спортивного стадиона, тогда можно визуально получить следующие пропорции. Электроны атома на таком «стадионе» будут располагаться на самом верху трибун. Каждый из них будет иметь размеры меньше, чем булавочная головка. Тогда ядро будет расположено в центре этого поля, а его размер будет не больше, чем размер горошины.
Иногда люди задают вопрос, как в действительности выглядит атом. На самом деле он в буквальном смысле слова не выглядит никак - не по той причине, что в науке используются недостаточно хорошие микроскопы. Размеры атома находятся в тех областях, где понятие «видимости» просто не существует.
Атомы обладают очень малыми размерами. Но насколько малы в действительности эти размеры? Факт состоит в том, что самая маленькая, едва различимая человеческим глазом крупица соли содержит в себе порядка одного квинтиллиона атомов.
Если же представить себе атом такого размера, который мог бы уместиться в человеческую руку, то тогда рядом с ним находились бы вирусы 300-метровой длины. Бактерии имели бы длину 3 км, а толщина человеческого волоса стала бы равна 150 км. В лежачем положении он смог бы выходить за границы земной атмосферы. А если бы такие пропорции были действительны, то человеческий волос в длину смог бы достигать Луны. Вот такой он непростой и интересный атом, изучением которого ученые продолжают заниматься и по сей день.
Электроны
Понятие атом возникло еще в античном мире для обозначения частиц вещества. В переводе с греческого атом означает «неделимый».

Ирландский физик Стони на основании опытов пришел к выводу, что электричество переносится мельчайшими частицами, сущеетвующими в атомах всех химических элементов. В 1891 г. Стони предложил эти частицы назвать электронами, что по-гречески означает «янтарь». Через несколько лет после того, как электрон получил свое название, английский физик Джозеф Томсон и французский физик Жан Перрен доказали, что электроны несут на себе отрицательный заряд. Это наименьший отрицательный заряд, который в химии принят за единицу (-1). Томсон даже сумел определить скорость движения электрона (скорость электрона на орбите обратно пропорциональна номеру орбиты n. Радиусы орбит растут пропорционально квадрату номера орбиты. На первой орбите атома водорода (n=1; Z=1) скорость равна ≈ 2,2·106 м/с, то есть примерно в сотню раз меньше скорости света с=3·108 м/с.) и массу электрона (она почти в 2000 раз меньше массы атома водорода).

Состояние электронов в атоме
Под состоянием электрона в атоме понимают совокупность информации об энергии определенного электрона и пространстве, в котором он находится . Электрон в атоме не имеет траектории движения, т. е. можно говорить лишь о вероятности нахождения его в пространстве вокруг ядра .
 Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек. При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек. При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
Пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью. В нем заключено приблизительно 90 % электронного облака , и это означает, что около 90 % времени электрон находится в этой части пространства. По форме различают 4 известных ныне типа орбиталей , которые обозначаются латинскими буквами s, p, d и f . Графическое изображение некоторых форм электронных орбиталей представлено на рисунке.

Важнейшей характеристикой движения электрона на определенной орбитали является энергия его связи с ядром . Электроны, обладающие близкими значениями энергии, образуют единый электронный слои, или энергетический уровень. Энергетические уровни нумеруют, начиная от ядра, - 1, 2, 3, 4, 5, 6 и 7.
Целое число n, обозначающее номер энергетического уровня, называют главным квантовым числом. Оно характеризует энергию электронов, занимающих данный энергетический уровень. Наименьшей энергией обладают электроны первого энергетического уровня, наиболее близкого к ядру. По сравнению с электронами первого уровня, электроны последующих уровней будут характеризоваться большим запасом энергии. Следовательно, наименее прочно связаны с ядром атома электроны внешнего уровня.
Наибольшее число электронов на энергетическом уровне определяется по формуле:
N = 2n 2 ,
где N - максимальное число электронов; n - номер уровня, или главное квантовое число. Следовательно, на первом, ближайшем к ядру энергетическом уровне может находиться не более двух электронов; на втором - не более 8; на третьем - не более 18; на четвертом - не более 32.
Начиная со второго энергетического уровня (n = 2) каждый из уровней подразделяется на подуровни (подслои), несколько отличающиеся друг от друга энергией связи с ядром. Число подуровней равно значению главного квантового числа: первый энергетический уровень имеет один подуровень; второй - два; третий - три; четвертый - четыре подуровня . Подуровни в свою очередь образованы орбиталями. Каждому значению n соответствует число орбиталей, равное n.
Подуровни принято обозначать латинскими буквами, равно как и форму орбиталей, из которых они состоят: s, p, d, f.

Протоны и нейтроны

Атом любого химического элемента сравним с крохотной Солнечной системой. Поэтому такую модель атома, предложенную Э. Резерфордом, называют планетарной .
Атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов - протонов и нейтронов .
Протоны имеют заряд, равный заряду электронов, но противоположный по знаку (+1), и массу, равную массе атома водорода (она принята в химии за единицу). Нейтроны не несут заряда, они нейтральны и имеют массу, равную массе протона.
Протоны и нейтроны вместе называют нуклонами (от лат. nucleus - ядро). Сумма числа протонов и нейтронов в атоме называется массовым числом . Например, массовое число атома алюминия:

13 + 14 = 27
число протонов 13, число нейтронов 14, массовое число 27
Так как массой электрона, ничтожно малой, можно пренебречь, то очевидно, что в ядре сосредоточена вся масса атома. Электроны обозначают e — .
Поскольку атом электронейтрален , то также очевидно, что число протонов и электронов в атоме одинаково. Оно равно порядковому номеру химического элемента, присвоенному ему в Периодической системе. Масса атома складывается из массы протонов и нейтронов. Зная порядковый номер элемента (Z), т. е. число протонов, и массовое число (А), равное сумме чисел протонов и нейтронов, можно найти число нейтронов (N) по формуле:

N = A — Z
Например, число нейтронов в атоме железа равно:
56 — 26 = 30
Изотопы
Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядра, но разное массовое число, называются изотопами . Химические элементы, встречающиеся в природе, являются смесью изотопов. Так, углерод имеет три изотопа с массой 12, 13, 14; кислород - три изотопа с массой 16, 17, 18 и т. д. Обычно приводимая в Периодической системе относительная атомная масса химического элемента является средним значением атомных масс природной смеси изотопов данного элемента с учетом их относительного содержания в природе. Химические свойства изотопов большинства химических элементов совершенно одинаковы. Однако изотопы водорода сильно различаются по свойствам из-за резкого кратного увеличения их относительной атомной массы; им даже присвоены индивидуальные названия и химические знаки.

Элементы первого периода
Схема электронного строения атома водорода:

Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням).

Графическая электронная формула атома водорода (показывает распределение электронов по энергетическим уровням и подуровням):

Графические электронные формулы атомов показывают распределение электронов не только по уровням и подуровням, но и по орбиталям.
В атоме гелия первый электронный слой завершен - в нем 2 электрона. Водород и гелий - s-элементы; у этих атомов заполняется электронами s-орбиталь.

У всех элементов второго периода первый электронный слой заполнен , и электроны заполняют s- и р-орбитали второго электронного слоя в соответствии с принципом наименьшей энергии (сначала s, а затем р) и правилами Паули и Хунда.
В атоме неона второй электронный слой завершен - в нем 8 электронов.
У атомов элементов третьего периода первый и второй электронные слои завершены, поэтому заполняется третий электронный слой, в котором электроны могут занимать 3s-, 3р- и 3d- подуровни.
У атома магния достраивается 3s- электронная орбиталь. Na и Mg - s-элементы.
У алюминия и последующих элементов заполняется электронами 3р-подуровень.
У элементов третьего периода остаются незаполненными 3d-орбитали.
Все элементы от Al до Ar - р-элементы. s- и р-элементы образуют главные подгруппы в Периодической системе.

Элементы четвертого — седьмого периодов
У атомов калия и кальция появляется четвертый электронный слой, заполняется 4s-подуровень, т. к. он имеет меньшую энергию, чем 3d-подуровень.
К, Са - s-элементы, входящие в главные подгруппы. У атомов от Sc до Zn заполняется электронами 3d-подуровень. Это 3d-элементы. Они входят в побочные подгруппы, у них заполняется предвнешний электронный слой, их относят к переходным элементам.
Обратите внимание на строение электронных оболочек атомов хрома и меди. В них происходит «провал» одного электрона с 4s- на 3d-подуровень, что объясняется большей энергетической устойчивостью образующихся при этом электронных конфигураций 3d 5 и 3d 10:

В атоме цинка третий электронный слой завершен - в нем заполнены все подуровни 3s, 3р и 3d, всего на них 18 электронов. У следующих за цинком элементов продолжает заполняться четвертый электронный слой, 4р-подуровень.
Элементы от Ga до Кr - р-элементы.
У атома криптона внешний слой (четвертый) завершен, имеет 8 электронов. Но всего в четвертом электронном слое может быть 32 электрона; у атома криптона пока остаются незаполненными 4d- и 4f-подуровни.У элементов пятого периода идет заполнение по-дуровней в следующем порядке: 5s — 4d — 5р. И так-же встречаются исключения, связанные с «провалом » электронов, у 41 Nb, 42 Мо, 44 Ru, 45 Rh, 46 Pd, 47 Ag.
В шестом и седьмом периодах появляются f-элементы, т. е. элементы, у которых идет заполнение соответственно 4f- и 5f-подуровней третьего снаружи электронного слоя.
4f-элементы называют лантаноидами.
5f-элементы называют актиноидами.
Порядок заполнения электронных подуровней в атомах элементов шестого периода: 55 Cs и 56 Ва - 6s-элементы; 57 La … 6s 2 5d x - 5d-элемент; 58 Се - 71 Lu - 4f-элементы; 72 Hf — 80 Hg - 5d-элементы; 81 Т1 — 86 Rn - 6d-элементы. Но и здесь встречаются элементы, у которых «нарушается» порядок заполнения электронных орбиталей, что, например, связано с большей энергетической устойчивостью наполовину и полностью заполненных f-подуровней, т. е. nf 7 и nf 14 . В зависимости от того, какой подуровень атома заполняется электронами последним, все элементы делят на четыре электронных семейства, или блока:
- s-элементы . Электронами заполняется s-подуровень внешнего уровня атома; к s-элементам относятся водород, гелий и элементы главных подгрупп I и II групп.
- p-элементы . Электронами заполняется р-подуровень внешнего уровня атома; к р-элементам относятся элементы главных подгрупп III- VIII групп.
- d-элементы . Электронами заполняется d-подуровень предвнешнего уровня атома; к d-элементам относятся элементы побочных подгрупп I-VIII групп, т. е. элементы вставных декад больших периодов, расположенных между s- и р-элементами. Их также называют переходными элементами.
- f-элементы . Электронами заполняется f-подуровень третьего снаружи уровня атома; к ним относятся лантаноиды и антиноиды.

Швейцарский физик В. Паули в 1925 г. установил, что в атоме на одной орбитали может находиться не более двух электронов, имеющих противоположные (антипараллельные) спины (в переводе с английского - «веретено»), т. е. обладающих такими свойствами, которые условно можно представить себе как вращение электрона вокруг своей воображаемый оси: по часовой или против часовой стрелки.

Этот принцип носит название принципа Паули . Если на орбитали находится один электрон, то он называется неспаренным, если два, то это спаренные электроны, т. е. электроны с противоположными спинами. На рисунке показана схема подразделения энергетических уровней на подуровни и очередность их заполнения.


Очень часто строение электронных оболочек атомов изображают с помощью энергетических или квантовых ячеек - записывают так называемые графические электронные формулы. Для этой записи используют следующие обозначения: каждая квантовая ячейка обозначается клеткой, которая соответствует одной орбитали; каждый электрон обозначается стрелкой, соответствующей направлению спина. При записи графической электронной формулы следует помнить два правила: принцип Паули и правило Ф. Хунда , согласно которому электроны занимают свободные ячейки сначала по одному и имеют при этом одинаковое значение спина, а лишь затем спариваются, но спины, при этом по принципу Паули будут уже противоположно направленными.
Правило Хунда и принцип Паули
Правило Хунда - правило квантовой химии, определяющее порядок заполнения орбиталей определённого подслоя и формулируется следующим образом: суммарное значение спинового квантового числа электронов данного подслоя должно быть максимальным. Сформулировано Фридрихом Хундом в 1925 году.
Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Другая формулировка : Ниже по энергии лежит тот атомный терм, для которого выполняются два условия.
- Мультиплетность максимальна
- При совпадении мультиплетностей суммарный орбитальный момент L максимален.
Разберём это правило на примере заполнения орбиталей p-подуровня p -элементов второго периода (то есть от бора до неона (в приведённой ниже схеме горизонтальными чёрточками обозначены орбитали, вертикальными стрелками - электроны, причём направление стрелки обозначает ориентацию спина).
Правило Клечковского
Правило Клечковского — по мере увеличения суммарного числа электронов в атомах (при возрастании зарядов их ядер, или порядковых номеров химических элементов) атомные орбитали заселяются таким образом, что появление электронов на орбитали с более высокой энергией зависит только от главного квантового числа n и не зависит от всех остальных квантовых чисел, в том числе и от l. Физически это означает, что в водородоподобном атоме (в отсутствие межэлектронного отталкивания) орбитальная энергия электрона определяется только пространственной удаленностью зарядовой плотности электрона от ядра и не зависит от особенностей его движения в поле ядра.
Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречатреальной энергетической последовательности атомых орбиталей только в двух однотипных случаях: у атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место “провал” электрона с s-подуровня внешнего слояна d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома, аименно: после заполнения двумя электронами орбитали 6s
Тема – 1: Строение атома. Заряд ядра, порядковый номер и масса атома.
Студент должен:
Знать:
· Современную формулировку периодического закона и строение таблицы
Уметь:
· Определять элементы по описанным свойствам, определять элемент по электронной формуле.
· Устанавливать по порядковому номеру элемента номер периода и номер группы, в которых он находится, а также формулы и характер высшего оксида и соответсующего ему гидрооксида.
· Записывать электронную формулу данного элемента и сравнивать с окружающими его элементами в периоде и группе.
1.1. Порядковый номер химического элемента и значение заряда ядра его атома. Изотопы
Классифицируя химические элементы, использовал два их признака: а) относительную атомную массу б) свойства простых веществ и соединений элементов.
Первый признак – ведущий, второй – проявляется связанно с первым: свойства элементов изменяются периодически с возрастанием относительной атомной массы.
Но при построении периодической системы, располагая химические элементы по возрастанию относительной атомной массы, в некоторых местах нарушил это правило: поменял кобальт и никель, теллур и йод. Позднее так же пришлось поступить еще с двумя парами химических элементов: аргон – калий и торий – протактиний. Ведь активный щелочной метал калий нельзя включить в семейство химически устойчивых инертных газов, которые или вовсе не образуют химических соединений (гелий, неон), или вступают в реакции с трудом.
не мог объяснить эти исключения из общего правила, так же, как и причину периодичности в изменении свойств химических элементов, расположенных по возрастанию относительной атомной массы.
В XX в. Ученые установили, что атом состоит из ядра и движущихся около него электронов. Движущиеся вокруг ядра электроны образуют электронную оболочку атома. Атом – электро – нейтральная частица, т. е. не имеющая заряда. Ядро же заряжено положительно, и его заряд нейтрализуется суммарным отрицательным зарядом всех электронов в атоме. Например, если ядро атома имеет заряд +4, то вокруг него движутся четыре электрона, каждый из которых имеет заряд, равный -1.
Экспериментально было установлено, что порядковые номера элементов в периодической системе совпадают со значениями зарядов ядер их атомов. Заряд ядра атома водорода равен +1, гелия +2, лития +3 ит. д. Положительный заряд атома у каждого последующего элемента на единицу больше, чем у предыдущего, и в его электронной оболочке на один электрон больше.
Порядковый (атомный) номер химического элемента численно равен заряду его атома.
С тех пор как ученые выявили физический смысл порядкового номера элемента, периодический закон формулируется так: свойства простых веществ, а также состав и свойства соединений химических элементов находятся в периодической зависимости от заряда ядра атомов.
Как можно объяснить, почему значения зарядов ядер атомов химических элементов в периодической системе возрастают, а правильная последовательность увеличения относительной атомной массы в ряде случаев нарушается? Для ответа на этот вопрос надо привлечь сведения о составе атомных ядер, известные вам из курса физики.
Ядра атомов заряжены положительно, так как в их состав входят протоны. Протон – это частица с зарядом +1 и относительной массой, равной 1. Ядро атома водорода имеющего относительную атомную массу, равную 1,- это протон. В ядре гелия два протона, но относительная атомная масса гелия равна 4. Это связано с тем, что в ядро атома гелия входят не только протоны, но и нейтроны – незаряженные частицы с относительной атомной массой, равной 1. Следовательно, чтобы найти число нейтронов в атоме, из относительной атомной массы надо вычесть число протонов (заряд ядра атома, порядковый номер) Масса электронов ничтожна, мала, ее в расчет не принимают.
Именно по числу протонов в ядре отличаются атомы разных элементов. Химический элемент – это вид атомов с одинаковым зарядом ядра. Число нейтронов в ядрах атомов одного и того же элемента может быть разным.
Разновидности атомов химического элемента, имеющие в ядрах разное число нейтронов, называют изотопами. Именно наличием изотопов объясняются те перестановки, которые в свое время. Современная наука подтвердила его правоту. Так, природный калий образован в основном атомами его легких изотопов, а аргон – тяжелых. Поэтому относительная атомная масса калия меньше, чем аргона, хотя порядковый номер (заряд) калия больше.
Большинство химических элементов представляет собой смеси изотопов. Например , природный хлор содержит изотопы с атомными массами 35 и 37. Относительная атомная масса 35,5 получена расчетным путем с учетом не только массы изотопов, но и содержания каждого из них в природе. Из-за того, что химические элементы имеют изотопы, а значения относительных атомных масс элементов – это усредненные по содержанию изотопов величины, они представляют собой дробные, а не целые числа.
Когда хотят подчеркнуть о каком именно изотопе идет речь, около химического знака слева вверху пишут значение относительной атомной массы атома этого изотопа, а слева внизу – заряд ядра, например 37Cl17.
1.2. Состояние электронов в атоме
Под состоянием электрона в атоме понимают совокупность информации об энергии определенного электрона и про странстве, в котором он находится. Мы уже знаем, что электрон в атоме не имеет траектории движения, то есть можно говорить лишь о вероятности нахождения его в пространстве вокруг ядра. Он может находиться в любой части этого пространства, окружающего ядро, и совокупность различных положений его рассматривают как электронное облако с определенной плотностью отрицательного заряда.
В. Гейзенберг ввел понятие о принципе неопределенности, то есть показал, что невозможно определить одновременно и точно энергию и местоположение электрона. Чем точнее определена энергия электрона, тем неопределеннее будет его положение, и наоборот, определив положение, нельзя определить энергию электрона. Область вероятности обнаружения электрона не имеет четких границ. Однако можно выделить пространство, где вероятность нахождения электрона будет максимальной.
Пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью.
Число энергетических уровней (электронных слоев) в атоме равно номеру периода в системе, к которому принадлежит химический элемент: у ато мов элементов первого периода - один энергетический уровень, второго периода - два, седьмого периода - семь.
Наибольшее число электронов на энергетическом уровне определяется по формуле
N = 2 n 2 ,
где N - максимальное число электронов; п - номер уровня или главное квантовое число. Следовательно, на первом, бли жайшем к ядру энергетическом уровне может находиться не более двух электронов;
на втором - не более 8;
на третьем - не более 18;
на четвертом - не более 32.
А как, в свою очередь, устроены энергетические уровни (электронные слои)?
Начиная со второго энергетического уровня (п = 2), каждый из уровней подразделяется на подуровни (подслои), несколько отличающиеся друг от друга энергией связи с ядром.
Число подуровней равно значению главного квантового числа: первый энергетический уровень имеет один подуровень; второй - два; третий - три; четвертый - четыре подуровня. Подуровни, в свою очередь, образованы орбиталями.
Каждому значению п соответствует число орбиталей, равное п2. По данным, представленным в таблице 1, можно проследить связь главного квантового числа п с числом подуровней, типом и числом орбиталей и максимальным числом электронов на подуровне и уровне.
s -Подуровень - первый, ближайший к ядру атома подуровень каждого энергетического уровня, состоит из одной s-орбитали;
р-подуровень - второй подуровень каждого, кроме первого, энергетического уровня, состоит из трехр-орбиталей;
d -подуровень - третий подуровень каждого, начиная с третьего, энергетического уровня, состоит из пяти d-орбиталей;
f -подуровень каждого, начиная с четвертого, энергетического уровня, состоит из семи - орбиталей.
На рисунке представлена схема, отражающая число, форму и положение в пространстве электронных орбиталей первых четырех электронных слоев отдельного атома.
1.3. Электронные конфигурации в атомах химических элементах
Швейцарский физик В. Паули в 1925 г. установил, что в атоме на одной орбитами может находиться не более двух электронов, имеющих противоположные (антипараллельные) спины (в переводе с английского «веретено »), то есть обладающих такими свойствами, которые условно можно представить себе как вращение электрона вокруг своей воображаемой оси: по часовой или против часовой стрелки. Этот принцип носит название принципа Паули.
Если на орбитали находится один электрон, то он называется неспаренным, если два, то это спаренные электроны, то есть электроны с противоположными спинами.
s-Орбиталь, как вы уже знаете, имеет сферическую форму. Электрон атома водорода (п = 1) располагается на этой орбитали и неспарен. Поэтому его электронная формула, или элек тронная конфигурация, будет записываться так: 1s1. В электронных формулах номер энергетического уровня обозначается цифрой, стоящей перед буквой (1...), латинской буквой обозначают подуровень (тип орбитали), а цифра, которая записывается справа вверху от буквы (как показатель степени), показывает число электронов на подуровне.
На втором энергетическом уровне (n = 2) имеется четыре орбитали: одна s и три р. Электроны s-орбитали второго уровня (2p-орбитали) обладают более высокой энергией, так как находятся на большем расстоянии от ядра, чем электроны ls-орбитали (n = 2)
Вообще, для каждого значения п существует одна s-орбиталь, но с соответствующим запасом энергии электронов на нем и, следовательно, с соответствующим диаметром, растущим по мере увеличения значения п.
р-Орбиталь имеет форму гантели или объемной восьмерки. Все три р-орбитали расположены в атоме взаимно перпендикулярно вдоль пространственных координат, проведенных через ядро атома. Следует подчеркнуть еще раз, что каждый энергетический уровень (электронный слой), начиная с п = 2, имеет три р-орбитали. С увеличением значения п электроны занимают. р-орбитали, расположенные на больших расстояниях от ядра и направленные по осям х, у, г.
У элементов второго периода (п = 2) заполняется сначала одна s-орбиталь, а затем три р-орбитали.
У элементов третьего периода заполняются соответственно 3s - и 3р-орбитали. Пять d-орбиталей третьего уровня при этом остаются свободными:
У элементов больших периодов (четвертого и пятого) первые два электрона занимают соответственно 4s - и 5s - орбитали.
Начиная с третьего элемента каждого большого периода, последующие десять электронов поступят на предыдущие 3d - и 4d - орбитали соответственно.
У элементов больших периодов - шестого и незавершенного седьмого - электронные уровни и подуровни заполняются электронами, как правило, так: первые два электрона поступят на внешний s-подуровень следующий один электрон (у La и Ас) на предыдущий d-подуровень. Затем последующие 14 электронов поступят на третий снаружи энергетический уровень на 4 f- и 5f-орбитали соответственно у лантаноидов и актиноидов:
Затем снова начнет застраиваться второй снаружи энергетический уровень (d-подуровень): у элементов побочных подгрупп: 73Та 2, 8, 18, 32, 11, 2; 104Rf 2, 8, 18, 32, 32, 10, 2, - и, наконец, только после полного заполнения десятью электронами d-подуровня будет снова заполняться внешний р-подуровень:
86Rn 2, 8, 18, 32, 18, 8.
Очень часто строение электронных оболочек атомов изображают с помощью энергетических или квантовых ячеек - записывают так называемые графические электронные формулы. Для этой записи используют следующие обозначения: каждая квантовая ячейка обозначается клеткой, которая соответствует одной орбитали; каждый электрон обозначается стрелкой, соответствующей направлению спина. При записи графической электронной формулы следует помнить два правила: принцип Паули , согласно которому в ячейке (орбитали) может быть не более двух электронов, но с антипараллельными спинами, и правило Ф. Хунда , согласно которому электроны занимают свободные ячейки (орбитали), располагаются в них сначала по одному и имеют при этом одинаковое значение спина, а лишь затем спариваются, но спины при этом по принципу Паули будут уже противоположно направленными.
1.4. Строение электронной оболочки атомов
В ходе химических реакций ядра атомов не изменяются. Этот вывод можно сделать из известного вам факта, что продукты реакции состоят из атомов тех же химических элементов, что и исходные вещества. Но что же происходит с атомами в ходе химических реакций? Существует ли связь между строением атома и проявлением тех или иных физических и химических свойств? Для ответа на вопросы надо сначала рассмотреть строение электронной оболочки атомов разных химических элементов.
Число электронов в атоме равно заряду его ядра. Электроны располагаются на разном удалении от ядра атома, группируясь в электронные слои. Чем ближе к ядру расположены электроны, тем прочнее они связаны с ядром.
Ядро атома водорода имеет заряд +1. В атоме только одни электрон и, естественно, одни электронный слой.
Следующий за водородом гелий. Не образует соединений с другими элементами, а значит, валентность не проявляет. Ядро атома гелия имеет заряд +2, вокруг него движутся два электрона, образуя один электронный слой. Атомы гелия не дают соединений с атомами других химических элементов, а это говорит о большой устойчивости его электронной оболочки. Электронные оболочки гелия и других атомов инертных газов называют завершенными.
Следующий элемент – литий. В атоме лития три электрона. Два из них находятся на первом, ближнем к ядру электронном слое, а третий образует второй внешний электронный слой. В атоме лития появился второй электронный слой. Находящийся на нем электрон более удален от ядра и слабее связан с ядром, чем два других.
Найдите в периодической таблице химический знак лития. От лития до неона закономерно возрастает заряд ядер атомов. Постепенно заполняется электронами второй электронный слой, и с ростом числа электронов на нем металлические свойства элементов постепенно ослабевают и сменяются нарастающими неметаллическими.
Фтор – самый активный неметалл, заряд его ядра +9, в его атоме два электронных слоя, содержащих 2 и 7 электронов. За фтором следует неон.
По свойствам элементы фтор и неон резко различаются. Неон инертен и так же, как гелий, не образует соединений. Значит, второй электронный слой, содержащий восемь электронов, является завершенным: электроны сформировали устойчивую систему, придавая атому инертность.
Если это так, то следующий элемент, атомы которого должны отличатся от атомов неона дополнительным протоном в ядре и электронном, будет иметь три электронных слоя. У атома этого элемента появится, таким образом, третий, внешний электронный слой, заселенный одним электроном. Этот элемент будет резко отличатся по свойствам от неона, он должен быть активным металлом, подобно литию, и проявлять в соединениях валентность, равную 1.
Данному описанию подходит элемент натрий. Он открывает третий период. Натрий – щелочной металл, еще более активный чем литий. Значит, наши предположения оказались верны. Единственный электрон внешнего электронного слоя атома натрия расположен дальше от ядра, чем внешний электрон лития, а потому еще слабее связан с ядром.
В ряду элементов от натрия до аргона вновь проявляется отмеченная выше закономерность: увеличивается число электронов, образующих внешний электронный слой атомов, металлические свойства простых веществ от натрия к алюминию ослабевают, неметаллические свойства усиливаются при переходе от кремния к фосфору и сере и наиболее ярко выражены у галогенов. В конце третьего периода находится элемент – аргон, в атоме которого завершенный, восьмиэлектронный внешний слой. При переходе от хлора к аргону резко изменяются свойства атомов элементов, а с ними и свойства простых веществ и соединений этого элемента. Известно, что аргон – инертный газ. Он не вступает в соединения с другими веществами.
Также резко изменяются свойства и при переходе от аргона – последнего элемента третьего периода к первому элементу четвертого периода – калию. Калий – щелочной металл, в химическом отношении очень активен.
Таким образом, количественные изменения в составе атома (число протонов в ядре и электронов на внешнем электронном слое) связаны с качественными (свойства простых веществ и соединений, образованных химическим элементом).
Систематизируем знания.
1. В электронной оболочке атома электроны расположены слоями. Первый от ядра слой завершен, когда на нем находятся два электрона, второй завершенный слой содержит восемь электронов.
2. Число электронных слоев в атоме совпадает с номером периода, в котором находится химический элемент
3. Электронная оболочка атома каждого следующего элемента в периодической системе повторяет строение электронной оболочки предыдущего элемента, но отличается от нее на один электрон.
Изученного вам достаточно, чтобы сделать выводы о взаимосвязи строения атомов и свойства химических элементов, понять причины периодического изменения их свойств, сходства и различия. Сформулировать эти выводы.
1. Свойства химических элементов, расположенных в порядке возрастания зарядов ядер атомов, изменяются периодически потому, что периодически повторяется сходное строение внешнего электронного слоя атомов .
2. Плавное изменение свойств элементов в пределах одного периода обусловлено постепенным увеличением числа электронов на внешнем слое атомов.
3. Завершение внешнего электронного слоя атома приводит к резкому скачку в свойствах при переходе от галогена к инертному газу; появление нового внешнего электронного слоя в атоме – причина резкого скачка в свойствах при переходе от инертного газа к щелочному металлу.
4. Свойства химических элементов, принадлежащих к одному семейству, сходны потому, что на внешнем электронном слое их атомов находится одинаковое число электронов.
1.5. Валентные возможности атомов химических элементов
Строение наружных энергетических уровней атомов химических элементов и определяет в основном свойства их атомов. Поэтому эти уровни называют валентными. Электроны этих уровней, а иногда и предвнешних уровней могут принимать участие в образовании химических связей. Такие электроны также называют валентными.
Валентность атома химического элемента определяется в первую очередь числом неспаренных электронов, принимающих участие в образовании химической связи .
Валентные электроны атомов элементов главных подгрупп расположены на s - и p-орбиталях внешнего электронного слоя. У элементов побочных подгрупп, кроме лантаноидов и актиноидов, валентные электроны расположены на s-орбитали внешнего и d-орбиталях предвнешнего слоев.
Для того чтобы верно оценить валентные возможности атомов химических элементов, нужно рассмотреть распределение электронов в них по энергетическим уровням и подуровням и определить число неспаренных электронов в соответствии с принципом Паули и правилом Хунда для невозбужденного (основного, или стационарного) состояния атома и для возбужденного (то есть получившего дополнительную энергию, в результате чего происходит распаривание электронов внешнего слоя и переход их на свободные орбитали). Атом в возбужденном состоянии обозначают соответствующим символом элемента со звездочкой.
https://pandia.ru/text/80/139/images/image003_118.gif" height="757">Например, рассмотрим валентные возможности атомов фосфора в стационарном и возбужденном состояниях:
https://pandia.ru/text/80/139/images/image006_87.jpg" width="384" height="92 src=">
Затраты энергии на возбуждение атомов углерода с избытком компенсируются энергией, выделяющейся при образова нии двух дополнительных ковалентных связей. Так, для перевода атомов углерода из стационарного состояния 2s22p2 в возбужденное - 2s12p3 требуется затратить около 400 кДж/моль энергии. Но при образовании С-Н-связи в предельных углеводородах выделяется 360 кДж/моль. Следовательно, при образовании двух молей С-Н-связей выделится 720 кДж, что превышает энергию перевода атомов углерода в возбужденное состояние на 320 кДж/моль.
В заключение следует отметить, что валентные возможности атомов химических элементов далеко не исчерпываются числом неспаренных электронов в стационарном и возбужденном состояниях атомов. Если вы вспомните донорно-акцепторный механизм образования ковалентных связей, то вам станут понятны и две другие валентные возможности атомов химических элементов, которые определяются наличием свободных орбиталей и наличием неподеленных электронных пар, способных дать ковалентную химическую связь по донорно-акцепторному механизму. Вспомните образование иона аммония NH4+ (Более подробно мы рассмотрим реализацию этих валентных возможностей атомами химических элементов при изучении химической связи.)
Сделаем общий вывод.
Валентные возможности атомов химических элементов определяются: 1) числом неспаренных электронов (одноэлектронных орбиталей); 2) наличием свободных орбиталей; 3) наличием неподеленных пар электронов.

Состав атома.
Атом состоит из атомного ядра и электронной оболочки .
Ядро атома состоит из протонов (p + ) и нейтронов (n 0). У большинства атомов водорода ядро состоит из одного протона.
Число протонов N (p + ) равно заряду ядра (Z ) и порядковому номеру элемента в естественном ряду элементов (и в периодической системе элементов).
N (p +) = Z
Сумма числа нейтронов N (n 0), обозначаемого просто буквой N , и числа протонов Z называется массовым числом и обозначается буквой А .
A = Z + N
Электронная оболочка атома состоит из движущихся вокруг ядра электронов (е -).
Число электронов N (e -) в электронной оболочке нейтрального атома равно числу протонов Z в его ядре.
Масса протона примерно равна массе нейтрона и в 1840 раз больше массы электрона, поэтому масса атома практически равна массе ядра.
Форма атома - сферическая. Радиус ядра примерно в 100000 раз меньше радиуса атома.
Химический элемент - вид атомов (совокупность атомов) с одинаковым зарядом ядра (с одинаковым числом протонов в ядре).
Изотоп - совокупность атомов одного элемента с одинаковым числом нейтронов в ядре (или вид атомов с одинаковым числом протонов и одинаковым числом нейтронов в ядре).
Разные изотопы отличаются друг от друга числом нейтронов в ядрах их атомов.
Обозначение отдельного атома или изотопа: (Э - символ элемента), например: .
Строение электронной оболочки атома
Атомная орбиталь - состояние электрона в атоме. Условное обозначение орбитали - . Каждой орбитали соответствует электронное облако.
Орбитали реальных атомов в основном (невозбужденном) состоянии бывают четырех типов: s , p , d и f .
Электронное облако - часть пространства, в которой электрон можно обнаружить с вероятностью 90 (или более) процентов.
Примечание : иногда понятия "атомная орбиталь" и "электронное облако" не различают, называя и то, и другое "атомной орбиталью".
Электронная оболочка атома слоистая. Электронный слой образован электронными облаками одинакового размера. Орбитали одного слоя образуют электронный ("энергетический") уровень , их энергии одинаковы у атома водорода, но различаются у других атомов.
Однотипные орбитали одного уровня группируются в электронные (энергетические)
подуровни:
s
-подуровень (состоит из одной s
-орбитали), условное обозначение - .
p
-подуровень (состоит из трех p
d
-подуровень (состоит из пяти d
-орбиталей), условное обозначение - .
f
-подуровень (состоит из семи f
-орбиталей), условное обозначение - .
Энергии орбиталей одного подуровня одинаковы.
При обозначении подуровней к символу подуровня добавляется номер слоя (электронного уровня), например: 2s , 3p , 5d означает s -подуровень второго уровня, p -подуровень третьего уровня, d -подуровень пятого уровня.
Общее число подуровней на одном уровне равно номеру уровня n . Общее число орбиталей на одном уровне равно n 2 . Соответственно этому, общее число облаков в одном слое равно также n 2 .
Обозначения: - свободная орбиталь (без электронов), - орбиталь с неспаренным электроном, - орбиталь с электронной парой (с двумя электронами).
Порядок заполнения электронами орбиталей атома определяется тремя законами природы (формулировки даны упрощенно):
1. Принцип наименьшей энергии - электроны заполняют орбитали в порядке возрастания энергии орбиталей.
2. Принцип Паули - на одной орбитали не может быть больше двух электронов.
3. Правило Хунда - в пределах подуровня электроны сначала заполняют свободные орбитали (по одному), и лишь после этого образуют электронные пары.
Общее число электронов на электронном уровне (или в электронном слое) равно 2n 2 .
Распределение подуровней по энергиям выражается рядом (в прядке увеличения энергии):
1s , 2s , 2p , 3s , 3p , 4s , 3d , 4p , 5s , 4d , 5p , 6s , 4f , 5d , 6p , 7s , 5f , 6d , 7p ...
Наглядно эта последовательность выражается энергетической диаграммой:
Распределение электронов атома по уровням, подуровням и орбиталям (электронная конфигурация атома) может быть изображена в виде электронной формулы, энергетической диаграммы или, упрощенно, в виде схемы электронных слоев ("электронная схема").
Примеры электронного строения атомов:
Валентные электроны - электроны атома, которые могут принимать участие в образовании химических связей. У любого атома это все внешние электроны плюс те предвнешние электроны, энергия которых больше, чем у внешних. Например: у атома Ca внешние электроны - 4s 2 , они же и валентные; у атома Fe внешние электроны - 4s 2 , но у него есть 3d 6 , следовательно у атома железа 8 валентных электронов. Валентная электронная формула атома кальция - 4s 2 , а атома железа - 4s 2 3d 6 .
Периодическая система химических элементов Д. И. Менделеева
(естественная система химических элементов)
Периодический закон химических элементов (современная формулировка): свойства химических элементов, а также простых и сложных веществ, ими образуемых, находятся в периодической зависимости от значения заряда из атомных ядер.
Периодическая система - графическое выражение периодического закона.
Естественный ряд химических элементов - ряд химических элементов, выстроенных по возрастанию числа протонов в ядрах их атомов, или, что то же самое, по возрастанию зарядов ядер этих атомов. Порядковый номер элемента в этом ряду равен числу протонов в ядре любого атома этого элемента.
Таблица химических элементов строится путем "разрезания" естественного ряда химических элементов на периоды (горизонтальные строки таблицы) и объединения в группы (вертикальные столбцы таблицы) элементов, со сходным электронным строением атомов.
В зависимости от способа объединения элементов в группы таблица может быть длиннопериодной (в группы собраны элементы с одинаковым числом и типом валентных электронов) и короткопериодной (в группы собраны элементы с одинаковым числом валентных электронов).
Группы короткопериодной таблицы делятся на подгруппы (главные и побочные ), совпадающие с группами длиннопериодной таблицы.
У всех атомов элементов одного периода одинаковое число электронных слоев, равное номеру периода.
Число элементов в периодах: 2, 8, 8, 18, 18, 32, 32. Большинство элементов восьмого периода получены искусственно, последние элементы этого периода еще не синтезированы. Все периоды, кроме первого начинаются с элемента, образующего щелочной металл (Li, Na, K и т. д.), а заканчиваются элементом, образующим благородный газ (He, Ne, Ar, Kr и т. д.).
В короткопериодной таблице - восемь групп, каждая из которых делится на две подгруппы (главную и побочную), в длиннопериодной таблице - шестнадцать групп, которые нумеруются римскими цифрами с буквами А или В, например: IA, IIIB, VIA, VIIB. Группа IA длиннопериодной таблицы соответствует главной подгруппе первой группы короткопериодной таблицы; группа VIIB - побочной подгруппе седьмой группы: остальные - аналогично.
Характеристики химических элементов закономерно изменяются в группах и периодах.
В периодах (с увеличением порядкового номера)
- увеличивается заряд ядра,
- увеличивается число внешних электронов,
- уменьшается радиус атомов,
- увеличивается прочность связи электронов с ядром (энергия ионизации),
- увеличивается электроотрицательность,
- усиливаются окислительные свойства простых веществ ("неметалличность"),
- ослабевают восстановительные свойства простых веществ ("металличность"),
- ослабевает основный характер гидроксидов и соответствующих оксидов,
- возрастает кислотный характер гидроксидов и соответствующих оксидов.
В группах (с увеличением порядкового номера)
- увеличивается заряд ядра,
- увеличивается радиус атомов (только в А-группах),
- уменьшается прочность связи электронов с ядром (энергия ионизации; только в А-группах),
- уменьшается электроотрицательность (только в А-группах),
- ослабевают окислительные свойства простых веществ ("неметалличность"; только в А-группах),
- усиливаются восстановительные свойства простых веществ ("металличность"; только в А-группах),
- возрастает основный характер гидроксидов и соответствующих оксидов (только в А-группах),
- ослабевает кислотный характер гидроксидов и соответствующих оксидов (только в А-группах),
- снижается устойчивость водородных соединений (повышается их восстановительная активность; только в А-группах).
Задачи и тесты по теме "Тема 9. "Строение атома. Периодический закон и периодическая система химических элементов Д. И. Менделеева (ПСХЭ)"."
- Периодический закон - Периодический закон и строение атомов 8–9 класс
Вы должны знать: законы заполнения орбиталей электронами (принцип наименьшей энергии, принцип Паули, правило Хунда), структуру периодической системы элементов.Вы должны уметь: определять состав атома по положению элемента в периодической системе, и, наоборот, находить элемент в периодической системе, зная его состав; изображать схему строения, электронную конфигурацию атома, иона, и, наоборот, определять по схеме и электронной конфигурации положение химического элемента в ПСХЭ; давать характеристику элемента и образуемых им веществ по его положению в ПСХЭ; определять изменения радиуса атомов, свойств химических элементов и образуемых ими веществ в пределах одного периода и одной главной подгруппы периодической системы.
Пример 1. Определите количество орбиталей на третьем электронном уровне. Какие это орбитали?
Для определения количества орбиталей воспользуемся формулой N орбиталей = n 2 , где n - номер уровня. N орбиталей = 3 2 = 9. Одна 3s -, три 3p - и пять 3d -орбиталей.Пример 2. Определите, у атома какого элемента электронная формула 1s 2 2s 2 2p 6 3s 2 3p 1 .
Для того, чтобы определить, кокой это элемент, надо выяснить его порядковый номер, который равен суммарному числу электронов атома. В данном случае: 2 + 2 + 6 + 2 + 1 = 13. Это алюминий.Убедившись, что все необходимое усвоено, переходите к выполнению заданий. Желаем успехов.
Рекомендованная литература:- О. С. Габриелян и др. Химия 11 кл. М., Дрофа, 2002;
- Г. Е. Рудзитис, Ф. Г. Фельдман. Химия 11 кл. М., Просвещение, 2001.