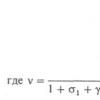Наиболее распространенным способом поступления токсических веществ в организм является пероральный. Токсическое действие на человека опасных химических веществ Пути поступления токсических химических веществ в организм
Министерство образования и науки Российской Федерации
Муромский институт (филиал)
федерального государственного бюджетного образовательного учреждения
высшего профессионального образования
«Владимирский государственный университет
имени Александра Григорьевича и Николая Григорьевича Столетовых»
(МИ (филиал) ВлГУ)
Кафедра техносферной безопасности
Практическое занятие №3
Методические указания к выполнению практической работы по дисциплине «Токсикология»
для студентов направления 280700.62 «Техносферная безопасность»
Пути поступления токсических веществ в организм.
Согласно варианта задания:
1. Описать механизм резорбции химического вещества через кожные покровы организма (перкутанно).
2. Описать механизм резорбции химического вещества через слизистые оболочки организма (ингаляционно).
3. Описать механизм резорбции химического вещества через слизистые оболочки организма (перорально).
Таблица 1
|
№ варианта |
Порядковый номер вещества по ГН 2.2.5.1313-03 |
Примечание |
||
Для определения полных характеристик веществ использовать данные INTERNET а
Материалы, необходимые для выполнения практической работы.
1. Пути поступления токсических химических веществ в организм
Токсические химические вещества (токсиканты) могут поступать в организм через кожные покровы (перкутанно), дыхательные пути (ингаляционно), желудочно-кишечный тракт (перорально). Поступление токсиканта из окружающей среды в кровеносную и лимфатическую системы организма называется резорбцией, а действие токсиканта при этом – резорбтивным (системным) действием. Токсические вещества могут оказывать местное действие на кожу, слизистые оболочки и при этом не поступать в кровеносную или лимфатическую системы (резорбция отсутствует). Токсиканты обладают способностью к местному и резорбтивному действиям.
Путь поступления вещества в организм определяется его агрегатным состоянием, месторасположением в окружающей среде, площадью соприкосновения с организмом. Так, вещество в форме пара имеет очень высокую вероятность всасываться в дыхательных путях, но не может попасть в организм через желудочно-кишечный тракт и кожные покровы.
Скорость и характер резорбции веществ определяется рядом факторов: особенностями организма; количеством и свойствами вещества; параметрами окружающей среды. Поэтому качественные и количественные характеристики резорбции токсиканта могут изменяться в широких пределах.
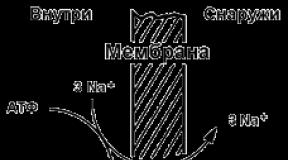
Резорбция через кожные покровы. Поверхностный роговой слой эпидермиса препятствует резорбции токсикантов. Кожа представляет собой электрически заряженную мембрану, где и осуществляется метаболизм токсических химических веществ в количестве 2-6% относительно метаболической активности печени.
Поступление веществ через кожу осуществляется тремя путями: через эпидермис; через сальные и потовые железы; через волосяные фолликулы. Для хорошо проникающих через кожу низкомолекулярных и липофильных соединений основным является трансэпидермальный путь. Медленно всасывающиеся вещества поступают трансфолликулярным и трансгландулярным путями. Напр., хорошо растворяющиеся в жирах сернистый и азотистый иприты проникают через кожу трансэпидермально.
При трансэпидермальном проникновении веществ возможно прохождение их через клетки и через межклеточные пространства. Рассматривая прохождение веществ через кожу, следует различать собственно резорбцию (поступление в кровь) и местное действие
(депонирование веществ в коже). Проникновение ксенобиотиков через кожу представляет
собой процесс пассивной диффузии. На скорость резорбции влияют площадь и локализация резорбирующей поверхности, интенсивность кровоснабжения кожи, а также свойства токсиканта. Количество вещества, проникающего через кожу, пропорционально площади контакта вещества и кожи. С увеличением площади увеличивается и количество всасываемого вещества. При действии веществ в форме аэрозоля площадь воздействия с кожей увеличивается с одновременным уменьшением диаметра частиц.
Кровоснабжение кожи меньше, чем других тканей и органов, напр., мышц. При усилении кожного кровотока увеличивается возможность токсических веществ проникать через кожные покровы. Действие раздражающих веществ, ультрафиолетовое облучение, температурное воздействие, сопровождающееся расширением сосудов, открытием анастомозов, усиливает резорбцию токсикантов.
На резорбцию влияют физико-химические свойства токсикантов, прежде всего способность растворяться в липидах (липофильность). Существует отчетливая корреляция между величиной коэффициента распределения в системе масло/вода и скоростью резорбции.
Липофильные агенты (напр., ФОС, иприты, хлорированные углеводы) легко преодолевают кожный барьер. Гидрофильные агенты, особенно заряженные молекулы, практически не проникают через кожу. В этой связи проницаемость барьера для слабых кислот и оснований существенно зависит от степени их диссоциации. Так, салициловая кислота и нейтральные молекулы алкалоидов способны к резорбции, однако анионы кислоты и катионы алкалоидов таким путем в организм не проникают. Вместе с тем проникновение в организм липофильных веществ, вообще не растворяющихся в воде, также невозможно: они депонируются в жировой смазке и эпидермисе и не захватываются кровью. Поэтому масла не проникают через кожу. Кислород, азот, диоксид углерода, сероводород, аммиак, гелий, водород способны к кожной резорбции. Увеличение парциального давления газа в воздухе ускоряет его проникновение в организм, что может приводить к тяжелым интоксикациям.
Повреждение рогового слоя эпидермиса и жировой смазки кожи кератолитическими средствами и органическими растворителями усиливает резорбцию токсикантов. Механическое повреждение кожи с образованием дефектов, особенно обширных, лишает ее барьерных свойств. Через увлажненную кожу токсиканты всасываются лучше, чем через сухую. На скорость резорбции веществ, наносимых в виде эмульсий, растворов, мазей, оказывают влияние свойства носителя (растворителя, эмульгатора, мазевой основы).
Резорбция через слизистые оболочки. Слизистые оболочки не имеют рогового слоя и жировой пленки на поверхности. Они покрыты водной пленкой, через которую вещества легко проникают в ткани организма. Резорбция веществ через слизистые определяется главным образом следующими факторами:
а) агрегатным состоянием вещества (газ, аэрозоль, взвесь, раствор);
б) дозой и концентрацией токсиканта;
в) видом слизистой оболочки, ее толщиной;
г) продолжительностью контакта;
д) интенсивностью кровоснабжения анатомической структуры;
е) дополнительными факторами (параметры среды, степень наполнения желудка).
Большая площадь поверхности, малая толщина слизистых и хорошее кровоснабжение делают наиболее вероятным проникновение веществ через органы дыхания и стенку тонкой кишки.
Многие токсиканты достаточно быстро всасываются уже в ротовой полости . Эпителий полости рта не представляет собой значительной преграды на пути ксенобиотиков. В резорбции участвуют все отделы ротовой полости. Проникать через слизистые могут лишь вещества, находящиеся в полости рта в молекулярной форме. Поэтому растворы лучше резорбируются, чем взвеси. Раствор обволакивает всю поверхность слизистой ротовой полости, покрывая ее пленкой, которая содержит токсические вещества. Кровь, оттекающая от слизистой полости рта, поступает в верхнюю полую вену, и поэтому вещество попадает непосредственно в сердце, в малый круг кровообращения, а затем и в общий кровоток. В отличие от других способов проникновения через слизистые желудочно-кишечного тракта, при резорбции в ротовой полости всосавшиеся токсиканты распределяются в организме, минуя печень, что влияет на биологическую активность быстро разрушающихся соединений.
В основе резорбции веществ в желудке – механизмы простой диффузии. Фактор, определяющий особенности желудка, – кислотность желудочного содержимого. Скорость диффузии определяется коэффициентом распределения веществ в системе масло/вода. Жирорастворимые (или растворимые в неполярных органических растворителях) соединения достаточно легко проникают через слизистую желудка в кровь.
Особенностью резорбции в желудке является то, что она осуществляется из среды с низким значением рН. В этой связи эпителий слизистой формирует своего рода липидный барьер между водными фазами: кислой (кислотность желудочного сока примерно равна 1) и щелочной (рН крови равен 7,4). Этот барьер токсиканты могут преодолеть лишь в форме незаряженных молекул. Многие соединения не способны к диссоциации в водных растворах (неэлектролиты), их молекулы не несут заряда, и они легко проходят через слизистую желудка (дихлорэтан, четыреххлористый углерод). Сильные кислоты и щелочи (серная, соляная, азотная кислоты, NaOH, KOH) в любом растворе полностью диссоциированы и потому переходят в кровь лишь в случае разрушения слизистой оболочки (химический ожог).
Для слабых кислот кислая среда способствует превращению вещества в неионизированную форму, для слабых оснований низкие значения рН (высокие концентрации водородных ионов в среде) способствуют превращению веществ в ионизированную форму.
Неионизированные молекулы более липофильны, они легче проникают через биологический барьер. Поэтому в желудке лучше абсорбируются слабые кислоты.
Необходимое условие резорбции вещества в желудке – его растворимость в желудочном соке. Поэтому не растворимые в воде вещества в желудке не всасываются. Взвеси химических соединений перед всасыванием должны перейти в раствор. Поскольку время нахождения в желудке ограниченно, взвеси действуют слабее, чем растворы того же вещества.
Если токсикант поступает в желудок с пищей, возможно взаимодействие с ее компонентами: растворение в жирах и воде, абсорбция белками. Величина концентрации ксенобиотика при этом снижается, уменьшается и скорость диффузии в кровь. Из пустого желудка вещества всасываются лучше, чем из наполненного.
Резорбция в кишечнике. Кишечник – одно из основных мест всасывания химических веществ. Здесь действует механизм пассивной диффузии веществ через эпителий. Пассивная диффузия в кишечнике – это дозо-зависимый процесс. При увеличении содержания токсиканта в кишечнике увеличивается и скорость его всасывания. Через слизистые кишечника проникают ионы слабых кислот и оснований, что обусловлено диффузией их через поры биологических мембран.
Скорость диффузии веществ через слизистую оболочку тонкой кишки пропорциональна величине коэффициента распределения в системе масло/вода. Вещества, не растворимые в липидах, даже в форме незаряженных молекул не проникают через слизистую кишечника. Так, ксилоза – низкомолекулярное соединение, относящееся к группе неэлектролитов, но не растворимое в липидах, – практически не поступает во внутренние среды организма при приеме через рот. Токсические вещества, хорошо растворяющиеся в жирах, не всасываются в кишечнике из-за их низкой растворимости в воде. С увеличением молекулярной массы проникновение химических соединений через слизистую кишечника уменьшается. Трехвалентные ионы вообще не всасываются в кишечнике.
С наивысшей скоростью всасывание происходит в тонкой кишке. Холодные растворы быстрее покидают желудок. В этой связи холодные растворы токсикантов порой оказываются более токсичными, чем теплые. Резорбция в толстой кишке происходит сравнительно медленно. Этому способствует не только меньшая площадь поверхности слизистой этого отдела, но и более низкая концентрация токсикантов в просвете кишки.
Кишечник имеет разветвленную сеть кровеносных сосудов, поэтому вещества, проникающие через слизистую оболочку, быстро уносятся оттекающей кровью. Содержимое толстой кишки может выступать в качестве инертного наполнителя, в который включено вещество и из которого замедляется его резорбция; при этом количество всасывающегося вещества остается неизменным.
Желчные кислоты, обладая свойствами эмульгаторов, способствуют всасыванию жиров. Микрофлора кишечника может вызвать химическую модификацию молекул токсикантов, – напр., способствует восстановлению нитратов до нитритов у грудных детей. Ионы этих нитритов проникают в кровь и вызывают образование метгемоглобина. Кишечная палочка содержит ферменты, под влиянием которых в кишечнике расщепляются глюкурониды. Конъюгаты ксенобиотиков с глюкуроновой кислотой (конечные метаболиты веществ, выделяющиеся в кишечник с желчью) плохо растворимы в жирах и хорошо растворимы в воде соединения. После отщепления глюкуроновой кислоты липофильность отделившихся молекул существенно возрастает, и они приобретают способность к обратной резорбции в кровоток. Этот процесс – основа феномена печеночно-кишечной циркуляции токсиканта.
Резорбция в легких. Кислород и другие газообразные вещества при выдыхании проникают через легкие в кровоток через тонкий капиллярно-альвеолярный барьер. Благоприятное условие всасывания веществ – большая площадь поверхности легких, составляющая у человека в среднем 70 м2. Продвижение газов по дыхательным путям сопряжено с их частичной адсорбцией на поверхности трахеи и бронхов. Чем хуже растворяется вещество в воде, тем глубже оно проникает в легкие. Ингаляционно в организм могут поступать не только газы и пары, но и аэрозоли, которые также достаточно быстро всасываются в кровь.
Процесс проникновения и распределения газов в организме представлен в виде нескольких последовательных этапов:
ингалируемый газ поступает через носоглотку и трахеи в альвеолы легких;
путем диффузии попадает в кровь и растворяется в ней;
током крови разносится по организму;
путем диффузии проникает в межклеточную жидкость и клетки тканей.
Для резорбции вдыхаемый газ должен вступить в контакт с альвеолярной поверхностью легких. Альвеолы расположены глубоко в легочной ткани, поэтому путем простой диффузии газ не сможет быстро преодолеть расстояние от полости носа или ротового отверстия до их стенок. У человека и других позвоночных, дышащих легкими, есть механизм, с помощью которого осуществляется механическое перемешивание (конвекция) газов в дыхательных путях и легких и обеспечивается постоянный обмен газами между внешней средой и организмом. Этот механизм вентиляции легких – последовательно сменяющие друг друга акты вдоха и выдоха.
Вентиляция легких обеспечивает быструю доставку газа из окружающей среды к поверхности альвеолярных мембран. Одновременно с вентиляцией легких осуществляются растворение газа в стенке альвеолы, диффузия его в кровь, конвекция в кровяном русле, диффузия в ткани. При снижении парциального давления газа в альвеолярном воздухе относительно крови газ из организма устремляется в просвет альвеол и удаляется во внешнюю среду. С помощью форсированной вентиляции легких можно быстро снизить концентрацию газообразного вещества в крови и тканях. Эту возможность используют для помощи отравленным газообразными или летучими веществами, вводя им карбоген (воздух с повышенным содержанием углекислого газа), который стимулирует вентиляцию легких, воздействуя на дыхательный центр головного мозга.
Из альвеолы в кровоток газ переходит посредством диффузии. При этом молекула соединения перемещается из газообразной среды в жидкую фазу. Поступление вещества зависит от следующих факторов: растворимости газа в крови; градиента концентрации газа между альвеолярным воздухом и кровью; интенсивности кровотока и состояния легочной ткани.
Растворимость в крови отличается от растворимости в воде, что связано с наличием растворенных в плазме крови ее составных частей (соли, липиды, углеводы, белки) и форменных элементов (лейкоциты, эритроциты). Повышение температуры снижает растворимость газов в жидкостях. Количество газа, растворенного в жидкости, всегда пропорционально величине его парциального давления.
При резорбции газов в кровь большую роль играет интенсивность легочного кровотока. Она идентична минутному объему сердечного выброса. Чем выше минутный объем, тем больше крови в единицу времени попадает в альвеолярные капилляры, тем больше газа уносится оттекающей от легких кровью и переносится к тканям, тем быстрее устанавливается равновесие в системе распределения газа между средой и тканями. Стенка капилляра в норме не представляет собой существенного препятствия для диффундирующих газов. Проникновение газов в кровь затруднено только в патологически измененных легких (отек, клеточная инфильтрация альвеолярно-капиллярного барьера).
Кровь, насыщенная в легких газом, распространяется по организму. Вследствие более высокого содержания в крови молекулы газа диффундируют в ткани. Кровь, освободившаяся от газа, возвращается к легким. Этот процесс повторяется, пока парциальное давление газа в тканях не выравняется с давлением в крови, а давление в крови – с давлением в алвеолярном воздухе (состояние равновесия).
Диффузия газов в ткани определяется: растворимостью газов в тканях, разницей концентрации газа в крови и тканях и интенсивностью кровоснабжения тканей. Эпителий дыхательного тракта и стенки капиллярного русла обладают проницаемостью пористой мембраны. Поэтому жирорастворимые вещества резорбируются быстро, а растворимые в воде – в зависимости от размеров их молекул. Насыщение веществ, проникающих через альвеолярно-капиллярный барьер, не наступает. Через барьер проникают даже крупные белковые молекулы, – напр., инсулина, ботулотоксина.
Проникновение токсикантов через слизистую глаз определяется физико-химическими свойствами вещества (растворимостью в липидах и воде, зарядом и размерами молекулы).
Липидный барьер роговицы глаза представляет собой тонкую структуру многослойного плоского эпителия, покрытого снаружи роговым слоем. Через этот барьер легко проникают жирорастворимые вещества и даже растворимые в воде соединения. При попадании токсиканта на роговицу большая его часть смывается слезами и распространяется по поверхности склеры и конъюнктивы глаз. Около 50% нанесенного на роговицу вещества удаляется в течение 30 сек., и более 85% – в течение 3-6 мин.
Резорбция из тканей. При действии веществ на раневые поверхности или введении в ткань (напр., подкожно или внутримышечно) возможно их поступление либо непосредственно в кровь, либо сперва в ткани, а уже затем в кровь. При этом в ткань могут проникать высокомолекулярные (белковые), водорастворимые и даже ионизированные молекулы. Создающийся градиент концентрации токсиканта между местом аппликации, окружающей тканью и кровью – движущая сила резорбции вещества в кровь и внутренние среды организма. Скорость резорбции определяется свойствами тканей и токсических веществ.
Свойства тканей. Стенка капилляра представляет собой пористую мембрану. Ее толщина в различных тканях колеблется от 0,1 до 1 мкм. Для капилляров большинства тканей человека характерны поры диаметром около 2 нм. Поверхность, занятая порами, составляет около 0,1% площади капиллярного русла. Поры представляют собой промежутки между эндотелиальными клетками. Поры делают мембрану капилляра проницаемой для водорастворимых веществ (в ограниченном количестве встречаются поры и с большим диаметром – до 80 нм). Кроме того, возможен перенос веществ через стенку капилляра через механизм пиноцитоза (образование везикул на мембране рецептора).
Стенки капилляров мышц млекопитающих имеют поры диаметром 3-4 нм, поэтому они непроницаемы для гемоглобина (r = 3,2 нм) и сывороточных альбуминов (r = 3,5 нм), но проницаемы для таких веществ как инулин (r = 1,5 нм) и миоглобин (r = 2 нм). В этой связи проникновение очень многих ксенобиотиков в кровь возможно при их введении в мышцы.
Капиллярная и лимфатическая системы. Сеть капилляров и лимфатических сосудов хорошо развита в подкожной клетчатке и в межмышечной соединительной ткани. Площадь поверхности капиллярного русла в объеме тканей оценивается по-разному. Для мышц ее величина составляет 7000-80000 см2/100 г ткани. Степень развития капиллярной сети ограничивает скорость резорбции ксенобиотика в ткани.
Время пребывания крови в капиллярах в процессе кровообращения составляет примерно 25 сек., в то время как оборот объема циркулирующей крови реализуется за 1 мин. Это считают причиной того, что степень резорбции вещества из ткани в кровь пропорциональна степени вазкуляризации тканей. Резорбция веществ из подкожной клетчатки в основном осуществляется через капилляры и в значительно меньшей степени – через лимфатические сосуды.
Для кровоснабжения тканей имеют значение процент раскрытых, функционирующих капилляров, а также величина давления крови в тканях. Интенсивность кровотока зависит от сердечной деятельности, а в тканях она регулируется вазоактивными факторами. Эндогенные регуляторы – адреналин, норадреналин, ацетилхолин, серотонин, оксид азота, эндотелий – зависимые релаксирующие факторы, простогландины влияют на скорость кровотока в ткани и следовательно на резорбцию токсических веществ. Охлаждение конечности замедляют в ней кровоток, нагревание – ускоряет его.
Выделяют следующие пути поступления ядов в организм:
1. пероральный;
2. ингаляционный;
3. перкутанный (через неповрежденную и поврежденную кожу);
4. через слизистые оболочки (конъюнктива глаза);
5. парентеральный.
Одним из распространенных способов поступления токсичных веществ в организм является пероральный. Ряд ядовитых жирорастворимых соединений – фенолы, некоторые соли, особенно цианиды – всасываются и поступают в кровь уже в полости рта.
На протяжении желудочно-кишечного тракта существуют значительные градиенты рН, определяющие различную скорость всасывания токсичных веществ. Токсичные вещества в желудке могут сорбироваться и разбавляться пищевыми массами, в результате чего уменьшается их контакт со слизистой оболочкой. Кроме того, на скорость всасывания влияют интенсивность кровообращения в слизистой оболочке желудка, перистальтика, количество слизи и т.д. В основном всасывание ядовитого вещества происходит в тонкой кишке, содержимое которой имеет рН 7,5 – 8,0. Колебания рН кишечной среды, наличие ферментов, большое количество соединений, образующихся в процессе пищеварения в химусе на крупных белковых молекулах и сорбция на них, - все это влияет на резорбцию ядовитых соединений и их депонирование в желудочно-кишечном тракте.
Явления депонирования токсичных веществ в желудочно-кишечном тракте при пероральных отравлениях свидетельствуют о необходимости его тщательного очищения в процессе лечения.
Ингаляционные отравления характеризуются наиболее быстрым поступлением яда в кровь. Это объясняется большой поверхностью всасывания легочных альвеол (100-150 м 2), малой толщиной альвеолярных мембран, интенсивным током крови по легочным капиллярам и отсутствием условий для значительного депонирования ядов.
Всасывание летучих соединений начинается уже в верхних дыхательных путях, но наиболее полно осуществляется в легких. Происходит оно по закону диффузии в соответствии с градиентом концентрации. Подобным образом поступают в организм многие летучие неэлектролиты: углеводороды, галогеноуглеводороды, спирты, эфиры и т.д. Скорость поступления определяется их физико-химическими свойствами и в меньшей степени состоянием организма (интенсивность дыхания и кровообращения в легких).
Проникновение токсичных веществ через кожу также имеет большое значение, преимущественно в военных и производственных условиях.
Существует по крайней мере три пути такого поступления:
1. через эпидермис;
2. волосяные фолликулы;
3. выводные протоки сальных и потовых желез.
Эпидермис рассматривается как липопротеиновый барьер, через который могут диффундировать разнообразные вещества в количествах, пропорциональных их коэффициентам распределения в системе липиды/вода . Это только первая фаза проникновения яда, второй фазой является транспорт этих соединений из дермы в кровь. Механические повреждения кожи (ссадины, царапины, раны и т.д.), термические и химические ожоги способствуют проникновению токсичных веществ в организм.
Распределение ядов в организме. Одним из основных токсикологических показателей является объем распределения, т.е. характеристика пространства, в котором распределяется данное токсичное вещество. Существует три главных сектора распределения чужеродных веществ: внеклеточная жидкость (примерно 14 л для человека массой тела 70 кг), внутриклеточная жидкость (28 л) и жировая ткань, объем которой значительно варьирует. Объем распределения зависит от трех основных физико-химических свойств данного вещества:
1. водорастворимости;
2. жирорастворимости;
3. способности к диссоциации (ионообразованию).
Водорастворимые соединения способны распространяться во всем водном секторе (внеклеточная и внутриклеточная жидкость) организма – около 42 л; жирорастворимые вещества накапливаются (депонируются) преимущественно в липидах.
Выведение ядов из организма . Пути и способы естественного выведения чужеродных соединений из организма различны. По их практическому значению они располагаются следующим образом: почки – кишечник – легкие – кожа. Степень, скорость и пути выведения зависят от физико-химических свойств выделяемых веществ. Через почки выделяются главным образом неионизированные соединения, обладающие высокой гидрофильностью и плохо реабсорбирующиеся в почечных канальцах.
Через кишечник с калом удаляются следующие вещества: 1) не всосавшиеся в кровь при их пероральном поступлении; 2) выделенные из печени с желчью; 3) поступившие в кишечник через его стенки (путем пассивной диффузии по градиенту концентрации).
Большинство летучих неэлектролитов выделяется из организма в основном в неизмененном виде с выдыхаемым воздухом. Чем меньше коэффициент растворимости в воде, тем быстрее происходит их выделение, особенно той части, которая находится в циркулирующей крови. Выделение их фракции, депонированной в жировой ткани, задерживается и происходит гораздо медленнее, тем более что это количество может быть очень значительным, т.к. жировая ткань может составить более 20 % общей массы тела человека. Например, около 50 % поступившего ингаляционным путем хлороформа выделяется в течение первых 8-12 часов, а остальная часть – во второй фазе выделения, которая длится несколько суток.
Через кожу, в частности с потом, выходят из организма многие токсичные вещества – неэлектролиты (этиловый спирт, ацетон, фенолы, хлорированные углеводороды т.д.). Однако, за редким исключением (концентрация сероуглерода в поте в несколько раз выше, чем в моче), общее количество удаляемого таким образом токсичного вещества невелико.
Основные патологические симптомы при острых отравлениях:
1) симптомы нарушений функций ССС: брадикардия или тахикардия, артериальная гипотензия или гипертензия, экзотоксический шок.
С экзотоксическим шоком связано 65-70% летальных исходов при отравлениях. Такие больные находятся в тяжелом состоянии, у них наблюдаются психомоторное возбуждение или заторможенность, кожные покровы бледные с синюшным оттенком, холодные на ощупь, одышка и тахикардия, гипотензия и олигурия. При этом нарушаются функции практически всех жизненно важных органов и систем, но острая недостаточность кровообращения выступает как одно из ведущих клинических проявлений шока.
2) Симптомы нарушений ЦНС: головная боль, нарушение координации движений, галлюцинации, делирий, судороги, параличи, кома.
Наиболее тяжелыми формами психоневрологических расстройств при острых отравлениях являются токсическая кома и интоксикационные психозы. Кома чаще всего развивается при отравлении веществами, угнетающими функции Ц Н С. Характерная черта неврологической картины токсической комы – отсутствие стойкой очаговой симптоматики и быстрое улучшение состояния пострадавшего в ответ на мероприятия по выведению яда из организма. Интоксикационные психозы могут возникать вследствие тяжелых отравлений атропином, кокаином, тубазидом, этиленгликолем, угарным газом и проявляться разнообразной психопатологической симптоматикой (помрачение сознания, галлюцинации и т.д.). У лиц, злоупотребляющих алкоголем, могут развиться так называемые алкогольные психозы (галлюциноз, «белая горячка»). При отравлениях некоторыми нейротоксичными веществами (ФОС, пахикарпин, бромистый метил) встречаются нарушения нервно-мышечной проводимости с развитием парезов и параличей, а как осложнение – миофибрилляции.
С диагностической точки зрения важно знать, что возможно острое нарушение зрения вплоть до слепоты при отравлении метиловым спиртом и хинином; неясное зрение на фоне миоза-отравление ФОС; мидриаз – при отравлении атропином, никотином, пахикарпином; «цветное зрение» -- при отравлении салицилатами; развитие нарушений слуха – при отравлении хинином, некоторыми антибиотиками (канамицина моносульфат, неомицина сульфат, стрептомицина сульфат).
После перенесенного тяжелого отравления обычно длительно сохраняются астения, состояние повышенной утомляемости, раздражительности, слабости.
3) Симптомы поражения органов дыхания: брадипноэ, тахипноэ, патологические типы дыхания (Куссмауля), ларингоспазм, бронхоспазм, токсический отек легких. При нарушениях дыхания центрального происхождения, типичных для отравлений нейротоксическими ядами, из-за угнетения дыхательного центра или паралича дыхательной мускулатуры дыхание становится поверхностным, аритмичным вплоть до полного его прекращения.
Механическая асфиксия возникает у больных, находящихся в коматозном состоянии, при закрытии воздухоносных путей в результате западения языка, аспирации рвотных масс, гиперсекреции бронхиальных желез, слюнотечении. Клинически «механическая асфиксия» проявляется цианозом, наличием крупнопузырчатых хрипов надобластью трахеи и крупных бронхов.
При ожогах верхних дыхательных путей возможен стеноз гортани, который проявляется осиплостью или исчезновением голоса, одышкой, цианозом, прерывистым дыханием, возбуждением больного.
Токсический отек легких вызывается непосредственным поражением легочной мембраны токсическим веществом с последующим воспалением и отеком легочной ткани. Наиболее часто он наблюдается при отравлениях окислами азота, фосгеном, угарным газом и другими токсическими веществами удушающего действия, при ингаляции паров едких кислот и щелочей и при аспирации этих веществ, сопровождающейся ожогом верхних дыхательных путей. Для токсического отека легких характерна стадийность развития: рефлекторная стадия – появление рези в глазах, першения в носоглотке, стеснения в груди, частого поверхностного дыхания; стадия мнимого благополучия – исчезновение неприятных субъективных ощущений; стадия выраженных клинических проявлений – клокочущее дыхание, обильная пенистая мокрота, множество мелкопузырчатых влажных хрипов над легкими. Кожа и видимые слизистые оболочки цианотичны, нередко развивается острая сердечно-сосудистая недостаточность (коллапс), кожа приобретает землистый оттенок.
4) Симптомы поражения желудочно-кишечного тракта: проявляются в виде диспепсических расстройств (тошнота, рвота), гастроэнтероколита, ожогов пищеварительного тракта, пищеводно- желудочно-кишечных кровотечений. Кровотечения наиболее часты при отравлении прижигающими ядами (кислотами и щелочами); они могут быть ранними (в первые сутки) и поздними (2-3 недели).
Рвоту на ранних этапах отравления во многих случаях можно рассматривать как благоприятное явление, так как она способствует удалению токсического вещества из организма. Однако появление рвоты при коматозном состоянии больного, при отравлении прижигающими ядами у детей, при стенозе гортани и отеке легких опасно, так как может произойти аспирация рвотных масс в дыхательные пути.
Гасторэнтериты при отравлениях обычно сопровождаются дегидратацией организма и нарушением электролитного баланса.
5) Симптомы поражения печени и почек имеют клинику токсической гепато- и нефропатии, могут иметь 3 степени тяжести.
Легкая степень характеризуется отсутствием заметных клинических проявлений.
Средняя степень: печень увеличена, болезненна при пальпации, имеется желтуха, геморрагический диатез; при поражении почек – боль в пояснице, олигурия.
Тяжелая степень: развивается ОПеН и ОПН.
Большое значение в диагностике токсического поражения печени и почек имеют лабораторные и инструментальные исследования.
Государственное бюджетное образовательное учреждение
Высшего профессионального образования
«СЕВЕРО-ОСЕТИНСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ»
Министерства здравоохранения и социального развития России
КАФЕДРА ОБЩЕЙ ГИГИЕНЫ И
ФИЗИЧЕСКОЙ КУЛЬТУРЫ
ОЦЕНКА ТОКСИЧНОСТИ ПРОМЫШЛЕННЫХ ЯДОВ НА ОРГАНИЗМ
Учебное пособие для студентов, обучающихся
по специальности «Стоматология»
ВЛАДИКАВКАЗ 2012г.
Составители:
Ø ассистент Ф.К. Худалова,
Ø ассистент А.Р. Наниева
Рецензенты:
Ø Каллагова Ф.В. - зав. кафедрой химии и физики, профессор, д.м.н.;
Ø И.Ф. Боциев - доцент кафедры химии и физики, к. ф./м. н.
Утверждено ЦКУМС ГБОУ ВПО СОГМА Минздравсоцразвития России
Г., протокол №
Цель занятия: ознакомить студентов с основными параметрами, характеризующими степень токсичности и опасности химических веществ в условиях производства, с основными принципами санитарно-эпидемиологических правил, с принципами первичной профилактики по отношению к промышленным ядам.
Студент должен знать:
Методы оценки токсичности и опасности промышленных ядов; ознакомиться с правилами защиты от действия промышленных ядов.
Студент должен уметь:
1. Дать токсикологическую характеристику веществ на основании физико-химических констант.
2. Перечислить принципы первичной профилактики на предприятиях с промышленными ядами.
3. Определить роль врача в сохранении здоровья работающих.
Основная литература:
Ø Румянцев Г.И. Гигиена XXI век, М.: ГЭОТАР, 2009.
Ø Пивоваров Ю.П., Королик В.В., Зиневич Л.С. Гигиена и основы экологии человека. М.: Академия, 2004, 2010.
Ø Лакшин А.М., Катаева В.А. Общая гигиена с основами экологии человека: Учебник. – М.: Медицина, 2004 (Учеб.лит. для студентов мед.вузов).
Дополнительная литература:
Ø Пивоваров Ю.П. Руководство к лабораторным занятиям и основами экологии человека, 2006.
Ø Катаева В.А., Лакшин А.М. Руководство к практическим и самостоятельным занятиям по общей гигиене и основам экологии человека. М.: Медицина, 2005.
Ø «Руководство для практических занятий по гигиене труда». Под ред. Н.Ф. Кирилова. Изд-во ГЕОТАР-Медиа, М., 2008
Ø ГН 2.2.5.1313-03 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны».
Ø ГН 2.2.5.1314-03 «Ориентировочные безопасные уровни воздействия (ОБУВ) вредных веществ в воздухе рабочей зоны».
Ø Р 2.2.755-99 «Методика контроля содержания вредных веществ в воздухе рабочей зоны»
Химические вещества, которые, проникая в организм в условиях производства даже в относительно небольших количествах, вызывают в нем различные нарушения нормальной жизнедеятельности, называются производственными ядами.
ПУТИ ПОСТУПЛЕНИЯ ЯДОВ В ОРГАНИЗМ
Яды могут поступать в организм тремя путями: через легкие, желудочно-кишечный тракт и неповрежденную кожу. Через дыхательные пути яды проникают в организм в виде паров, газов и пыли, через желудочно-кишечный тракт - чащевсего с загрязненных рук, но также и вследствие заглатывания пыли, паров, газов; через кожу проникают органические химические вещества преимущественно жидкой, маслянистой и тестообразной консистенции.
Поступление ядов через органы дыхания является основным и наиболее опасным путем, т.к. легких создаются благоприятные условия для проникновения газов, паров и пыли в кровь.
Нереагирующие газы и пары поступают в кровь через легкие на основе закона диффузии, т.е. вследствие разницы парциального давления газов или паров в альвеолярном воздухе и крови. В начале насыщение крови газами или парами вследствие большой разницы парциального давления происходит быстро, затем замедляется и, наконец, когда парциальное давление газов или паров в альвеолярном воздухе и крови уравнивается, насыщение крови газами или парами прекращается. После удаления пострадавшего из загрязненной атмосферы начинается десорбция газов и паров и удаление их через легкие. Десорбция также происходит на основе законов диффузии.
Если вещества хорошо растворимы в воде, то они хорошо растворимы и в крови. Иная закономерность присуща сорбции при вдыхании реагирующих газов, т.е. таких которые в организме быстро вступают в реакцию при вдыхании этих газов насыщения никогда не наступает. Опасность острого отравления тем значительнее, чем дольше находится человек в загрязненной атмосфере.
Поступление ядов через желудочно-кишечный тракт. В полость рта яды чаще всего попадают с загрязненных рук.Классическим примером такого пути может служить поступление свинца. Это - мягкий металл, он легко стирается загрязняет руки, не отмывается водой и при еде и курении может попасть в полость рта. Возможно заглатывание ядовитых веществ из воздуха при задержке их на слизистых оболочках носоглотки и полости рта. Всасывание ядов происходит главным образом в тонком кишечнике и лишь в незначительной степени - в желудке. Большая часть ядовитых веществ, всосавшихся через желудочно-кишечную стенку, поступают через систему воротной вены в печень, где они задерживаются и обезвреживаются.
Поступление ядов через кожу. Через неповрежденную кожу могут проникать химические вещества, которые хорошо растворяются в жирах и липоидах, т.е. неэлектролиты; электролиты же, т. е. вещества, которые диссоциируют на ионы, через кожу не проникают.
Количество ядовитых веществ, которое может проникнуть через кожу, находится в прямой зависимости от их растворимости в воде, величины поверхности соприкосновения с кожей и скорости кровотока в ней. Последним объясняется то обстоятельство, что при работе в условиях высокой температуры воздуха, когда кровообращение в коже значительно усиливается, количество отравлений через кожу увеличивается. Большое значение для поступления ядов через кожу имеет консистенция и летучесть вещества. Жидкие органические вещества с большой летучестью быстро испаряются с поверхности кожи и в организм не попадают. При известных условиях летучие вещества могут вызвать отравление через кожу, например если они входят в состав мазей, паст, клеев, задерживающихся длительное время на коже. В практической работе знание путей поступления ядов в организм и определяет меры профилактики отравления.
РАСПРЕДЕЛЕНИЕ, ПРЕВРАЩЕНИЕ
И ВЫДЕЛЕНИЕ ЯДОВ ИЗ ОРГАНИЗМА
Распределение ядов в организме . По распределению в тканях и прониканию в клетки химические вещества можно разделить на две основные группы: неэлектролиты и электролиты.
Неэлектролиты, растворяющиеся в жирах и липоидах, вещество тем скорее и тем в большем количестве проникает в клетку, чем больше его растворимость в жирах. Это объясняется тем, что оболочка клеток содержит много липоидов. Для данной группы химических веществ барьеров в организме не существует: распределение неэлектролитов в организме при динамическом поступлении их определяется в основном условиями кровоснабжения органов и тканей. Это подтверждается следующими примерами.
Мозг, содержащий много липоидов и имеющий богатую кровеносную систему, насыщается этиловым эфиром очень быстро, в то время как другие ткани, содержащие много жира, но с плохим кровоснабжением насыщаются эфиром очень медленно. Насыщение анилином мозга происходит очень бытстро, в то время как околопочечный жир, имеющий слабое кровоснабжение, насыщается очень медленно. Удаление неэлектролитов из тканей также зависит в основном от кровоснабжения: после прекращения поступления яда в организм быстрее всего освобождаются от него органы ткани, богатые кровеносными сосудами. Из мозга, например, удаление анилина происходит значительно быстрее, чем из околопочечного жира. В конечном же итоге неэлектролиты после прекращения поступления их в организм распределяются во всех тканях равномерно.
Способность электролитов проникать в клетку резко ограничена и зависит от заряда ее поверхностного слоя. Если поверхность клетки заряжена отрицательно, она не пропускает анионов, а при положительном заряде она не пропускает катионов. Распределение электролитов в тканях очень неравномерно. Наибольшее количество свинца, например, накапливается в костях, затем в печени, почках, мышцах, а через 16 дней после прекращения его поступления в организм весь свинец переходит в кости. Фтор накапливается в костях, зубах и в небольшом количестве в печени и коже. Марганец в основном откладывается в печени и в небольших количествах в костях и сердце, еще меньше - в мозге, почках и др. Ртуть в основном откладывается в выделительных органах - почках и толстом кишечнике.
Судьба ядов в организме . Поступившие в организм яды подвергаются разнообразным превращениям. Почти все органические вещества подвергаются превращениям путем различных химических реакций: окисления, восстановления гидролиза, дезаминирования, метилирования, ацетилировяния и др. Не подвергаются превращениям лишь химически инертные вещества, как, например, бензин, выделяющийся из организма в неизмененном виде.
Выделение ядов из организма. Яды выделяются через легкие, почки, желудочно-кишечный тракт, кожу. Через легкие выделяются летучие вещества, не изменяющиеся или медленно изменяющиеся в организме. Через почки выделяются хорошо растворимые в воде вещества ипродукты превращения ядов в организме. Плохо растворимые вещества, например тяжелые металлы - свинец, ртуть, а также марганец, мышьяк выделяются через почки медленно. Через желудочно-кишечный тракт выделяются плохо растворимые или нерастворимые вещества: свинец, ртуть, марганец, сурьма и др. Некоторые вещества (свинец, ртуть) выделяются вместе со слюной в полости рта. Через кожу сальными железами выделяются все растворимые в жирах вещества. Потовыми железами выделяются ртуть, медь, мышьяк, сероводород и др.
Концентрации и дозы. Предельно допустимая концентрация (ПДК) вредных веществ в воздухе рабочей зоны, т. е. таких концентраций, которые при ежедневной работе в пределах 8 часов в течение всего рабочего стажа не могут вызывать у работающего каких-либо отклонений от нормального состояния или заболеваний, обнаруживаемых современными методами исследования непосредственно в процессе работы или в отдаленные сроки. Предельно допустимые концентрации имеют весьма важное значение для гигиенической оценки санитарных условий труда.
Возможность поступления вещества через легкие определяется прежде всего ее агрегатным состоянием (пар, газ, аэрозоль). Этот путь проникновения производственных ядов в организм является основным и наиболее опасным, поскольку поверхность легочных альвеол занимает значительную площадь (100-120 м2), а кровоток в легких довольно интенсивный.
Скорость всасывания химических веществ в кровь зависит от их агрегатного состояния, растворимости в воде и биосредах, парциального давления в альвеолярном воздухе, величины легочной вентиляции, кровопотоку в легких, состояния легочной ткани (наличие воспалительных очагов, транссудатов, экссудатов), характера химического взаимодействия с биосубстратами дыхательной системы.
Поступления в кровь летучих химических веществ (газов и паров) подчинено определенным закономерностям. По-разному всасываются никак реагирующие и реагирующие газ и парообразных вещества. Всасывания Нереагирующие газов и паров (углеводороды жирного и ароматического рядов и их производные) осуществляется в легких по принципу простой диффузии в направлении снижения градиента концентрации.
Для Нереагирующие газов (паров) коэффициент распределения является величиной постоянной. По его значению судить об опасности возникновения тяжелого отравления. Пары бензина (К - 2,1), например, при больших концентрациях способны вызвать мгновенное острое и даже смертельное отравление. Пары ацетона, которые имеют высокий коэффициент распределения (К = 400), не могут вызвать острого, тем более смертельного отравления, поскольку ацетон, в отличие от бензина, насыщает кровь медленнее, при возникновении симптомов интоксикации легко отвлечь.
При вдыхании реагирующих газов насыщения тканей организма не наступает из-за их быстрое химическое превращение; чем быстрее проходят процессы биотрансформации ядов, тем меньше они накапливаются в виде исходных продуктов. Сорбция реагирующих газов и паров происходит с постоянной скоростью. Процент сорбированного вещества находится в прямой зависимости от объема дыхания. В результате опасность острого отравления тем значительнее, чем дольше человек находится в загрязненной атмосфере; развития интоксикации может способствовать физическая работа, выполняемая в условиях нагревательного микроклимата.
Точка приложения действия реагирующих газов и паров может быть разной. Некоторые из них (хлороводород, аммиак, оксид серы (IV)), которые хорошо растворяются в воде, сорбируются преимущественно в верхних дыхательных путях. Вещества (хлор, оксид азота (IV)), которые хуже растворяются в воде, проникают в альвеолы и сорбируются в основном там.
Механизм всасывания химических веществ через кожу сложный. Возможно их прямое (трансэпидермальных) проникновение через эпидермис, волосяные фолликулы и сальные железы, протоки потовых желез. Различные участки кожи имеют неодинаковую способность к всасыванию производственных ядов; более пригодна для проникновения токсичных агентов кожа на медиальной поверхности бедер и рук, в паховой области, половых органов, груди и живота.
На первом этапе токсический агент проходит через эпидермис - липопротеиновый барьер, пропускающий только для газов и жирорастворимых органических веществ. На втором этапе вещество попадает из дермы в кровь. Этот барьер доступен для соединений, хорошо или частично растворимых в воде (крови). Так, через кожу проникают вещества, которые наряду с хорошей жиророзчиннистю водорастворимые. Опасность кожно-резорбтивного действия значительно возрастает, если указанные физико-химические свойства яда сочетаются с высокой токсичностью.
К производственным ядов, способных вызвать интоксикацию в случае проникновения через кожу, относят ароматические аминокислот и нитросоединения, фосфорорганические инсектициды, хлорированные углеводороды, металлоорганические соединения, то есть соединения, которым не свойственна диссоциация на ионы (неэлектролиты). Электролиты через кожу не проникают; они задерживаются, как правило, в роговом или блестящем слое эпидермиса. Исключение составляют тяжелые металлы (свинец, олово, медь, мышьяк, висмут, ртуть, сурьма) и их соли. Соединяясь с жирными кислотами и кожным салом на поверхности или внутри рогового слоя эпидермиса, они образуют жирорастворимые соли, способные преодолевать эпидермальный барьер.
Через кожу проникают не только жидкие вещества, загрязняющие ее, но и летучие газ и парообразных неэлектролиты. В отношении них кожа является инертным мембраной, через которую они проникают с помощью диффузий. С увеличением жиророзчинности проникающая способность легких неэлектролитов растет.
Всасывания токсических веществ из пищеварительного канала в большинстве случаев носит избирательный характер, поскольку разные его отделы имеют свою личную строение, иннервацию, химическую среду и ферментный состав.
Некоторые токсичные вещества (все жирорастворимые соединения, фенолы, некоторые соли, особенно цианиды) всасываются уже в полости рта. При этом токсичность веществ увеличивается за счет того, что они не поддаются воздействию желудочного сока и, минуя печень, а не обезвреживаются в ней.
Из желудка всасываются все жирорастворимые вещества и неионизированные молекулы органических веществ с помощью простой диффузии. Через поры клеточной мембраны желудочного эпителия возможно проникновение веществ фильтрацией. Многие яды, в том числе соединения свинца, в желудочном содержимом растворяются лучше, чем в воде, поэтому лучше и всасываются. Некоторые химические вещества, попав в желудок, полностью теряют токсичность или она значительно уменьшается из-за инактивации желудочным содержимым. Так, яд кураре, тетануса, змей и насекомых, бактериальные токсины, попадая внутрь через пищеварительный канал, практически безвредны.
На характер и скорость всасывания существенно влияют степень наполнения желудка, растворимость в желудочном содержимом и его рН. Вещества, принятые натощак, всасываются, как правило, интенсивнее.
Всасывания токсических веществ из пищеварительного канала происходит в основном в тонкой кишке. Жирорастворимые вещества хорошо всасываются с помощью диффузии. Липофильные соединения быстро проникают в стенку кишечника, однако сравнительно медленно всасываются в кровь. Для быстрого всасывания вещество имеет хорошо растворяться в липоидов и воде. Растворимость в воде способствует всасыванию яда из стенки кишки в кровь. Скорость всасывания химических веществ зависит от степени ионизации молекулы. Кислые вещества всасываются при условии, что их негативное логарифм константы ионизации (рКа) превышает 3, щелочные - до 8, то есть плохо всасываются вещества, которые в слабокислой или слабощелочной среде находятся в ионизированном состоянии. Сильные кислоты и щелочи всасываются медленно из-за образования комплексов с кишечным слизью. Вещества, близкие по строению к природным соединениям, всасываются через слизистую оболочку активным транспортом, который обеспечивает поступление питательных веществ.
Синдром нарушения сознания . Обусловлен непосредственным воздействием яда на кору головного мозга, а также вызванными им расстройствами мозгового кровообращения и кислородной недостаточностью. Такого рода явления (кома, ступор) возникают при тяжелом отравлении хлорированными углеводородами, фосфорорганическими соединениями (ФОС), спиртами, препаратами опия, снотворными.
Синдром нарушения дыхания . Часто наблюдается при коматозных состояниях, когда угнетается дыхательный центр. Расстройства акта дыхания возникают также вследствие паралича дыхательной мускулатуры, что резко осложняет течение отравлений. Тяжелые нарушения дыхательной функции наблюдаются при токсическом отеке легких и нарушениях проходимости дыхательных путей.
Синдром поражения крови . Характерен для отравлений окисью углерода, окислителями гемоглобина, гемолитическими ядами. При этом инактивируется гемоглобин, снижается кислородная емкость крови.
Синдром нарушения кровообращения . Почти всегда сопутствует острым отравлениям. Причинами расстройства функции сердечно-сосудистой системы могут быть: угнетение сосудодвигательного центра, нарушение функции надпочечниковых желез, повышение проницаемости стенок кровеносных сосудов и др.
Синдром нарушения терморегуляции . Наблюдается при многих отравлениях и проявляется или понижением температуры тела (алкоголь, снотворные, цианиды), или ее повышением (окись углерода, змеиный яд, кислоты, щелочи, ФОС). Эти сдвиги в организме, с одной стороны, являются следствием снижения обменных процессов и усиления теплоотдачи, а с другой - всасывания в кровь токсичных продуктов распада тканей, расстройства снабжения мозга кислородом, инфекционными осложнениями.
Судорожный синдром . Как правило, является показателем тяжелого или крайне тяжелого течения отравления. Приступы судорог возникают как следствие остро наступающего кислородного голодания мозга (цианиды, окись углерода) или в результате специфического действия ядов на центральные нервные структуры (этиленгликоль, хлорированные углеводороды, ФОС, стрихнин).
Синдром психических нарушений . Характерен для отравлений ядами, избирательно действующими на центральную нервную систему (алкоголь, диэтиламид лизергиновой кислоты, атропин, гашиш, тетраэтилсвинец).
Синдромы поражения печени и почек . Сопутствуют многим видам интоксикаций, при которых эти органы становятся объектами прямого воздействия ядов или страдают из-за влияния на них токсичных продуктов обмена и распада тканевых структур. Это особенно часто сопутствует отравлениям дихлорэтаном, спиртами, уксусной эссенцией, гидразином, мышьяком солями тяжелых металлов, желтым фосфором.
Синдром нарушения водно-электролитного баланса и кислотно-щелочного равновесия . При острых отравлениях является главным образом следствием расстройства функции пищеварительной и выделительной систем, а также секреторных органов. При этом возможно обезвоживание организма, извращение окислительно-восстановительных процессов в тканях, накопление недоокисленных продуктов обмена.
Доза. Концентрация. Токсичность
Как уже отмечалось, воздействуя на организм в различных количествах, одно и то же вещество вызывает неодинаковый эффект. Минимальная действующая , или пороговая, доза (концентрация) ядовитого вещества - это такое его наименьшее количество, которое вызывает явные, но обратимые изменения жизнедеятельности. Минимальная токсическая доза - это уже гораздо большее количество яда, вызывающее выраженное отравление с комплексом характерных патологических сдвигов в организме, но без смертельного исхода. Чем сильнее яд, тем ближе величины минимально действующей и минимально токсической доз. Помимо названных, в токсикологии принято еще рассматривать смертельные (летальные) дозы и концентрации ядов, т. е. те их количества, которые приводят человека (или животное) к гибели при отсутствии лечения. Летальные дозы определяются в результате опытов на животных. В экспериментальной токсикологии чаще всего пользуются средней летальной дозой (DL 50) или концентрацией (CL 50) яда, при которых погибает 50% подопытных животных. Если же наблюдается 100%-ная их гибель, то такая доза или концентрация обозначается как абсолютная летальная (DL 100 и CL 100). Понятие токсичности (ядовитости) означает меру несовместимости вещества с жизнью и определяется величиной, обратной DL 50 (CL 50), т. е. ).
В зависимости от путей поступления яда в организм определяют следующие токсикометрические параметры: мг/кг массы тела - при воздействии яда, попавшего с отравленной пищей и водой внутрь организма, а также на кожу и слизистые оболочки; мг/л или г/м 3 воздуха - при ингаляционном (т. е. через органы дыхания) проникновении яда в организм в виде газа, пара или аэрозоля; мг/см 2 поверхности - при попадании яда на кожу. Имеются способы и более углубленной количественной оценки ядовитости химических соединений. Так, при воздействии через дыхательные пути степень токсичности яда (Т) характеризует модифицированная формула Габера:
где с - концентрация яда в воздухе (мг/л); t - время воздействия (мин); ? - объем вентиляции легких (л/мин); g - масса тела (кг).
При разных способах введения ядов в организм требуются неодинаковые их количества для того, чтобы вызвать один и тот же токсический эффект. Например, DL 50 диизопропилфторфосфата, установленные на кроликах при различных способах введения, следующие (в мг/кг):

Значительное превышение пероральной дозы над парентеральными (т. е. введенными в организм, минуя желудочно-кишечный тракт) свидетельствует прежде всего о разрушении большей части яда в пищеварительной системе.
C учетом величины среднесмертельных доз (концентраций) при различных путях поступления в организм яды подразделяются на группы. Одна из таких классификаций, разработанных в нашей стране, приводится в таблице.
Классификация вредных веществ по степени токсичности (рекомендована Всесоюзной проблемной комиссией по научным основам гигиены труда и профессиональной патологии в 1970 г.)

При повторном воздействии одного и того же яда на организм может изменяться течение отравления из-за развития явлений кумуляции, сенсибилизации и привыкания. Под кумуляцией понимается накопление в организме токсичного вещества (материальная кумуляция ) или вызываемых им эффектов (функциональная кумуляция ). Понятно, что накапливается то вещество, которое медленно выводится или медленно обезвреживается, при этом суммарно действующая доза очень быстро возрастает. Что касается функциональной кумуляции, то она может проявляться тяжелыми расстройствами тогда, когда сам яд не задерживается в организме. Такое явление может наблюдаться, например, при отравлении алкоголем. Степень выраженности кумулятивных свойств ядовитых веществ принято оценивать коэффициентом кумуляции (K), который определяется в эксперименте на животных:
где а - повторно вводимое животному количество яда, составляющее 0,1–0,05 DL 50 ; b - количество введенных доз (а); с - однократно введенная доза.
В зависимости от величины коэффициента кумуляции токсичные вещества делят на 4 группы:
1) с резко выраженной кумуляцией (К<1);
2) с выраженной кумуляцией (К от 1 до 3);
3) с умеренной кумуляцией (К от 3 до 5);
4) со слабо выраженной кумуляцией (К>5).
Сенсибилизация - состояние организма, при котором повторное воздействие вещества вызывает больший эффект, чем предыдущее. В настоящее время нет единого взгляда на биологическую сущность этого явления. На основании экспериментальных данных можно полагать, что эффект сенсибилизации связан с образованием под влиянием токсичного вещества в крови и других внутренних средах измененных и ставших чужеродными для организма белковых молекул. Последние индуцируют формирование антител - особых структур белковой природы, осуществляющих защитную функцию организма. По-видимому, повторное даже значительно более слабое токсическое воздействие с последующей реакцией яда с антителами (или измененными рецепторными белковыми структурами) вызывает извращенный ответ организма в виде явлений сенсибилизации.
При повторяющемся воздействии ядов на организм можно наблюдать и обратное явление - ослабление их эффектов вследствие привыкания , или толерантности . Механизмы развития толерантности неоднозначны. Так, например, было показано, что привыкание к мышьяковистому ангидриду обусловлено возникновением под его влиянием воспалительных процессов на слизистой оболочке желудочно-кишечного тракта и уменьшением вследствие этого всасывания яда. В то же время, если препараты мышьяка вводить парентерально, толерантности не наблюдается. Однако наиболее частой причиной толерантности является стимуляция, или индукция, ядами активности ферментов, обезвреживающих их в организме. Об этом явлении пойдет еще речь впереди. А сейчас отметим, что привыкание к некоторым ядам, например ФОС, может быть еще обусловлено снижением чувствительности к ним соответствующих биоструктур или перегрузкой последних из-за массированного воздействия на них избыточного количества молекул токсичного вещества.
В связи с изложенным особое значение приобретает законодательная регламентация предельно допустимых концентраций (ПДК) вредных веществ в воздухе рабочей зоны промышленных и сельскохозяйственных предприятий, научно-исследовательских и испытательных учреждений, конструкторских бюро. Считается, что ПДК этих веществ при ежедневной восьмичасовой работе в течение всего рабочего стажа не могут вызывать у работающих заболеваний или отклонений в состоянии здоровья, обнаруживаемых современными методами исследования непосредственно в процессе работы или в отдаленные сроки. По сравнению с другими индустриальными странами в СССР существует более строгий подход к установлению ПДК многих химических агентов. В первую очередь это относится к веществам, обладающим первоначально незаметным, но постепенно нарастающим действием. Например, в Советском Союзе приняты более низкие уровни ПДК, чем в США, для окиси углерода (20 мг/м 3 против 100 мг/м 3), паров ртути и свинца (0,01 мг/м 3 против 0,1 мг/м 3), бензола (5 мг/м 3 против 80 мг/м 3), дихлорэтана (10 мг/м 3 против 400 мг/м 3) и других токсичных веществ. В нашей стране на предприятиях и учреждениях функционируют специальные токсикологические и санитарные лаборатории, которые осуществляют строгий контроль за содержанием вредных веществ в рабочих помещениях, за внедрением новых экологически безвредных технологических процессов, за работой газопылеулавливающих установок, за сточными водами и т. д. Любой химический продукт, выпускаемый промышленностью СССР, проходит проверку на токсичность и получает токсикологическую характеристику.
Пути поступления ядов в организм
Поступление ядов в организм человека может происходить через органы дыхания, пищеварительный тракт и кожу. Огромная поверхность легочных альвеол (около 80–90 м 2) обеспечивает интенсивное всасывание и быстрый эффект действия ядовитых паров и газов, присутствующих во вдыхаемом воздухе. При этом в первую очередь легкие становятся «входными воротами» для тех из них, которые хорошо растворимы в жирах. Диффундируя через альвеолярно-капиллярную мембрану толщиною около 0,8 мкм, отделяющую воздушную сроду от кровяного русла, молекулы ядов наикратчайшим путем проникают в малый круг кровообращения и затем, минуя печень, через сердце достигают кровеносных сосудов большого круга.
С отравленной пищей, водой, а также в «чистом» виде токсичные вещества всасываются в кровь через слизистые оболочки полости рта, желудка и кишечника. Большинство из них всасывается в эпителиальные клетки пищеварительного тракта и далее в кровь по механизму простой диффузии. При этом ведущим, фактором проникновения ядов во внутренние среды организма является их растворимость в липидах (жирах), точнее - характер распределения между липидной и водной фазами в месте всасывания. Существенную роль играет также степень диссоциации ядов.
Что касается жиронерастворимых чужеродных веществ, то многие из них проникают через клеточные мембраны слизистых оболочек желудка и кишечника по порам или пространствам между мембранами. Хотя площадь пор составляет только около 0,2% всей поверхности мембраны, тем не менее это обеспечивает всасывание многих водорастворимых и гидрофильных веществ. Током крови из желудочно-кишечного тракта токсичные вещества доставляются в печень - орган, выполняющий барьерную функцию по отношению к подавляющему большинству чужеродных соединений.
Как показывают многие исследования, скорость проникновения ядов через неповрежденную кожу прямо пропорциональна их растворимости в липидах, а дальнейший их переход в кровь зависит от способности растворяться в воде. Это относится не только к жидкостям и твердым веществам, но и к газам. Последние могут диффундировать через кожу как через инертную мембрану. Таким способом, например, кожный барьер преодолевают HCN, СО 2 , СО, H 2 S и другие газы. Небезынтересно отметить, что прохождению через кожу тяжелых металлов способствует образование ими солей с жирными кислотами жирового слоя кожи.
Прежде чем оказаться в том или ином органе (ткани), находящиеся в крови яды преодолевают ряд внутренних клеточных и мембранных барьеров. Важнейшими из них являются гематоэнцефалический и плацентарный - биологические структуры, которые находятся на границе кровеносного русла, с одной стороны, и центральной нервной системой и материнским плодом - с другой. Поэтому результат действия ядов и лекарств часто зависит от того, насколько выражена их способность проникать через барьерные структуры. Так, вещества, растворимые в липидах и быстро диффундирующие через липопротеидные мембраны, например спирты, наркотические средства, многие сульфаниламидные препараты, хорошо проникают в головной и спинной мозг. Они сравнительно легко попадают в кровь плода через плаценту. В этой связи нельзя не упомянуть случаи рождения детей с признаками привыкания к наркотикам, если их матери являлись наркоманками. Пока младенец находится в утробе матери, он адаптируется к определенной дозе наркотика. В то же время отдельные чужеродные вещества плохо проникают через барьерные структуры. Особенно это относится к препаратам, образующим в организме четвертичные аммониевые основания, к сильным электролитам, некоторым антибиотикам, а также коллоидным растворам.
Превращение токсичных веществ в организме
Проникающие в организм яды, как и другие чужеродные соединения, могут подвергаться разнообразным биохимическим превращениям (биотрансформации ), в результате которых чаще всего образуются менее токсичные вещества (обезвреживание , или детоксикация ). Но известно немало случаев усиления токсичности ядов при изменении их структуры в организме. Есть и такие соединения, характерные свойства которых начинают проявляться только вследствие биотрансформации. В то же время определенная часть молекул яда выделяется из организма без каких-либо изменений или вообще остается в нем на более или менее длительный период, фиксируясь белками плазмы крови и тканей. В зависимости от прочности образующегося комплекса «яд-белок» действие яда при этом замедляется или же утрачивается совсем. Кроме того, белковая структура может быть лишь переносчиком ядовитого вещества, доставляющим его к соответствующим рецепторам.
 Рис.1. Общая схема поступления, биотрансформации и выведения чужеродных веществ из организма
Рис.1. Общая схема поступления, биотрансформации и выведения чужеродных веществ из организма
Изучение процессов биотрансформации позволяет решить ряд практических вопросов токсикологии. Во-первых, познание молекулярной сущности детоксикации ядов дает возможность оцепить защитные механизмы организма и на этой основе наметить пути направленного воздействия на токсический процесс. Во-вторых, о величине поступившей в организм дозы яда (лекарства) можно судить по количеству выделяющихся через почки, кишечник и легкие продуктов их превращения - метаболитов, что дает возможность контролировать состояние здоровья людей, занятых производством и применением токсичных веществ; к тому же при различных заболеваниях образование и выделение из организма многих продуктов биотрансформации чужеродных веществ существенно нарушается. В-третьих, появление ядов в организме часто сопровождается индукцией ферментов, катализирующих (ускоряющих) их превращения. Поэтому, влияя с помощью определенных веществ на активность индуцированных ферментов, можно ускорить или затормозить биохимические процессы превращений чужеродных соединений.
В настоящее время установлено, что процессы биотрансформации чужеродных веществ протекают в печени, желудочно-кишечном тракте, легких, почках (рис. 1). Кроме того, согласно результатам исследований профессора И. Д. Гадаскиной, немалое число токсичных соединений подвергается необратимым превращениям и в жировой ткани. Однако главное значение здесь имеет печень, точнее - микросомальная фракция ее клеток. Именно в клетках печени, в их эндоплазматическом ретикулуме, локализуется большинство ферментов, катализирующих превращения чужеродных веществ. Сам ретикулум представляет собой сплетение линопротеидных канальцев, пронизывающих цитоплазму (рис. 2). Наивысшая ферментативная активность связывается с так называемым гладким ретикулумом, который в отличие от шероховатого не имеет на своей поверхности рибосом. Неудивительно поэтому, что при заболеваниях печени резко повышается чувствительность организма ко многим чужеродным веществам. Надо отметить, что, хотя число микросомальных ферментов невелико, они обладают очень важным свойством - высоким сродством к различным чужеродным веществам при относительной химической неспецифичности. Это создает им возможность вступать в реакции обезвреживания практически с любым химическим соединением, попавшим во внутренние среды организма. В последнее время доказано присутствие ряда таких ферментов в других органоидах клетки (например, в митохондриях), а также в плазме крови и в микроорганизмах кишечника.
 Рис. 2. Схематическое изображение клетка печени (Парк, 1373). 1 - ядро; 2 - лизосомы; 3 - эндоплазматический ретикулум; 4 - поры в ядерной оболочке; 5 - митохондрии; 6 - шероховатый зндоплазматический ретикулум; 7 - инвагинации плазматической мембраны; 8 - вакуоли; 9 - верна гликогена; 10 - гладкий эндонлазматический ретикулум
Рис. 2. Схематическое изображение клетка печени (Парк, 1373). 1 - ядро; 2 - лизосомы; 3 - эндоплазматический ретикулум; 4 - поры в ядерной оболочке; 5 - митохондрии; 6 - шероховатый зндоплазматический ретикулум; 7 - инвагинации плазматической мембраны; 8 - вакуоли; 9 - верна гликогена; 10 - гладкий эндонлазматический ретикулум
Считается, что главным принципом превращения в организме чужеродных соединений является обеспечение наибольшей скорости их выведения путем перевода из жирорастворимых в более водорастворимые химические структуры. В последние 10–15 лет при изучении сущности биохимических превращений чужеродных соединений из жирорастворимых в водорастворимые все большее значение придается так называемой монооксигеназной ферментной системе со смешанной функцией, которая содержит особый белок - цитохром Р-450. Он близок по строению к гемоглобину (в частности, содержит атомы железа с переменной валентностью) и является конечным звеном в группе окисляющих микросомальных ферментов - биотрансформаторов, сосредоточенных преимущественно в клетках печени. В организме цитохром Р-450 может находиться в 2 формах: окисленной и восстановленной. В окисленном состоянии он вначале образует с чужеродным веществом комплексное соединение, которое после этого восстанавливается специальным ферментом - цитохромредуктазой. Затем это, уже восстановленное, соединение реагирует с активированным кислородом, в результате чего образуется окисленное и, как правило, нетоксичное вещество.
В основе биотрансформации токсичных веществ лежит несколько типов химических реакций, в результате которых происходит присоединение или же отщепление метальных (-СН 3), ацетильных (СН 3 СОО-), карбоксильных (-СООН), гидроксильных (-ОН) радикалов (групп), а также атомов серы и серосодержащих группировок. Немалое значение имеют процессы распада молекул ядов вплоть до необратимой трансформации их циклических радикалов. Но особую роль среди механизмов обезвреживания ядов играют реакции синтеза
, или конъюгации
, в результате которых образуются нетоксичные комплексы - конъюгаты. При этом биохимическими компонентами внутренней среды организма, вступающими в необратимое взаимодействие с ядами, являются: глюкуроновая кислота (С 5 Н 9 О 5 СООН), цистеин(![]() ), глицин (NH 2 -CH 2 -CОOH),серная кислота и др. Молекулы ядов, содержащие несколько функциональных групп, могут трансформироваться посредством 2 и более метаболических реакций. Попутно отметим одно существенное обстоятельство: поскольку превращение и детоксикация ядовитых веществ за счет реакций конъюгации связаны с расходованием важных для жизнедеятельности веществ, то эти процессы могут вызвать дефицит последних в организме. Таким образом, появляется опасность другого рода - возможность развития вторичных болезненных состояний из-за нехватки необходимых метаболитов. Так, детоксикация многих чужеродных веществ находится в зависимости от запасов гликогена в печени, поскольку из него образуется глюкуроновая кислота. Поэтому при поступлении в организм больших доз веществ, обезвреживание которых осуществляется посредством образования эфиров глюкуроновой кислоты (например, бензольных производных), снижается содержание гликогена - основного легко мобилизуемого резерва углеводов. С другой стороны, есть вещества, которые под воздействием ферментов способны отщеплять молекулы глюкуроновой кислоты и тем самым способствовать обезвреживанию ядов. Одним из таких веществ оказался глицирризин, входящий в состав солодкового корня. Глицирризин содержит 2 молекулы глюкуроновой кислоты в связанном состоянии, которые освобождаются в организме, и это, по-видимому, определяет защитные свойства солодкового корня при многих отравлениях, известные издавна медицине Китая, Тибета, Японии.
), глицин (NH 2 -CH 2 -CОOH),серная кислота и др. Молекулы ядов, содержащие несколько функциональных групп, могут трансформироваться посредством 2 и более метаболических реакций. Попутно отметим одно существенное обстоятельство: поскольку превращение и детоксикация ядовитых веществ за счет реакций конъюгации связаны с расходованием важных для жизнедеятельности веществ, то эти процессы могут вызвать дефицит последних в организме. Таким образом, появляется опасность другого рода - возможность развития вторичных болезненных состояний из-за нехватки необходимых метаболитов. Так, детоксикация многих чужеродных веществ находится в зависимости от запасов гликогена в печени, поскольку из него образуется глюкуроновая кислота. Поэтому при поступлении в организм больших доз веществ, обезвреживание которых осуществляется посредством образования эфиров глюкуроновой кислоты (например, бензольных производных), снижается содержание гликогена - основного легко мобилизуемого резерва углеводов. С другой стороны, есть вещества, которые под воздействием ферментов способны отщеплять молекулы глюкуроновой кислоты и тем самым способствовать обезвреживанию ядов. Одним из таких веществ оказался глицирризин, входящий в состав солодкового корня. Глицирризин содержит 2 молекулы глюкуроновой кислоты в связанном состоянии, которые освобождаются в организме, и это, по-видимому, определяет защитные свойства солодкового корня при многих отравлениях, известные издавна медицине Китая, Тибета, Японии.
Что касается выведения из организма токсичных веществ и продуктов их превращения, то в этом процессе определенную роль играют легкие, органы пищеварения, кожа, различные железы. Но наибольшее значение здесь имеют ночки. Вот почему при многих отравлениях с помощью специальных средств, усиливающих отделение мочи, добиваются быстрейшего удаления ядовитых соединений из организма. Вместе с тем приходится считаться и с повреждающим воздействием на почки некоторых выводимых с мочой ядов (например, ртути). Кроме того, в почках могут задерживаться продукты превращения токсичных веществ, как это имеет место при тяжелых отравлениях этиленгликолем. При его окислении в организме образуется щавелевая кислота и в почечных канальцах выпадают кристаллы оксалата кальция, препятствующие мочеотделению. Вообще подобные явления наблюдаются тогда, когда концентрация выводимых через почки веществ высока.
Чтобы понять биохимическую сущность процессов превращения в организме ядовитых веществ, рассмотрим несколько примеров, касающихся распространенных компонентов химического окружения современного человека.
 Рис. 3. Окисление (гидроксилирование) бензола в ароматические спирты, образование конъюгатов и полное разрушения его молекулы (разрыв ароматического кольца)
Рис. 3. Окисление (гидроксилирование) бензола в ароматические спирты, образование конъюгатов и полное разрушения его молекулы (разрыв ароматического кольца)
Так, бензол , который, подобно другим ароматическим углеводородам, широко используется в качестве растворителя различных веществ и как промежуточный продукт при синтезе красителей, пластических масс, лекарств и других соединений, трансформируется в организме по 3 направлениям с образованием токсичных метаболитов (рис. 3). Последние выделяются через почки. Бензол может очень долго (по некоторым данным, до 10 лет) задерживаться в организме, в особенности в жировой ткани.
Определенный интерес представляет изучение процессов превращения в организме токсичных металлов , оказывающих все более широкое влияние на человека в связи с развитием науки и техники и освоением природных богатств. Прежде всего надо отметить, что в результате взаимодействия с окислительно-восстановительными буферными системами клетки, при котором осуществляется перенос электронов, валентность металлов меняется. При этом переход в состояние низшей валентности обычно связывается с уменьшением токсичности металлов. Например, ионы шестивалентного хрома переходят в организме в малотоксичную трехвалентную форму, а трехвалентный хром удается достаточно быстро удалить из организма с помощью некоторых веществ (пиросульфата натрия, виннокаменной кислоты и др.). Ряд металлов (ртуть, кадмий, медь, никель) активно связывается с биокомплексами, в первую очередь - с функциональными группировками ферментов (-SH, -NH 2 , -СООН и др.), что подчас определяет избирательность их биологического действия.
В числе ядохимикатов - веществ, предназначенных для уничтожения вредных живых существ и растений, имеются представители различных классов химических соединений, в той или иной мере токсичных для человека: хлорорганических, фосфорорганических, металлоорганических, нитрофенольных, цианистых и др. Согласно имеющимся данным, около 10% всех смертельных отравлений в настоящее время вызывается ядохимикатами. Наиболее значимыми из них, как известно, являются ФОС. Гидролизуясь, они, как правило, утрачивают токсичность. В противоположность гидролизу окисление ФОС почти всегда сопровождается усилением их токсичности. Это можно видеть, если сопоставить биотрансформацию 2 инсектицидов - диизопропилфторфосфата, который теряет токсические свойства, отщепляя при гидролизе атом фтора, и тиофоса (производное тиофосфорной кислоты), который окисляется в значительно более токсичный фосфакол (производное ортофосфорной кислоты).

Среди широко используемых лекарственных веществ снотворные препараты являются наиболее частыми источниками отравлений. Процессы их превращений в организме изучены достаточно хорошо. В частности, показано, что биотрансформация одного из распространенных производных барбитуровой кислоты - люминала (рис. 4) - протекает медленно, и это лежит в основе его достаточно длительного снотворного действия, так как оно зависит от количества неизмененных молекул люминала, контактирующих с нервными клетками. Распад барбитурового кольца приводит к прекращению действия люминала (как, впрочем, и других барбитуратов), который в лечебных дозах вызывает сон длительностью до 6 ч. В этой связи небезынтересна судьба в организме другого представителя барбитуратов - гексобарбитала. Его снотворное действие намного короче даже при применении значительно больших, чем люминала, доз. Полагают, что это зависит от большей скорости и от большего числа путей инактивации гексобарбитала в организме (образование спиртов, кетонов, деметилированных и других производных). С другой стороны, те барбитураты, которые сохраняются в организме почти в неизмененном виде, как например барбитал, оказывают более длительное снотворное действие, чем люминал. Из этого следует, что вещества, которые в неизмененном виде выводятся с мочой, могут вызвать интоксикацию, если почки не справляются с их удалением из организма.
Важно также отметить, что для понимания непредвиденного токсического эффекта при одновременном применении нескольких лекарств должное значение надо придавать ферментам, влияющим на активность комбинирующихся веществ. Так, например, лекарственный препарат физостигмин при совместном применении с новокаином делает последний весьма токсичным веществом, так как блокирует фермент (эстеразу), гидролизирующий новокаин в организме. Подобным же образом проявляет себя и эфедрин, связывая оксидазу, инактивирующую адреналин и тем самым удлиняя и усиливая действие последнего.
 Рис. 4. Видоизменение люминала в организме по двум направлениям: посредством окисления и за счет распада барбитурового кольца с последующим превращением продукта окисления в конъюгат
Рис. 4. Видоизменение люминала в организме по двум направлениям: посредством окисления и за счет распада барбитурового кольца с последующим превращением продукта окисления в конъюгат
Большую роль в биотрансформации лекарств играют процессы индукции (активации) и торможения активности микросомалыных ферментов различными чужеродными веществами. Так, этиловый алкоголь, некоторые инсектициды, никотин ускоряют инактивацию многих лекарственных препаратов. Поэтому фармакологи обращают внимание на нежелательные последствия контакта с названными веществами на фоне лекарственной терапии, при котором лечебный эффект ряда лекарств снижается. B то же время надо учитывать, что если контакт с индуктором микросомальных ферментов внезапно прекращается, то это может привести к токсическому действию лекарств и потребует уменьшения их доз.
Надо также иметь в виду, что, по данным Всемирной организации здравоохранения (ВОЗ), у 2,5% населения значительно повышен риск проявления токсичности лекарств, так как генетически обусловленный период их полураспада в плазме крови у данной группы людей в 3 раза больше среднего. При этом около трети всех описанных у человека ферментов во многих этнических группах представлены различными по своей активности вариантами. Отсюда - индивидуальные различия в реакциях па тот или иной фармакологический агент, зависящие от взаимодействия многих генетических факторов. Так, установлено, что примерно у одного на 1–2 тыс. человек резко снижена активность сывороточной холинэстеразы, которая гидролизует дитилин - средство, применяемое для расслабления скелетной мускулатуры на несколько минут при некоторых хирургических вмешательствах. У таких людей действие дитилина резко удлиняется (до 2 ч и более) и может стать источником тяжелого состояния.
Среди людей, живущих в странах Средиземноморья, в Африке и Юго-Восточной Азии, имеется генетически обусловленная недостаточность активности фермента глюкозо-6-фосфат-дегидрогеназы эритроцитов (снижение до 20% от нормы). Эта особенность делает эритроциты малоустойчивыми к ряду медикаментов: сульфаниламидам, некоторым антибиотикам, фенацетину. Вследствие распада эритроцитов у таких лиц на фоне лекарственного лечения возникают гемолитическая анемия и желтуха. Совершенно очевидно, что профилактика этих осложнений должна заключаться в предварительном определении активности соответствующих ферментов у больных.
Хотя приведенный материал лишь в общих чертах дает представление о проблеме биотрансформации токсичных веществ, он показывает, что организм человека обладает многими защитными биохимическими механизмами, которые в определенной степени предохраняют его от нежелательного воздействия этих веществ, по крайней мере - от небольших их доз. Функционирование такой сложной барьерной системы обеспечивается многочисленными ферментными cруктурами, активное влияние на которые дает возможность изменять течение процессов превращения и обезвреживания ядов. Но это уже - одна из следующих наших тем. При дальнейшем изложении мы будем еще возвращаться к рассмотрению отдельных аспектов превращения в организме некоторых токсичных веществ в той мере, в какой это необходимо для понимания молекулярных механизмов их биологического действия.
Биологические особенности организма, влияющие на токсический процесс
Какие же внутренние факторы, т. е. относящиеся к организму человека и животных как к объекту токсического воздействия, определяют возникновение, течение и последствия отравлений?
Прежде всего надо назвать видовые различия чувствительности к ядам, которые в конечном счете оказывают влияние на возможности переноса на человека экспериментальных данных, полученных в опытах на животных. Например, собаки и кролики могут переносить атропин в дозе, превосходящей в 100 раз дозу, смертельную для человека. С другой стороны, есть яды, обладающие более сильным действием на отдельные виды животных, чем на человека. К ним относится синильная кислота, окись углерода и др.
Животные, занимающие более высокое положение в эволюционном ряду, как правило, чувствительнее к большинству нейротропных, т. е. действующих преимущественно на нервную систему, химических соединений. Так, результаты опытов, приведенные К. С. Шадурским, свидетельствуют, что большие одинаковые дозы некоторых ФОС на морских свинок действуют в 4 раза сильнее, чем на мышей, и в сотни раз сильнее, чем на лягушек. В то же время к малым дозам тетраэтилсвинца - яда, также поражающего центральную нервную систему, более чувствительны крысы, чем кролики, а последние более чувствительны к эфиру, чем собаки. Можно полагать, что эти различия определяются прежде всего биологическими особенностями, присущими животным каждого вида: степенью развития отдельных систем, их компенсаторными механизмами и возможностями, а также интенсивностью и характером обменных процессов, в том числе биотрансформации чужеродных веществ. Такой подход, к примеру, позволяет биохимически оценить факт устойчивости кроликов и других животных к большим дозам атропина. Оказалось, что их кровь содержит эстеразу, которая гидролизует атропин и отсутствует у человека.
В отношении человека в практическом плане принято считать, что в целом он более чувствителен к химическим веществам, нежели теплокровные животные. В этой связи несомненный интерес представляют результаты опытов на добровольцах (врачах одного из московских медицинских институтов). Эти опыты показали, что человек в 5 раз чувствительнее морских свинок и кроликов и в 25 раз чувствительнее крыс к токсическому действию соединений серебра. К таким веществам, как мускарин, героин, атропин, морфин, человек оказался в десятки раз чувствительнее лабораторных животных. Действие же некоторых ФОС на человека и животных различалось мало.
При детальном изучении картины отравления было выявлено, что и многие признаки воздействия одного и того же вещества на особей разных видов подчас существенно разнятся. На собак, к примеру, морфий оказывает наркотическое действие, как и на человека, а у кошек это вещество вызывает сильное возбуждение и судороги. С другой стороны, бензол, вызывая у кроликов, как и у человека, угнетение кроветворной системы, у собак не приводит к таким сдвигам. Здесь надо отметить, что даже ближайшие к человеку представители животного мира - обезьяны - значительно отличаются от него по реакции на яды и лекарственные препараты. Вот почему эксперименты на животных (в том числе - высших) по изучению действия лекарств и других чужеродных веществ не всегда дают основания для определенных суждений о возможном их влиянии на организм человека.
Иной вид различий течения интоксикаций определяется особенностями пола . Изучению этого вопроса было посвящено большое количество экспериментальных и клинических наблюдений. И хотя в настоящее время не складывается впечатления, что половая чувствительность к ядам имеет какие-то общие закономерности, в общебиологическом плане принято считать, что женский организм более устойчив к действию различных вредоносных факторов внешней среды. Согласно экспериментальным данным, к воздействию окиси углерода, ртутя, свинца, наркотическим и снотворным веществам более устойчивы самки животных, в то время как самцы устойчивое самок к ФОС, никотину, стрихнину, некоторым мышьяковистым соединениям. При объяснении такого рода явлений надо учитывать по крайней мере 2 фактора. Первый - это существенные различия особей разного пола в скорости биотрансформации ядовитых веществ в клетках печени. Не следует забывать, что в итоге этих процессов в организме могут образовываться еще более токсичные соединения и именно они могут в конечном счете определять быстроту наступления, силу и последствия токсического эффекта. Вторым фактором, определяющим неодинаковое реагирование животных разного пола на одни и те же яды, надо считать биологическую специфику мужских и женских половых гормонов. Их роль в формировании устойчивости организма к вредным химическим агентам внешней среды подтверждается, например, таким фактом: у неполовозрелых особей различия в чувствительности к ядам между самцами и самками практически отсутствуют и начинают проявляться лишь при достижении ими половой зрелости. Об этом же свидетельствует и следующий пример: если самкам крыс вводить мужской половой гормон тестостерон, а самцам - женский половой гормон эстрадиол, то самки начинают реагировать на некоторые яды (например, наркотики) как самцы, и наоборот.
Клинико-гигиенические и экспериментальные данные свидетельствуют о более высокой чувствительности к ядам детей, чем взрослых , что принято объяснять своеобразием нервной и эндокринной систем детского организма, особенностями вентиляции легких, процессов всасываемости в желудочно-кишечном тракте, проницаемости барьерных структур и др. Но все же, как и для понимания причин половых различий в чувствительности к ядам, надо прежде всего иметь в виду низкую активность биотрансформационных печеночных ферментов организма ребенка, из-за чего он хуже переносит такие яды, как никотин, алкоголь, свинец, сероуглерод, а также сильнодействующие лекарства (например, стрихнин, алкалоиды опия) и многие другие вещества, которые обезвреживаются главным образом в печени. Но к некоторым токсичным химическим агентам дети (равно как и животные раннего возраста) оказываются даже более устойчивыми, чем взрослые. К примеру, в силу меньшей чувствительности к кислородному голоданию дети до 1 года более резистентны к действию окиси углерода - яду, блокирующему кислород - передающую функцию крови. К этому надо добавить, что и у разных возрастных групп животных также определяются существенные различия чувствительности по отношению ко многим токсичным веществам. Так, Г. Н. Красовский и Г. Г. Авилова в упомянутой выше работе отмечают, что молодые и новорожденные особи более чувствительны к сероуглероду и нитриту натрия, в то время как взрослые и старые - к дихлорэтану, фтору, гранозану.
Последствия воздействия ядов на организм
Уже накоплено много данных, свидетельствующих о развитии различных болезненных состояний спустя длительные сроки после воздействия на организм тех или иных ядовитых веществ. Так, в последние годы все большее значение в возникновении заболеваний сердечнососудистой системы, в частности атеросклероза, придается сероуглероду, свинцу, окиси углерода, фторидам. Особо опасным следует считать бластомогенный, т. е. вызывающий развитие опухолей, эффект некоторых веществ. Эти вещества, получившие название канцерогенов, встречаются как в воздухе промышленных предприятий, так и населенных пунктов и жилых помещений, в водоемах, почве, продуктах питания, растениях. Распространенными среди них являются полициклические ароматические углеводороды, азосоединения, ароматические амины, нитрозоамины, некоторые металлы, соединения мышьяка. Так, в недавно вышедшей в русском переводе книге американского исследователя Экхольма приводятся случаи канцерогенного действия ряда веществ на промышленных предприятиях США. Например, у людей, работающих с мышьяком на медных, свинцовых и цинковых плавильных заводах без достаточной техники безопасности, наблюдается особенно высокий процент рака легких. Жители близлежащих мест также чаще обычного болеют раком легких, по-видимому, от того, что они вдыхают рассеянный в воздухе мышьяк и другие вредные вещества, которые содержатся в выбросах этих заводов. Однако, как отмечает автор, за последние 40 лет владельцами предприятий не были введены какие-либо меры предосторожности при контакте рабочих с канцерогенными ядами. Все это в еще большей степени относится к горнякам на урановых рудниках и рабочим красильного производства.
Естественно, что для профилактики профессиональных злокачественных новообразований прежде всего необходимо изъятие канцерогенов из производства и замена их веществами, не обладающими бластомогенной активностью. Там же, где это невозможно, наиболее правильным решением, способным гарантировать безопасность их применения, является установление их ПДК. Одновременно в нашей стране ставится задача резкого ограничения содержания таких веществ в биосфере до количеств, значительно меньших ПДК. Делаются также попытки воздействия на канцерогены и токсичные продукты их превращений в организме с помощью специальных фармакологических средств.
Одним из опасных отдаленных последствий некоторых интоксикаций являются различные пороки развития и уродства, наследственные болезни и т. п., что зависит как от непосредственного влияния яда на половые железы (мутагенное действие), так и от расстройства внутриутробного развития плода. К веществам, действующим в этом направлении, токсикологи относят бензол и его производные, этиленимин, сероуглерод, свинец, марганец и другие промышленные яды, а также отдельные ядохимикаты. В этой связи должен быть назван и печально известный лекарственный препарат талидомид, который в качестве успокаивающего средства применяли в ряде западных стран беременные женщины и который стал причиной уродств для нескольких тысяч новорожденных. Еще одним примером такого рода является скандал, разыгравшийся в 1964 г. в США вокруг препарата под названием «Мер-29», который усиленно рекламировался как средство профилактики атеросклероза и сердечно-сосудистых заболеваний и которым воспользовались свыше 300 тыс. пациентов. В последующем обнаружилось, что «Мер-29» при длительном приеме приводил у многих людей к тяжелым заболеваниям кожи, облысению, снижению остроты зрения и даже слепоте. Концерн «У. Меррел и К о », производитель этого лекарства, был оштрафован на 80 тыс. долларов, в то время как за 2 года препарат «Мер-29» был продан на сумму в 12 млн. долларов. И вот спустя 16 лет, в начале 1980 г. этот концерн снова на скамье подсудимых. Ему предъявлен иск на 10 млн. долларов в качестве компенсации за многочисленные случаи уродств у новорожденных в США и Англии, матери которых принимали против тошноты на ранней стадии беременности лекарство под названием бендектин. Вопрос об опасности этого препарата впервые был поднят в медицинских кругах в начале 1978 г., однако фармацевтические предприятия продолжают производить бендектин, приносящий их хозяевам большие прибыли.
Примечания:
Саноцкий И. В. Предупреждение вредных химических воздействий на человека - комплексная задача медицины, экологии, химии и техники. - ЖВХО, 1974, № 2, с. 125–142.
Измеров Н. Ф. Научно-технический прогресс, развитие химической промышленности и задачи гигиены и токсикологии. - ЖВХО, 1974, № 2, с. 122–124.
Кириллов В. Ф. Санитарная охрана атмосферного воздуха. М.: Медицина, 1976.
Рудаки А. Касыды. - В кн.: Ирано-таджикская поэзия/ Пер. с фарси. М.: Худож. лит., 1974, с. 23. (Сер. Б-ка всемир. лит.).
(Лужников Е. А., Дагаее В. Н., Фарсов Н. Н. Основы реаниматологии при острых отравлениях. М.: Медицина, 1977.
Тиунов Л. А. Биохимические основы токсического действия. - К кн.: Основы общей промышленной токсикологии / Под ред. Н. А. Толокояцева и В. А. Филова. Л.: Медицина, 1976, с. 184–197.
Покровский А. А. Ферментный механизм некоторых интоксикаций. - Успехи биол. химии, 1962, т. 4, с. 61–81.
Тиунов Л. А. Ферменты и яды. - В кн.: Вопросы общей промышленной токсикологии / Под ред. И. В. Лазарева. Л., 1983, с. 80–85.
Локтионов С. И. Некоторые общие вопросы токсикологии. - В кн.: Неотложная помощь при острых отравлениях / Под ред. С. Н. Голикова. М.: Медицина, 1978, с. 9–10.
Грин Д., Гольдбергер Р. Молекулярные аспекты жизни. М.: Мир, 1988.
Гадаскина И. Д. Теоретическое и практическое значение изучения. превращения ядов в организме. - В кн.: Матер. науч. сессии, досвящ. 40-летию НИИ гигиены труда и проф. заболеваний. Л., 1964, с. 43–45.
Копосов Е. С. Острые отравления. - В кн.: Реаниматология. М.: Медицина, 1976, с. 222–229.
Применительно к лекарственной терапии близость этих двух показателей нередко свидетельствует о непригодности соответствующих фармакологических препаратов для лечебных целей.
Франке З. Химия отравляющих веществ / Пер. с нем. под peд. И. Л. Кнунянца и Р. Н. Стерлина. М.: Химия, 1973.
Демидов А. В. Авиационная токсикология. М.: Медицина, 1967.
Закусав В. В., Комиссаров И. В., Синюхин В. Н. Повторность действия лекарственных веществ. - В кн.: Клиническая фармакология /Под ред. В. В. Закусова. М.: Медицина, 1978, с. 52–56.
Цит. по: Хоцянов Л. К., Хухрина Е. В. Труд и здоровье в свете научно-технического прогресса. Ташкент: Медицина, 1977.
Амиров В. Н. Механизм всасываемости лекарственных веществ при приеме внутрь. - Здравоохр. Казахстана, 1972, № 10, с. 32–33.
Термином «рецептор» (или «рецепторная структура» мы будем обозначать «точку приложения» ядов: фермент, объект его каталитического воздействия (субстрат), а также белковые, липидные, мукополисахаридные и прочие тела, составляющие структуру клеток или участвующие в обмене веществ. Молекулярно-фармакологические представления о сущности этих понятий будут рассмотрены в гл. 2.
Под метаболитами принято также понимать различные биохимические продукты нормального обмена веществ (метаболизма).
Гадаскина И. Д. Жировая ткань и яды. - В кн.: Актуальные вопросы промышленной токсикологии/Под ред. Н. В. Лазарева, А. А. Голубева, Е. Т. Лыхипой. Л., 1970, с. 21–43.
Красовский Г. Н. Сравнительная чувствительность человека и лабораторных животных к действию токсических веществ. - В кн.: Общие вопросы промышленной токсикологии / Под ред. А, В. Рощина и И. В. Саноцкого. М., 1967, с. 59–62.
Красовский Г. Н., Авилова Г. Г. Видовая, половая и возрастная чувствительность к ядам. - ЖВХО, 1974, № 2, с. 159–164.
От cancer (лат. - рак), genos (греч.- рождение).
Экхольм Э. Окружающая среда и здоровье человека. М.: Прогресс, 1980.
Огрызков Н. И. Польза и вред лекарств. М.: Медицина, 1968.
Читайте также...
- Курсовая работа: Колебательные химические реакции Исследования концентрационных колебаний до открытия реакции Белоусовым
- Английские слова для изучения на каждый день: полезная лексика и советы для запоминания
- Публичное выступление: интересные примеры
- Сетевая викторина «Когда Россия молодая мужала с гением Петра