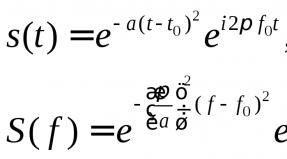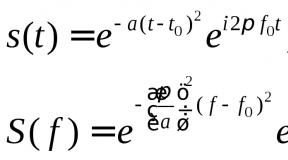Строение электронных оболочек атомов радия. Строение электронных оболочек атома. Что такое нейтрон
8 класс
Тема урока
«Строение электронных оболочек атомов».
Цель урока:
Рассмотрение модели строения атома.
Введение понятия «электронное облако», «электронная орбиталь» , «движение без траектории».
Рассмотрение модели энергетических состояний атома.
Задачи урока :
Образовательные: формирование представления об электронной оболочке атома и энергетических уровнях, рассмотрение электронного строения некоторых элементов, развитие умений по составлению электронных формул атомов, определению элементов по их электронным формулам, определение состава атома.
Воспитательные : рассмотрение значимости работы русского химика Д.И.Менделеева ;
Развивающие: формирование умений работать с периодической системой, логически мыслить и оформлять результаты логических операций, проводить параллели между химическими понятиями, изучаемыми в теме.
Ход урока
Организационные моменты.
Доброе утро, ребята, уважаемые гости! Меня зовут Ирина Александровна Губская, я– учитель химии, представляю Раменский муниципальный район, Удельнинскую гимназию.
Нам сегодня вместе предстоит продолжить постигать тайны и загадки, которыми полна наука «химия».Вы только в этом году начали изучать этот удивительно интересный, но вместе с тем сложный предмет, но наверняка многое уже знаете.
Тема нашего урока «Строение электронных оболочек атомов» (запишем в тетрадях).
Ребята, вам хочется увидеть атомы, электроны?...Можно ли это сделать?...
Можно….в воображении. Умозрительно. Мы многое видим умозрительно, почему бы не увидеть атом или электрон? Давайте попробуем. Итак, в путь!
Наша общая задача на уроке – продолжить изучение темы «Атомы химических элементов», нам предстоит актуализировать знания о строении атома и познакомиться со строением электронных оболочек атомов.
2. Объяснение нового материала
Поэт В.Брюсов в 1922 году под впечатлением от удивительных открытий физиков написал:
Быть может, эти электроны-
Миры, где пять материков,
Искусства, знанья, войны, троны
И память сорока веков!
Еще, быть может, каждый атом-
Вселенная, где сто планет;
Там – все, что здесь, в объеме сжатом,
Но также то, чего здесь нет.
? Как вы понимаете эти строки?
Может быть… Сходство электронов и атомов с астрономическими объектами пока не подтвердилось, но того, «чего здесь нет», оказалось более чем достаточно, и об этом вы будете узнавать на уроках химии и физики.
Науке потребовалось более 2000 лет, чтобы определить, на что он похож. И даже сейчас он все еще остается для нас загадкой.
Предлагаю вам заполнить анкету от имени атома.
Анкета.
1. Имя Атом
2. Место обитания любое тело в газообразном, жидком, твердом агрегатном состоянии
3. Поразительные
качества невероятная малость
4. Строение атома
? А из чего состоит атом? (схема)
Атом состоит из положительно заряженного ядра и движущихся вокруг него электронов
? А из чего состоит ядро атома?
Из протонов и нейтронов
А движущиеся вокруг ядра электроны образуют электронную оболочку
В начале ХХ в. была принята планетарная модель строения атома , согласно которой вокруг ядра движутся электроны, как планеты вокруг солнца. Следовательно, в атоме есть траектории, по которым движется электрон. Однако дальнейшие исследования показали, что в атоме не существует траекторий движения электронов. Движение без траектории означает, что мы не знаем, как электрон движется в атоме, но можем установить область, где чаще всего встречается электрон. Это уже не орбита, а орбиталь.
Двигаясь вокруг атома, электроны образуют в совокупности его электронную оболочку .
Совокупность всех электронов, окружающих ядро, называется электронной оболочкой (записываем определение)
? Давайте выясним, как движутся электроны вокруг ядра?
? Беспорядочно или в определенном порядке? Оказывается, движение электронов происходит в определенном порядке.
Электроны в атоме различаются определенной энергией, и, как показывают опыты, одни притягиваются к ядру сильнее, другие слабее. Объясняется это удаленностью электронов от ядра. Чем ближе электроны к ядру, тем больше связь их с ядром, но меньше запас энергии. По мере удаления от ядра атома сила притяжения электрона к ядру уменьшается, а запас энергии увеличивается. Каждый электрон в зависимости от своей энергии будет находиться на определенном расстоянии от ядра. Так образуются электронные слои в электронной оболочке атома.
Каждый слой состоит из электронов с близкими значениями энергии, поэтому слои электронов называют энергетическими уровнями .
Электронный слой, состоящий из электронов с близкими значениями энергии, называется энергетическим уровнем . (записываем определение)
? А как же определить, сколько слоев (энергетических уровней) в атоме того или иного элемента?
- Число уровней определяется номером периода, в котором располагается элемент.
Например:
У Na -2 энергетических уровня, т.к. он находиться во 2 периоде
У N – 3, 3 период
У Fe – 4 , 4 период
? А сколько электронов может находиться на каждом энергетическом уровне?
Максимальное число электронов, которое может находиться на том или ином энергетическом уровне, определяется по формуле
N = 2n 2
Где N - максимальное число электронов на уровне;
n – номер энергетического уровня.
Например:
1 энергетический уровень, n =1, N =2
n =2, N=8
Каждый уровень вмещает не больше рассчитанного количества электронов.
Если электронный слой содержит максимально возможное число электронов, то его называют завершенным . Электронные слои, не содержащие максимального числа электронов, называют незавершенными .
Как ранее было сказано, электрон движется не по орбите, а по орбитали и не имеет траектории.
Пространство вокруг ядра, где наиболее вероятно нахождение данного электрона, называется орбиталью этого электрона, или электронным облаком.
(записываем определение)
Орбитали, или подуровни , как их еще называют, могут иметь разную форму, и их количество соответствует номеру уровня, но не превышает четырех. Первый энергетический уровень имеет один подуровень (s ), второй- два (s , p ), третий – три (s , p , d ) и т.д. Электроны, находящиеся на одном энергетическом уровне тоже отличаются друг от друга.
Электроны разных подуровней одного и того же уровня имеют разную форму
электронного облака: сферическую (s ), гантелеобразную (p ) и более сложную конфигурацию.
S - орбиталь - это просто шарик. Путь электрона по ней напоминает путь нитки, которую наматывают на клубок. С нее начинается каждый уровень.
P – орбиталь похожа на объемную восьмерку или перекрученную сосиску, и вместе перекрутки расположено ядро. Таких орбиталей на каждом энергетическом уровне -3, они располагаются под углом 90 – как оси координат.
D - орбиталь – это две p-орбитали, соединенные центрами – как объемная четырехлепестковая ромашка, их на подуровне может быть 5.
F – орбиталь имеет более сложную форму, ее трудно описать словами.
Представьте путь своей мысли при решении системы уравнений с 3 неизвестными – это примерно такой же сложности.
Каждая орбиталь вмещает максимум 2 электрона с противоположными спинами.
Спин - это условное направление движения электрона вокруг своей оси – оно может быть либо по часовой стрелке, либо против. Только электроны с разными спинами уживаются на одной орбитали, т.к. отталкивание их из-за одноименных зарядов частично гасится.
Составим схему последовательного заполнения электронами энергетических уровней.
2 ē 8 ē 18 ē
n=1 n=2 n=3
s s p s p d
2ē 2ē 6ē 2ē 6ē 8ē
Теперь мы можем составить схему строения электронных оболочек атомов:
Определяем общее число электронов на оболочке по порядковому номеру элемента.
Определяем число энергетических уровней в электронной оболочке. Их число равно номеру периода в таблице Д. И. Менделеева, в котором находится элемент.
Определяем число электронов на каждом энергетическом уровне.
Используя для обозначения уровня арабские цифры и обозначая орбитали буквами s и p , а число электронов данной орбитали арабской цифрой вверху справа над буквой, изображаем строение атомов более полными электронными формулами.
Пример:
Ядро атома водорода имеет заряд +1, поэтому вокруг его ядра движется только один электрон на единственном энергетическом уровне. Запишем электронную конфигурацию атома водорода
Элемент № 3- литий. Ядро лития имеет заряд +3,следовательно, в атоме лития три электрона. Два из них находятся на первом энергетическом уровне, а третий электрон начинает заполнять второй энергетический уровень. Сначала заполняется s -орбиталь первого уровня, потом s -орбиталь второго уровня.
Свойства элементов изменяются периодически. У всех атомов семейств элементов (щелочные металлы, галогены, благородные газы) на внешнем энергетическом уровне одинаковое число электронов.
У щелочных металлов – 1 электрон
У галогенов – 7 электронов
У благородных газов – внешний уровень их атомов завершен, 8 электронов
Вывод: свойства химических элементов периодически (через определенные промежутки – периоды) повторяются потому, что периодически повторяется одинаковое строение внешних энергетических уровней их атомов.
3. Закрепление
Вариант 1
Заряд ядра атома АЗОТА равен
а)7 б)13 в)4 г)26 д)11
Число протонов в ядре атома КРИПТОНА равно
а)36 б)17 в)4 г)31 д)6
3 .Число нейтронов в ядре атома ЦИНКА равно
а)8 б)35 в)11 г)30 д)4
4 .Число электронов в атоме ЖЕЛЕЗА равно
а)11 б)8 в)56 г)26 д)30
Вариант 2
Максимальное число электронов на 4 энергетическом уровне
а) 32 б)36 в)16 г)24
Число электронных уровней у атома кальция равно
а)1 б)2 в)3 г)4
3.Число электронов на внешнем уровне атома БРОМА равно
а) 7 б) 6 в)5 г)4
4.Общее число s -электронов у атома ЛИТИЯ равно
а) 1 б)2 в)3 г)4
Электронная формула внешнего уровня 2s2 2p 6 соответствует атому
а) кислорода б) серы
в) фтора г) неона
Подведение итогов. Рефлексия .
Домашнее задание : записи в тетради, 8, упр. по карточкам
Домашнее задание:
1. Изобразите строение атомов следующих элементов:
1 вариант
фосфора
2 вариант
Магния
2 . Сравните строение атомов
1 вариант
бора и фтора
2 вариант
кислорода и серы
3 . По данным о распределении валентных электронов найдите элемент :
а) 2s 1
б) 2s 2 2p 4
в) 3s 2 3p 6
г) 3d 10 4s 1
д) 4s 2 4p 3
е) 4s 2 4p 5
ж) 3s 2 3p 4
Давайте подведем итоги урока.
? Что мы сегодня узнали нового?
Электрон не имеет траектории и движение его происходит по орбитали.
По схеме последовательного заполнения электронами энергетических уровней научились составлять электронные формулы элементов.
Научились по электронным формулам определять химический элемент.
«Далеко лежит за пределами нашего чувства вся природа начал»
Тит Лукреций Кар
I в. до н.э.
В приведенных словах древнеримского поэта сконцентрирована вся трудность устройства атома.
Но мы его попытались описать,используя математические подходы и формулы.
У вас на столах находятся карточки для самооценки урока. Отметьте,пожалуйста, «+» или «-» свою самооценку. Я рада была с вами познакомиться. Молодцы, вы хорошо работали, хочется отметить, спасибо за сотрудничество. До свидания, урок окончен, успехов вам в изучении химии.
Химическими веществами называют то, из чего состоит окружающий нас мир.
Свойства каждого химического вещества делятся на два типа: это химические, которые характеризуют его способность образовывать другие вещества, и физические, которые объективно наблюдаются и могут быть рассмотрены в отрыве от химических превращений. Так, например, физическими свойствами вещества являются его агрегатное состояние (твердое, жидкое или газообразное), теплопроводность, теплоемкость, растворимость в различных средах (вода, спирт и др.), плотность, цвет, вкус и т.д.
Превращения одних химических веществ в другие вещества называют химическими явлениями или химическими реакциями. Следует отметить, что существуют также и физические явления, которые, очевидно, сопровождаются изменением каких-либо физических свойств вещества без его превращения в другие вещества. К физическим явлениям, например, относятся плавление льда, замерзание или испарение воды и др.
О том, что в ходе какого-либо процесса имеет место химическое явление, можно сделать вывод, наблюдая характерные признаки химических реакций, такие как изменение цвета, образование осадка, выделение газа, выделение теплоты и (или) света.
Так, например, вывод о протекании химических реакций можно сделать, наблюдая:
Образование осадка при кипячении воды, называемого в быту накипью;
Выделение тепла и света при горении костра;
Изменение цвета среза свежего яблока на воздухе;
Образование газовых пузырьков при брожении теста и т.д.
Мельчайшие частицы вещества, которые в процессе химических реакций практически не претерпевают изменений, а лишь по-новому соединяются между собой, называются атомами.
Сама идея о существовании таких единиц материи возникла еще в древней Греции в умах античных философов, что собственно и объясняет происхождение термина «атом», поскольку «атомос» в буквальном переводе с греческого означает «неделимый».
Тем не менее, вопреки идее древнегреческих философов, атомы не являются абсолютным минимумом материи, т.е. сами имеют сложное строение.
Каждый атом состоит из так называемых субатомных частиц – протонов, нейтронов и электронов, обозначаемых соответственно символами p + , n o и e − . Надстрочный индекс в используемых обозначениях указывает на то, что протон имеет единичный положительный заряд, электрон – единичный отрицательный заряд, а нейтрон заряда не имеет.
Что касается качественного устройства атома, то у каждого атома все протоны и нейтроны сосредоточены в так называемом ядре, вокруг которого электроны образуют электронную оболочку.
Протон и нейтрон обладают практически одинаковыми массами, т.е. m p ≈ m n , а масса электрона почти в 2000 раз меньше массы каждого из них, т.е. m p /m e ≈ m n /m e ≈ 2000.
Поскольку фундаментальным свойством атома является его электронейтральность, а заряд одного электрона равен заряду одного протона, из этого можно сделать вывод о том, что количество электронов в любом атоме равно количеству протонов.
Так, например, в таблице ниже представлен возможный состав атомов:
Вид атомов с одинаковым зарядом ядер, т.е. с одинаковым числом протонов в их ядрах, называют химическим элементом. Таким образом, из таблицы выше можно сделать вывод о том, что атом1 и атом2 относятся в одному химическому элементу, а атом3 и атом4 — к другому химическому элементу.
Каждый химический элемент имеет свое название и индивидуальный символ, который читается определенным образом. Так, например, самый простой химический элемент, атомы которого содержат в ядре только один протон, имеет название «водород» и обозначается символом «Н», что читается как «аш», а химический элемент с зарядом ядра +7 (т.е. содержащий 7 протонов) — «азот», имеет символ «N» , который читается как «эн».
Как можно заметить из представленной выше таблицы, атомы одного химического элемента могут отличаться количеством нейтронов в ядрах.
Атомы, относящиеся к одному химическому элементу, но имеющие разное количество нейтронов и, как следствие массу, называют изотопами.
Так, например, химический элемент водород имеет три изотопа – 1 Н, 2 Н и 3 Н. Индексы 1, 2 и 3 сверху от символа Н означают суммарное количество нейтронов и протонов. Т.е. зная, что водород – это химический элемент, который характеризуется тем, что в ядрах его атомов находится по одному протону, можно сделать вывод о том, что в изотопе 1 Н вообще нет нейтронов (1-1=0), в изотопе 2 Н – 1 нейтрон (2-1=1) и в изотопе 3 Н – два нейтрона (3-1=2). Поскольку, как уже было сказано, нейтрон и протон имеют одинаковые массы, а масса электрона по сравнению с ними пренебрежимо мала, это значит, что изотоп 2 Н практически в два раза тяжелее изотопа 1 Н, а изотоп 3 Н — и вовсе в три раза. В связи с таким большим разбросом масс изотопов водорода изотопам 2 Н и 3 Н даже были присвоены отдельные индивидуальные названия и символы, что не характерно больше ни для одного другого химического элемента. Изотопу 2 Н дали название дейтерий и присвоили символ D, а изотопу 3 Н дали название тритий и присвоили символ Т.
Если принять массу протона и нейтрона за единицу, а массой электрона пренебречь, фактически верхний левый индекс помимо суммарного количества протонов и нейтронов в атоме можно считать его массой, в связи с чем этот индекс называют массовым числом и обозначают символом А. Поскольку за заряд ядра любого атома отвечают протоны, а заряд каждого протона условно считается равным +1, количество протонов в ядре называют зарядовым числом (Z). Обозначив количество нейтронов в атоме буквой N, математически взаимосвязь между массовым числом, зарядовым числом и количеством нейтронов можно выразить как:
Согласно современным представлениям, электрон имеет двойственную (корпускулярно-волновую) природу. Он обладает свойствами как частицы, так и волны. Подобно частице, электрон имеет массу и заряд, но в то же время поток электронов, подобно волне, характеризуется способностью к дифракции.
Для описания состояния электрона в атоме используют представления квантовой механики, согласно которым электрон не имеет определенной траектории движения и может находиться в любой точке пространства, но с разной вероятностью.
Область пространства вокруг ядра, где наиболее вероятно нахождение электрона, называется атомной орбиталью.
Атомная орбиталь может обладать различной формой, размером и ориентацией. Также атомную орбиталь называют электронным облаком.
Графически одну атомную орбиталь принято обозначать в виде квадратной ячейки:
Квантовая механика имеет крайне сложный математический аппарат, поэтому в рамках школьного курса химии рассматриваются только лишь следствия квантово-механической теории.
Согласно этим следствиям, любую атомную орбиталь и находящийся на ней электрон полностью характеризуют 4 квантовых числа.
- Главное квантовое число – n — определяет общую энергию электрона на данной орбитали. Диапазон значений главного квантового числа – все натуральные числа, т.е. n = 1,2,3,4, 5 и т.д.
- Орбитальное квантовое число — l – характеризует форму атомной орбитали и может принимать любые целочисленные значения от 0 до n-1, где n, напомним, — это главное квантовое число.
Орбитали с l = 0 называют s -орбиталями . s-Орбитали имеют сферическую форму и не обладают направленностью в пространстве:
Орбитали с l = 1 называются p -орбиталями . Данные орбитали обладают формой трехмерной восьмерки, т.е. формой, полученной вращением восьмерки вокруг оси симметрии, и внешне напоминают гантель:
Орбитали с l = 2 называются d -орбиталями , а с l = 3 – f -орбиталями . Их строение намного более сложное.
3) Магнитное квантовое число – m l – определяет пространственную ориентацию конкретной атомной орбитали и выражает проекцию орбитального момента импульса на направление магнитного поля. Магнитное квантовое число m l соответствует ориентации орбитали относительно направления вектора напряженности внешнего магнитного поля и может принимать любые целочисленные значения от –l до +l, включая 0, т.е. общее количество возможных значений равно (2l+1). Так, например, при l = 0 m l = 0 (одно значение), при l = 1 m l = -1, 0, +1 (три значения), при l = 2 m l = -2, -1, 0, +1, +2 (пять значений магнитного квантового числа) и т.д.
Так, например, p-орбитали, т.е. орбитали с орбитальным квантовым числом l = 1, имеющие форму «трехмерной восьмерки», соответствуют трем значениям магнитного квантового числа (-1, 0, +1), что, в свою очередь, соответствует трем перпендикулярным друг другу направлениям в пространстве.
4) Спиновое квантовое число (или просто спин) — m s — условно можно считать отвечающим за направление вращения электрона в атоме, оно может принимать значения. Электроны с разными спинами обозначают вертикальными стрелками, направленными в разные стороны: ↓ и .
Совокупность всех орбиталей в атоме, имеющих одно и то же значение главного квантового числа, называют энергетическим уровнем или электронной оболочкой. Любой произвольный энергетический уровень с некоторым номером n состоит из n 2 орбиталей.
Множество орбиталей с одинаковыми значениями главного квантового числа и орбитального квантового числа представляет собой энергетический подуровень.
Каждый энергетический уровень, которому соответствует главное квантовое число n, содержит n подуровней. В свою очередь, каждый энергетический подуровень с орбитальным квантовым числом l, состоит из (2l+1) орбиталей. Таким образом, s-подуровень состоит из одной s-орбитали, p-подуровень – трех p-орбиталей, d-подуровень – пяти d-орбиталей, а f-подуровень — из семи f-орбиталей. Поскольку, как уже было сказано, одна атомная орбиталь часто обозначается одной квадратной ячейкой, то s-, p-, d- и f-подуровни можно графически изобразить следующим образом:
Каждой орбитали соответствует индивидуальный строго определенный набор трех квантовых чисел n, l и m l .
Распределение электронов по орбиталям называют электронной конфигурацией.
Заполнение атомных орбиталей электронами происходит в соответствии с тремя условиями:
- Принцип минимума энергии : электроны заполняют орбитали, начиная с подуровня с наименьшей энергией. Последовательность подуровней в порядке увеличения их энергий выглядит следующим образом: 1s<2s<2p<3s<3p<4s≤3d<4p<5s≤4d<5p<6s…;
Для того чтобы проще запомнить данную последовательность заполнения электронных подуровней, весьма удобна следующая графическая иллюстрация:
- Принцип Паули : на каждой орбитали может находиться не более двух электронов.
Если на орбитали находится один электрон, то он называется неспаренным, а если два, то их называют электронной парой.
- Правило Хунда : наиболее устойчивое состояние атома является такое, при котором в пределах одного подуровня атом обладает максимально возможным числом неспаренных электронов. Такое наиболее устойчивое состояние атома называется основным состоянием.
Фактически вышесказанное означает то, что, например, размещение 1-го, 2-х, 3-х и 4-х электронов на трех орбиталях p-подуровня будет осуществляться следующим образом:
Заполнение атомных орбиталей от водорода, имеющего зарядовое число равное 1, до криптона (Kr) с зарядовым числом 36 будет осуществляться следующим образом:
Подобное изображение порядка заполнения атомных орбиталей называется энергетической диаграммой. Исходя из электронных диаграмм отдельных элементов, можно записать их так называемые электронные формулы (конфигурации). Так, например, элемент с 15ю протонами и, как следствие, 15ю электронами, т.е. фосфор (P), будет иметь следующий вид энергетической диаграммы:
При переводе в электронную формулу атома фосфора примет вид:
15 P = 1s 2 2s 2 2p 6 3s 2 3p 3
Цифрами нормального размера слева от символа подуровня показан номер энергетического уровня, а верхними индексами справа от символа подуровня показано количество электронов на соответствующем подуровне.
Ниже приведены электронные формул первых 36 элементов периодической системы Д.И. Менделеева.
| период | № элемента | символ | название | электронная формула |
| I | 1 | H | водород | 1s 1 |
| 2 | He | гелий | 1s 2 | |
| II | 3 | Li | литий | 1s 2 2s 1 |
| 4 | Be | бериллий | 1s 2 2s 2 | |
| 5 | B | бор | 1s 2 2s 2 2p 1 | |
| 6 | C | углерод | 1s 2 2s 2 2p 2 | |
| 7 | N | азот | 1s 2 2s 2 2p 3 | |
| 8 | O | кислород | 1s 2 2s 2 2p 4 | |
| 9 | F | фтор | 1s 2 2s 2 2p 5 | |
| 10 | Ne | неон | 1s 2 2s 2 2p 6 | |
| III | 11 | Na | натрий | 1s 2 2s 2 2p 6 3s 1 |
| 12 | Mg | магний | 1s 2 2s 2 2p 6 3s 2 | |
| 13 | Al | алюминий | 1s 2 2s 2 2p 6 3s 2 3p 1 | |
| 14 | Si | кремний | 1s 2 2s 2 2p 6 3s 2 3p 2 | |
| 15 | P | фосфор | 1s 2 2s 2 2p 6 3s 2 3p 3 | |
| 16 | S | сера | 1s 2 2s 2 2p 6 3s 2 3p 4 | |
| 17 | Cl | хлор | 1s 2 2s 2 2p 6 3s 2 3p 5 | |
| 18 | Ar | аргон | 1s 2 2s 2 2p 6 3s 2 3p 6 | |
| IV | 19 | K | калий | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 |
| 20 | Ca | кальций | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 | |
| 21 | Sc | скандий | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1 | |
| 22 | Ti | титан | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2 | |
| 23 | V | ванадий | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 3 | |
| 24 | Cr | хром | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 5 здесь наблюдается проскок одного электрона с s на d подуровень | |
| 25 | Mn | марганец | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5 | |
| 26 | Fe | железо | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 | |
| 27 | Co | кобальт | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 7 | |
| 28 | Ni | никель | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 8 | |
| 29 | Cu | медь | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 10 здесь наблюдается проскок одного электрона с s на d подуровень | |
| 30 | Zn | цинк | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 | |
| 31 | Ga | галлий | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 1 | |
| 32 | Ge | германий | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 2 | |
| 33 | As | мышьяк | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 3 | |
| 34 | Se | селен | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 4 | |
| 35 | Br | бром | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5 | |
| 36 | Kr | криптон | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 |
Как уже было сказано, в основном своем состоянии электроны в атомных орбиталях расположены согласно принципу наименьшей энергии. Тем не менее, при наличии пустых p-орбиталей в основном состоянии атома, нередко, при сообщении ему избыточной энергии атом можно перевести в так называемое возбужденное состояние. Так, например, атом бора в основном своем состоянии имеет электронную конфигурацию и энергетическую диаграмму следующего вида:
5 B = 1s 2 2s 2 2p 1
А в возбужденном состояниии (*), т.е. при сообщении некоторой энергии атому бора, его электронная конфигурация и энергетическая диаграмма будут выглядеть так:
5 B* = 1s 2 2s 1 2p 2
В зависимости от того, какой подуровень в атоме заполняется последним, химические элементы делят на s, p, d или f.
Нахождение s, p, d и f-элементов в таблице Д.И. Менделеева:
- У s-элементов последний заполняемый s-подуровень. К данным элементам относятся элементы главных (слева в ячейке таблицы) подгрупп I и II групп.
- У p-элементов заполняется p-подуровень. К p-элементам относят последние шесть элементов каждого периода, кроме первого и седьмого, а также элементы главных подгрупп III-VIII групп.
- d-Элементы расположены между s – и p-элементами в больших периодах.
- f-Элементы называют лантаноидами и актиноидами. Они вынесены вниз таблицы Д.И. Менделеева.
Электроны
Понятие атом возникло еще в античном мире для обозначения частиц вещества. В переводе с греческого атом означает «неделимый».

Ирландский физик Стони на основании опытов пришел к выводу, что электричество переносится мельчайшими частицами, сущеетвующими в атомах всех химических элементов. В 1891 г. Стони предложил эти частицы назвать электронами, что по-гречески означает «янтарь». Через несколько лет после того, как электрон получил свое название, английский физик Джозеф Томсон и французский физик Жан Перрен доказали, что электроны несут на себе отрицательный заряд. Это наименьший отрицательный заряд, который в химии принят за единицу (-1). Томсон даже сумел определить скорость движения электрона (скорость электрона на орбите обратно пропорциональна номеру орбиты n. Радиусы орбит растут пропорционально квадрату номера орбиты. На первой орбите атома водорода (n=1; Z=1) скорость равна ≈ 2,2·106 м/с, то есть примерно в сотню раз меньше скорости света с=3·108 м/с.) и массу электрона (она почти в 2000 раз меньше массы атома водорода).

Состояние электронов в атоме
Под состоянием электрона в атоме понимают совокупность информации об энергии определенного электрона и пространстве, в котором он находится . Электрон в атоме не имеет траектории движения, т. е. можно говорить лишь о вероятности нахождения его в пространстве вокруг ядра .
 Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек. При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек. При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
Пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью. В нем заключено приблизительно 90 % электронного облака , и это означает, что около 90 % времени электрон находится в этой части пространства. По форме различают 4 известных ныне типа орбиталей , которые обозначаются латинскими буквами s, p, d и f . Графическое изображение некоторых форм электронных орбиталей представлено на рисунке.

Важнейшей характеристикой движения электрона на определенной орбитали является энергия его связи с ядром . Электроны, обладающие близкими значениями энергии, образуют единый электронный слои, или энергетический уровень. Энергетические уровни нумеруют, начиная от ядра, - 1, 2, 3, 4, 5, 6 и 7.
Целое число n, обозначающее номер энергетического уровня, называют главным квантовым числом. Оно характеризует энергию электронов, занимающих данный энергетический уровень. Наименьшей энергией обладают электроны первого энергетического уровня, наиболее близкого к ядру. По сравнению с электронами первого уровня, электроны последующих уровней будут характеризоваться большим запасом энергии. Следовательно, наименее прочно связаны с ядром атома электроны внешнего уровня.
Наибольшее число электронов на энергетическом уровне определяется по формуле:
N = 2n 2 ,
где N - максимальное число электронов; n - номер уровня, или главное квантовое число. Следовательно, на первом, ближайшем к ядру энергетическом уровне может находиться не более двух электронов; на втором - не более 8; на третьем - не более 18; на четвертом - не более 32.
Начиная со второго энергетического уровня (n = 2) каждый из уровней подразделяется на подуровни (подслои), несколько отличающиеся друг от друга энергией связи с ядром. Число подуровней равно значению главного квантового числа: первый энергетический уровень имеет один подуровень; второй - два; третий - три; четвертый - четыре подуровня . Подуровни в свою очередь образованы орбиталями. Каждому значению n соответствует число орбиталей, равное n.
Подуровни принято обозначать латинскими буквами, равно как и форму орбиталей, из которых они состоят: s, p, d, f.

Протоны и нейтроны

Атом любого химического элемента сравним с крохотной Солнечной системой. Поэтому такую модель атома, предложенную Э. Резерфордом, называют планетарной .
Атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов - протонов и нейтронов .
Протоны имеют заряд, равный заряду электронов, но противоположный по знаку (+1), и массу, равную массе атома водорода (она принята в химии за единицу). Нейтроны не несут заряда, они нейтральны и имеют массу, равную массе протона.
Протоны и нейтроны вместе называют нуклонами (от лат. nucleus - ядро). Сумма числа протонов и нейтронов в атоме называется массовым числом . Например, массовое число атома алюминия:

13 + 14 = 27
число протонов 13, число нейтронов 14, массовое число 27
Так как массой электрона, ничтожно малой, можно пренебречь, то очевидно, что в ядре сосредоточена вся масса атома. Электроны обозначают e — .
Поскольку атом электронейтрален , то также очевидно, что число протонов и электронов в атоме одинаково. Оно равно порядковому номеру химического элемента, присвоенному ему в Периодической системе. Масса атома складывается из массы протонов и нейтронов. Зная порядковый номер элемента (Z), т. е. число протонов, и массовое число (А), равное сумме чисел протонов и нейтронов, можно найти число нейтронов (N) по формуле:

N = A — Z
Например, число нейтронов в атоме железа равно:
56 — 26 = 30
Изотопы
Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядра, но разное массовое число, называются изотопами . Химические элементы, встречающиеся в природе, являются смесью изотопов. Так, углерод имеет три изотопа с массой 12, 13, 14; кислород - три изотопа с массой 16, 17, 18 и т. д. Обычно приводимая в Периодической системе относительная атомная масса химического элемента является средним значением атомных масс природной смеси изотопов данного элемента с учетом их относительного содержания в природе. Химические свойства изотопов большинства химических элементов совершенно одинаковы. Однако изотопы водорода сильно различаются по свойствам из-за резкого кратного увеличения их относительной атомной массы; им даже присвоены индивидуальные названия и химические знаки.

Элементы первого периода
Схема электронного строения атома водорода:

Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням).

Графическая электронная формула атома водорода (показывает распределение электронов по энергетическим уровням и подуровням):

Графические электронные формулы атомов показывают распределение электронов не только по уровням и подуровням, но и по орбиталям.
В атоме гелия первый электронный слой завершен - в нем 2 электрона. Водород и гелий - s-элементы; у этих атомов заполняется электронами s-орбиталь.

У всех элементов второго периода первый электронный слой заполнен , и электроны заполняют s- и р-орбитали второго электронного слоя в соответствии с принципом наименьшей энергии (сначала s, а затем р) и правилами Паули и Хунда.
В атоме неона второй электронный слой завершен - в нем 8 электронов.
У атомов элементов третьего периода первый и второй электронные слои завершены, поэтому заполняется третий электронный слой, в котором электроны могут занимать 3s-, 3р- и 3d- подуровни.
У атома магния достраивается 3s- электронная орбиталь. Na и Mg - s-элементы.
У алюминия и последующих элементов заполняется электронами 3р-подуровень.
У элементов третьего периода остаются незаполненными 3d-орбитали.
Все элементы от Al до Ar - р-элементы. s- и р-элементы образуют главные подгруппы в Периодической системе.

Элементы четвертого — седьмого периодов
У атомов калия и кальция появляется четвертый электронный слой, заполняется 4s-подуровень, т. к. он имеет меньшую энергию, чем 3d-подуровень.
К, Са - s-элементы, входящие в главные подгруппы. У атомов от Sc до Zn заполняется электронами 3d-подуровень. Это 3d-элементы. Они входят в побочные подгруппы, у них заполняется предвнешний электронный слой, их относят к переходным элементам.
Обратите внимание на строение электронных оболочек атомов хрома и меди. В них происходит «провал» одного электрона с 4s- на 3d-подуровень, что объясняется большей энергетической устойчивостью образующихся при этом электронных конфигураций 3d 5 и 3d 10:

В атоме цинка третий электронный слой завершен - в нем заполнены все подуровни 3s, 3р и 3d, всего на них 18 электронов. У следующих за цинком элементов продолжает заполняться четвертый электронный слой, 4р-подуровень.
Элементы от Ga до Кr - р-элементы.
У атома криптона внешний слой (четвертый) завершен, имеет 8 электронов. Но всего в четвертом электронном слое может быть 32 электрона; у атома криптона пока остаются незаполненными 4d- и 4f-подуровни.У элементов пятого периода идет заполнение по-дуровней в следующем порядке: 5s — 4d — 5р. И так-же встречаются исключения, связанные с «провалом » электронов, у 41 Nb, 42 Мо, 44 Ru, 45 Rh, 46 Pd, 47 Ag.
В шестом и седьмом периодах появляются f-элементы, т. е. элементы, у которых идет заполнение соответственно 4f- и 5f-подуровней третьего снаружи электронного слоя.
4f-элементы называют лантаноидами.
5f-элементы называют актиноидами.
Порядок заполнения электронных подуровней в атомах элементов шестого периода: 55 Cs и 56 Ва - 6s-элементы; 57 La … 6s 2 5d x - 5d-элемент; 58 Се - 71 Lu - 4f-элементы; 72 Hf — 80 Hg - 5d-элементы; 81 Т1 — 86 Rn - 6d-элементы. Но и здесь встречаются элементы, у которых «нарушается» порядок заполнения электронных орбиталей, что, например, связано с большей энергетической устойчивостью наполовину и полностью заполненных f-подуровней, т. е. nf 7 и nf 14 . В зависимости от того, какой подуровень атома заполняется электронами последним, все элементы делят на четыре электронных семейства, или блока:
- s-элементы . Электронами заполняется s-подуровень внешнего уровня атома; к s-элементам относятся водород, гелий и элементы главных подгрупп I и II групп.
- p-элементы . Электронами заполняется р-подуровень внешнего уровня атома; к р-элементам относятся элементы главных подгрупп III- VIII групп.
- d-элементы . Электронами заполняется d-подуровень предвнешнего уровня атома; к d-элементам относятся элементы побочных подгрупп I-VIII групп, т. е. элементы вставных декад больших периодов, расположенных между s- и р-элементами. Их также называют переходными элементами.
- f-элементы . Электронами заполняется f-подуровень третьего снаружи уровня атома; к ним относятся лантаноиды и антиноиды.

Швейцарский физик В. Паули в 1925 г. установил, что в атоме на одной орбитали может находиться не более двух электронов, имеющих противоположные (антипараллельные) спины (в переводе с английского - «веретено»), т. е. обладающих такими свойствами, которые условно можно представить себе как вращение электрона вокруг своей воображаемый оси: по часовой или против часовой стрелки.

Этот принцип носит название принципа Паули . Если на орбитали находится один электрон, то он называется неспаренным, если два, то это спаренные электроны, т. е. электроны с противоположными спинами. На рисунке показана схема подразделения энергетических уровней на подуровни и очередность их заполнения.


Очень часто строение электронных оболочек атомов изображают с помощью энергетических или квантовых ячеек - записывают так называемые графические электронные формулы. Для этой записи используют следующие обозначения: каждая квантовая ячейка обозначается клеткой, которая соответствует одной орбитали; каждый электрон обозначается стрелкой, соответствующей направлению спина. При записи графической электронной формулы следует помнить два правила: принцип Паули и правило Ф. Хунда , согласно которому электроны занимают свободные ячейки сначала по одному и имеют при этом одинаковое значение спина, а лишь затем спариваются, но спины, при этом по принципу Паули будут уже противоположно направленными.
Правило Хунда и принцип Паули
Правило Хунда - правило квантовой химии, определяющее порядок заполнения орбиталей определённого подслоя и формулируется следующим образом: суммарное значение спинового квантового числа электронов данного подслоя должно быть максимальным. Сформулировано Фридрихом Хундом в 1925 году.
Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Другая формулировка : Ниже по энергии лежит тот атомный терм, для которого выполняются два условия.
- Мультиплетность максимальна
- При совпадении мультиплетностей суммарный орбитальный момент L максимален.
Разберём это правило на примере заполнения орбиталей p-подуровня p -элементов второго периода (то есть от бора до неона (в приведённой ниже схеме горизонтальными чёрточками обозначены орбитали, вертикальными стрелками - электроны, причём направление стрелки обозначает ориентацию спина).
Правило Клечковского
Правило Клечковского — по мере увеличения суммарного числа электронов в атомах (при возрастании зарядов их ядер, или порядковых номеров химических элементов) атомные орбитали заселяются таким образом, что появление электронов на орбитали с более высокой энергией зависит только от главного квантового числа n и не зависит от всех остальных квантовых чисел, в том числе и от l. Физически это означает, что в водородоподобном атоме (в отсутствие межэлектронного отталкивания) орбитальная энергия электрона определяется только пространственной удаленностью зарядовой плотности электрона от ядра и не зависит от особенностей его движения в поле ядра.
Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречатреальной энергетической последовательности атомых орбиталей только в двух однотипных случаях: у атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место “провал” электрона с s-подуровня внешнего слояна d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома, аименно: после заполнения двумя электронами орбитали 6s
Основой современной теории строения атома являются законы и положения квантовой механики – раздела физики, изучающего движение микрообъектов (электронов, протонов и других частиц, которые имеют ничтожную массу).
Согласно квантово-механическим представлениям, движущимся микрообъектам присуща двойственная природа: они являются частицами, но имеют волной характер движения, т.е. микрообъекты обладают одновременно корпускулярными и волновыми свойствами.
Для описания движения микрочастиц используется вероятностный подход , т.е. определяется не их точное положение, а вероятность нахождения в той или иной области околоядерного пространства.
Состояние (в квантовой механике синоним слова «движение») электрона в атоме описывается с помощью квантово-механической модели - электронного облака. Электронное облако графически отражает вероятность пребывания электрона в каждом участке электронной орбитали. Под электронной орбиталью следует понимать область пространства, где с определенной долей вероятности (около 90-95%) возможно пребывание электрона. Электронная орбиталь каждого электрона в атоме называется атомной орбиталью (АО) , в молекуле – молекулярной орбиталью (МО) . Полное описание состояния электронного облака осуществляется с помощью уравнения Шредингера. Решение этого уравнения, т.е. математическое описание орбитали, возможно лишь при определенных дискретных (прерывных) значениях квантовых чисел
Главное квантовое число n
Орбитальное l ( l n )
Магнитное квантовое число m ( m l )
Спиновое квантовое число S ( m s )
Главное квантовое число (n) определяет основной запас энергии электрона, т.е. степень его удаления от ядра или размер электронного облака (орбитали). Оно принимает любые целочисленные значения, начиная с единицы. Для реально существующих атомов в основном состоянии n = 1÷7.
Состояние электрона, которое характеризуется определенным значением n, называется энергетическим уровнем электрона в атоме. Электроны, имеющие одинаковые значения n, образуют электронные слои (электронные оболочки ), которые можно обозначить и цифрами и буквами.
Значение n…………………………….1 2 3 4 5 6 7
Обозначение электронного слоя …….K L M N O P Q
Наименьшее значение энергии соответствует n = 1, и электроны с n = 1 образуют ближайший к ядру атома электронный слой, они более прочно связаны с ядром.
Орбитальное (побочное или азимутальное) квантовое число l определяет орбитальный момент количества движения электрона и характеризует форму электронного облака. Оно может принимать целочисленные значения от 0 до (п-1). Для реально существующих атомов в основном состоянии l принимает значение 0,1,2 и 3.
Каждому значению l соответствует орбиталь особой формы. При l =0 атомная орбиталь, независимо от значения главного квантового числа, имеет сферическую форму (S-орбиталь). Значению l=1 соответствует атомная орбиталь, имеющая форму гантели (p- орбиталь). Более сложные формы у d- и f-орбиталей (l =2, l =3).
Каждому n соответствует определенное число значений орбитального квантового числа, т.е. энергетический уровень представляет собой совокупность энергетических подуровней. Число энергетических подуровней каждого электронного слоя равно номеру слоя, т.е. значению главного квантового числа. Так первому энергетическому уровню (n=1) соответствуют один подуровень-s; второму (n=2) – два подуровня s и p; третьему (n=3) – три подуровня s, p, d; четвертому (n=4) – четыре подуровня s, p, d, f.
Таким образом, энергетический подуровень – это состояние электрона в атоме, которое характеризуется определенным набором квантовых чисел n и l . Такое состояние электрона, соответствующее определённым значениям n и l (тип орбитали), записывается в виде сочетания цифрового обозначения n и буквенного l , например 4p (n = 4; l = 1); 5d (n = 5; l = 2).
Таблица 1
Соответствие обозначений орбитального квантового числа и подуровня
Магнитное квантовое число определяет значение проекции орбитального момента количества движения электрона на произвольно выделенную ось, т.е. характеризует пространственную ориентацию электронного облака. Оно принимает все целочисленные значения от –l до +l , в том числе значение 0.
Так, при l =0 m=0. Это значит, что S- орбиталь имеет одинаковую ориентацию относительно трёх осей координат. При l =1 m может принимать три значения: -1; 0; +1. Это значит, что могут быть три р-орбитали с ориентацией по координатным осям x, y, z.
Любому значению l соответствует (2l +1) значений магнитного квантового числа, т.е. (2l + 1) возможных расположений электронного облака данного типа в пространстве. S – состоянию соответствует 20 + 1 = 1 одна орбиталь, p- состоянию 21 + 1 = 3 три орбитали, d-состоянию 22 + 1 = 5 пять орбиталей, f-состоянию 23 + 1 = 7 семь орбиталей и т.д.
Состояние электрона в атоме, которое характеризуется определёнными значениями квантовых чисел n, l , m , т.е. определёнными размерами, формой и ориентацией в пространстве электронного облака, называется атомной электронной орбиталью .
Спиновое квантовое число S(m s) характеризует собственный механический момент электрона, связанный с вращением его вокруг своей оси. Оно имеет только два значения +и –.
Итак, подводя итоги изложенному выше, можно составить блок-схему «Квантовые числа» (таблица 2).
Таблица 2. Блок-схема «Квантовые числа»
|
Квантовое число |
Название |
Физический смысл |
Какие значения принимает |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
главное квантовое число |
определяет общий запас энергии и размеры электронных орбиталей; характеризует энергетический уровень |
nN (теоретически) n 1 2 3 4 5 6 7 (практически) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
l (эль) |
орбитальное (азимутальное) квантовое число |
определяет форму атомной орбитали характеризует энергетические подуровни |
l (теоретически) l 0 1 2 3 (практически) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
m l (эм) |
магнитное квантовое число |
показывает ориентацию электронного облака в пространстве |
от –l до +l все целые числа, включая ноль при l =3 3 -2 -1 0 +1 +2 +3 Поведение электронов в атомах подчиняется принципу запрета, В. Паули : в атоме не может быть двух электронов, у которых были бы одинаковыми все четыре квантовых числа. Согласно принципу Паули, на одной орбитали, характеризующейся определёнными значениями квантовых чисел n, l и m может находиться либо один электрон, либо два, но различающихся значением s. Орбиталь с двумя электронами, спины которых антипараллельны (квантовая ячейка), схематически можно изобразить так: Максимально в одном электронном слое может быть 2n 2 электронов, так называемая емкость электронного слоя. В таблице 3 приведены значения квантовых чисел для различных состояний электрона, а так же указано максимальное число электронов, которое может находиться на том или ином энергетическом уровне и подуровне в атоме. Таблица 3. Квантовое состояние электронов, емкость энергетических уровней и подуровней.
Расположение электронов по слоям и орбиталям изображают в виде электронных конфигураций . При этом электроны размещаются согласно принципу минимальной энергии : наиболее устойчивое состояние электрона в атоме соответствует минимально возможному значению его энергии. Конкретная реализация этого принципа отражается с помощью принципа Паули (см. стр. 8), правила Хунда, а также правила Клечковского. П равило Хунда: в пределах энергетического подуровня электроны располагаются так, чтобы их суммарный спин был максимальный . Правило Клечковского : орбитали заполняются электронами в порядке возрастания их энергии, которая характеризуется суммой (n + l ). При этом, если сумма (n + l ) двух разных орбиталей одинакова, то раньше заполняется орбиталь , у которой главное квантовое число меньше. Последовательность заполнения электронных энергетических подуровней в атоме смотрите в таблице 4. Таблица 4. Порядок заполнения орбиталей по сумме главного и побочного квантовых чисел (n + l ) .
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Возьмем мысленно атом любого химического элемента. В каких состояниях находятся в нем электроны? Из предыдущего параграфа ясно, что для каждого электрона необходимо знать значения четырех квантовых чисел, характеризующих его состояние. Но нам пока не известно, сколько электронов находятся в каждом состоянии. Какие состояния более, а какие менее вероятны? Ответ на эти вопросы дают два важнейших принципа (закона). Первый из них открыт в 1925 г. швейцарским физиком В. Паули (1900-1958) и назван его именем - принцип Паули.
Все электроны в атоме находятся в разных состояниях, т.е. характеризуются разными наборами четырех квантовых чисел.
В данном случае понятием «принцип» обозначен один из фундаментальных законов природы, который делает атом тем, что он есть, - микрочастицей вещества с индивидуальной электронной структурой для каждого химического элемента. Роль принципа Паули в природе становится яснее, если представить себе, что он не действует. Тогда электронное окружение ядра атома теряет структурную определенность. Все электроны скатываются в какое-то одно наиболее выгодное состояние.
Следует отметить, что этот закон справедлив для всех фермионов.
Из принципа Паули вытекает следствие, определяющее вместимость орбитали, т.е. число электронов, которые могут образовать единое электронное облако. Выбрав любую из орбиталей, мы фиксируем первые три квантовых числа. Например, для орбитали 2р 2: п = 2, /= 1, mj= 0. Но можно изменять еще спиновое квантовое число m s Получаются два набора квантовых чисел:
Следовательно, орбиталь вмещает не более двух электронов, и в атомах могут быть одно- и двухэлектронные облака.
Два электрона, находящиеся на одной орбитали, называют электронной парой.
Зная вместимость орбитали, легко понять, что вместимость энергетического подуровня равна удвоенному числу орбиталей (табл. 5.1).
Таблица 5.1
Структура подуровней в атомах
Совокупность электронов одного энергетического подуровня называют подоболочкой атома.
Вместимость энергетического уровня складывается из вместимости подуровней (табл. 5.2). В первой колонке таблицы кроме значений главного квантового числа приведены буквенные обозначения для электронных оболочек атома.
Таблица 5.2
Структура энергетических уровней в атомах
Совокупность электронов одного энергетического уровня называют оболочкой атома.
Реальное заполнение («заселение») орбиталей, подуровней и уровней электронами определяет второй принцип - принцип наименьшей энергии.
Основному (устойчивому) состоянию атома соответствует минимальная суммарная энергия электронов.
Состояния атома с повышенной энергией называются возбужденными. Атом в возбужденном состоянии неустойчив в том смысле, что за очень короткое время (~10 -8 с) переходит в основное состояние, излучая кванты энергии.
Любая физическая система тем устойчивее, чем меньше ее потенциальная энергия. Поэтому мы неизменно наблюдаем, что брошенное тело надает на землю или скатывается с горки вниз, согнутая пружина выпрямляется и т.д. Также и электронные оболочки атомов находятся в устойчивом состоянии, если общий запас энергии электронов минимален. Набор возможных энергетических состояний атома мы уже знаем (см. рис. 5.7). Рассмотрим, как соответствующие подуровни и уровни заселяются электронами. При этом строго выполняется принцип Паули, который имеет приоритетное значение по отношению к принципу наименьшей энергии и не нарушается. Будем изображать электронную структуру атомов с помощью энергетических диаграмм и электронных формул. Энергетическая диаграмма представляет собой часть общей последовательности подуровней (см. рис. 5.7), содержащую заселенные подуровни. В электронной формуле перечисляются заселенные подуровни в порядке возрастания энергии с указанием числа электронов верхними индексами. Первые два элемента периодической системы можно представить диаграммами I и II. Па диаграмме показано, что положение 1л*-уровня в атоме гелия ниже, чем в атоме водорода, так как у гелия заряд ядра больше и электроны сильнее притягиваются к ядру. Вместимость первого энергетического уровня в атоме гелия исчерпана.

У следующих за гелием элементов заселяется второй энергетический уровень. Рассмотрим энергетические диаграммы трех ближайших элементов - лития, бериллия и бора (диаграммы III, IV и V).

У лития и бериллия заселяется подуровень 2s. Пятый электрон атома бора начинает заселение подуровня 2р в соответствии с принципом Паули. У атомов углерода и азота заселение этого подуровня продолжается (диаграммы VI и VII).

В структуре этих элементов проявляется еще одна важная закономерность формирования электронных оболочек - правило Хунда (1927).
Основном} 7 состоянию атома соответствует заселение электронами максимального числа энергетически равноценных орбиталей. При этом электроны имеют одинаковые значения спиновых квантовых чисел (все +1/2 или все -1/2).
При рассмотрении энергетической диаграммы атома кажется, что перенесение электрона между одинаковыми орбиталями 2р не изменяет его энергию. В действительности при движении электронов по разным орбиталям уменьшается отталкивание между ними, за счет чего потенциальная энергия все-таки уменьшается. Электроны, занимающие орбитали поодиночке, называют неспаренными. Далее при изучении природы химических связей мы увидим, что валентность атомов определяется числом неспаренных электронов. Азот имеет три неспаренных электрона, и он действительно трехвалентен. Достаточно вспомнить формулу аммиака NH 3 . Углерод, согласно диаграмме, двухвалентен. Однако при поглощении сравнительно небольшой энергии один электрон переносится с подуровня 25 на подуровень 2р. Углерод переходит в возбужденное состояние с электронной формулой s 2 2s { 2p s . В этом состоянии он имеет четыре неспаренных электрона. Свободный атом может пребывать в возбужденном состоянии лишь очень короткое время. Но, оказываясь в составе молекулы, атом получает добавочные электроны для заселения орбиталей. После этого исключается возможность перехода в основное состояние, и атом углерода остается четырехвалентным. Фактически, энергия, затраченная на возбуждение электрона, компенсируется энергией образования дополнительных химических связей.
Заселение 2р-орби галей вторыми электронами происходит у кислорода, фтора и неона (диаграммы VIII, IX, X). При этом последовательно уменьшается число оставшихся неспаренных электронов и, соответственно, валентность атомов. Это соответствует элементарным знаниям о свойствах кислорода, фтора и неона: кислород двухвалентен, фтор одновалентен, а неон химических связей не образует, т.е. его валентность равна нулю.

Мы увидели, что у элементов от лития до неона заселяется электронами второй энергетический уровень, и именно поэтому они составляют
- 2- й период таблицы Менделеева. У следующего за неоном натрия начинается заселение третьего энергетического уровня, и далее формируется
- 3- й период по мере заселения подуровней 35 и 3р. Энергетические диаграммы и электронные формулы элементов от натрия до аргона можно представить в сокращенной форме, обозначив повторяющийся у них набор электронов неона как . Смысл сокращенной электронной формулы заключается в том, что в ней указываются только валентные электроны атома. Остальные электроны, составляющие электронный остов атома , для химии имеют второстепенное значение. В качестве примера напишем сокращенные формулы и диаграммы натрия, кремния и аргона (диаграммы XI, XII и XIII).

Число химических элементов во 2-м и 3-м периодах определяется суммарной вместимостью 5- и /^-подуровней, составляющей восемь электронов. Таким образом, получает физическое объяснение наличие в таблице Менделеева именно восьми групп. Становится понятной и причина наблюдаемого сходства химических элементов в группах. Сравнивая энергетические диаграммы элементов одной и той же группы - лития и натрия, углерода и кремния и т.д., - мы замечаем, что они характеризуются одинаковой заселенностью внешнего энергетического уровня. Из этого вытекает, в первую очередь, одинаковая валентность атомов, чем и обусловлено сходство химических свойств. Но электронные структуры атомов, взятые в целом, различны. От периода к периоду увеличивается число электронных оболочек, что влечет за собой и увеличение радиусов атомов. Поэтому, как уже отмечалось, наряду со сходством наблюдается и определенная направленность в изменении свойств.
Из электронных формул и энергетических диаграмм атомов очевидно, что в группах IA и ПА электроны заполняют внешний 5-подуровень, а в группах I НА-V111А - внешний p-подуровень. Это дает основание для классификации химических элементов на блоки. Первые две группы рассматривают как блок s-элементов, а группы с ША по VIIIА - как блок р -элементов.
В таблице Менделеева имеются еще группы с теми же номерами, но с добавлением символа «В». Как объясняется существование этих групп? Из рис. 5.6 очевидно, что подуровень 3d по энергии находится между подуровнями 45 и 4р. В таблице Менделеева 4-й период, как и предыдущие, начинается двумя 5-элементами - калием ([Аг]45 л) и кальцием (fАг]4л 2). После кальция начинается заселение не подуровня р , как во 2-м и 3-м периодах, а подуровня 3d , вместимость которого составляет 10 электронов. Электроны на ^-подуровне один за другим появляются у скандия и следующих за ним элементов, включая цинк. Они входят в блок d-элементов. Нумерация групп d-элементов основана на том, что в группах с III по VIII имеется одинаковое число электронов на двух верхних подуровнях как у р-элементов (5- и р-подуровни), так и у d-элементов (5- и d-подуровни). Группы IB и ПВ нумеруются по заселенности внешнего 5-подуровня, подобно 5-элементам.
Четвертый период завершают p-элементы, следующие за цинком. Заполненный Зг/-нодуровень у них энергетически стабилизируется и становится ниже подуровня As. Это объясняется разным ходом понижения энергии орбиталей 45- и 3^/-подуровней по мере увеличения заряда ядра атома (рис. 5.9).

Рис. 5.9.
Пример 5.1. Напишите сокращенные электронные формулы железа и криптона.
Решение. Как у железа, так и у криптона ближайший предшествующий благородный газ - аргон (Z = 18). У железа (Z = 26) на заполнение верхних 45- и Зб/-подуровней остается восемь электронов. Пишем формулу 45 2 3rf 6 . У криптона (Z = 36) добавляется еще 10 электронов, которые полностью заселяют подуровни 3d и Ар. Заполненный 3d -подуровень ставим в формуле до 45-подуровня: [Аг]3 10 45 2 4/? 6 .
Пятый период таблицы Менделеева по структуре аналогичен четвертому. Оба они содержат по 18 химических элементов. В 5-м периоде рубидий и стронций принадлежат к 5-блоку элементов, 10 элементов от иттрия до кадмия принадлежат к d-блоку и оставшиеся шесть элементов от индия до ксенона - к р- блоку.
Далее следуют самые длинные 6-й и 7-й периоды, содержащие но 32 элемента. В 6-м периоде добавляется семейство из 14 химических элементов - от лантана до иттербия, называемых лантаноидами , а в 7-м - аналогичное семейство актиноидов - от актиния до нобелия. В их атомах заполняются электронами 4/- и 5/-подуровни соответственно. Лантаноиды и актиноиды составляют блок /-элементов. Вследствие особых характеристик орбиталей /-подуровней, все лантаноиды и все актиноиды проявляют между собой большое сходство но химическим свойствам.
Пример 5.2. Чем объясняется, что семейства /-элементов содержат по 14 химических элементов?
Решение. В соответствии с формулой 2/+1 подуровень f (1 = 3) состоит из семи орбиталей. Поэтому его вместимость 14 электронов, и постепенное заполнение /-подуровня происходит у 14 химических элементов.
Таким образом, краткий обзор электронной структуры атомов в общих чертах раскрывает физическую основу периодичности изменения свойств химических элементов и, следовательно, периодического закона Д. И. Менделеева. Коротко можно сказать, что периодический закон является следствием принципа Паули и принципа наименьшей энергии.
Читайте также...
- Вероятностно-статистические методы исследований Вероятностно статистические методы
- Воронежский государственный архитектурно-строительный университет Воронежский государственный строительный
- Монашеские и духовно-рыцарские ордена западной европы периода средневековья
- Происхождение и единство человеческих рас