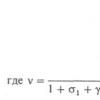Наиболее распространены фосфорсодержащие органические соединения. Фосфорорганические соединения (ФОС). Признаки отравления ФОС
В разумных количествах фосфор необходим человеческому организму. Это основа полноценного функционирования его нервной системы, прочности зубов, ногтей и костной ткани. Однако фосфорорганические вещества (ФОВ или ФОС), с которыми человеку приходится сталкиваться в бытовых или рабочих условиях, чрезвычайно токсичны и несут опасность при несоблюдении мер предосторожности. Отравление ФОС может вызвать развитие судорог, впадение человека в состояние комы и даже летальный исход .
Соединения фосфора в быту
Фосфорорганические соединения представляют собой сложные вещества с большим содержанием фосфорных кислот. Чаще всего они представлены в виде твердых либо жидких летучих субстанций с характерным керосиновым запахом. ФОС легко растворяются в жире и плохо растворимы в воде
.
Отравление фосфорорганическими соединениями может произойти несколькими способами: через органы пищеварительной и дыхательной систем, при соприкосновении с кожными покровами .
Причинами отравления могут стать:
- вода, отравленная токсическими препаратами;
- употребление плохо вымытых фруктов либо овощей, обработанных препаратами с содержанием фосфорорганических веществ;
- прием нестерилизованного коровьего молока от животного, питавшегося травой, отравленной химикатами;
- вдыхание паров ФОС при обработке помещений, садов и сельскохозяйственных культур от насекомых.
Признаки отравления ФОС
Фосфорорганические соединения, попавшие внутрь организма человека, моментально всасываются через слизистые оболочки ротовой полости и желудочно-кишечного тракта, после чего проникают в кровь. Опасность интоксикации веществами, содержащими фосфор, заключатся в том, что более половины таких препаратов склонны к преобразованию в организме человека в соединения с более токсичными свойствами . Кроме того такие яды характеризуются циклическим превращением, что ведет к возникновению рецидивов у 10% единожды отравленных людей.
При интоксикации фосфорорганическими соединениями в первую очередь страдает нервная система человека. Отравление ФОВ протекает в 3 стадии:

- головокружение и головная боль;
- ухудшение зрения;
- повышенное пото- и слюноотделение;
- снижение ритма сердца;
- мышечная слабость, судороги отдельных мышц;
- усиление перистальтики кишечника, появление спастических болей, диарея;
- нарушение дыхательной функции;
- поражение ЦНС, выражающееся возбуждением, беспокойством, появлением чувства страха, одышкой, перепадами артериального давления, увеличением и снижением температуры тела.
- Стадия судорог и гиперкинезов. Симптоматика первого этапа ослабевает, но добавляются дополнительные признаки интоксикации:
- заторможенность;
- отсутствие реакции зрачков на свет;
- ярко выраженный цианоз кожных покровов;
- тахикардия;
- повышение, а затем резкое падение артериального давления;
- отек легких.
У человека наблюдаются гиперкинезы – частое подергивание всех мышц тела, наблюдается общий мышечный гипертонус, судороги. В некоторых случаях на данной стадии происходит развитие токсического гепатита, пневмонии, поражения почек.
- Стадия паралича. У человека происходит ослабление всех рефлексов, сужение зрачков, повышение потоотделения. Мышцы тела находятся в паралитическом состоянии, наблюдается нарушение дыхания и признаки экзотоксического шока. Ритм сердца может быть чрезмерно повышенным – свыше 120 ударов в минуту либо слишком сниженным – до 20 ударов в минуту. В ряде случаев наблюдается коматозное состояние больного, признаки коллапса. При остром отравлении может наступить смерть в результате удушья, связанного с нарушениями функционирования дыхательной системы.
Время проявления характерных признаков отравления зависит от пути проникновения токсина в организм. При поступлении большой дозы яда через органы пищеварения первые симптомы интоксикации будут заметны в течение 10-15 минут , спустя 20-30 минут вероятно возникновение коматозного состояния, а по истечении от 3 до 9 часов может наступить смерть. В случае затяжного течения острого отравления летальный исход случается спустя 2-5 дней.
Признаки отравления при проникновении яда через кожу проявляются гораздо позже – через 2-3 суток. В этом случае первыми симптомами интоксикации могут стать головная боль, общая слабость, потливость в месте соприкосновения кожи с ядом.
Диагностика интоксикации
 Диагностика отравления фосфорорганическими соединениями начинается с внешних признаков: от больного будет исходить характерный бензиново-чесночный запах
. Помимо этого, об интоксикации фосфорорганическими отравляющими веществами будут свидетельствовать нарушение зрения, чрезмерное потоотделение, судороги и подергивания отдельных мышц.
Диагностика отравления фосфорорганическими соединениями начинается с внешних признаков: от больного будет исходить характерный бензиново-чесночный запах
. Помимо этого, об интоксикации фосфорорганическими отравляющими веществами будут свидетельствовать нарушение зрения, чрезмерное потоотделение, судороги и подергивания отдельных мышц.
После зрительного осмотра проводится биохимический анализ крови, помогающий подтвердить диагноз. При молниеносном протекании отравления через полчаса после контакта с токсином у человека появляются сильные судороги.
Первая помощь
Учитывая высокую скорость всасывания ФОС в кровь, первая помощь при отравлении должна быть оказана незамедлительно
. Мероприятия по ее оказанию зависят от пути проникновения токсинов в организм:
- При пероральном приеме фосфорорганических соединений больному делают промывание желудка большим количеством теплой воды либо слабоконцентрированным раствором марганцовки. После очищения желудка отравившемуся человеку необходимо принять активированный уголь или иной сорбент. Можно сделать промывание кишечника солевым и содовым растворами.
- При отравлении через органы дыхания необходимо срочно вынести больного на свежий воздух. Рекомендуется сделать ему промывание желудка и вызвать скорую помощь.
- При попадании фосфорорганических веществ на кожу место соприкосновения необходимо тщательно промыть прохладной водой с использованием мыла либо полностью окунуть человека в воду. При контакте кожных покровов с чистым фосфором необходимо следить, чтобы пораженный участок всегда был влажным во избежание воспламенения паров вещества с кислородом. Поврежденные участки кожи можно обрабатывать раствором соды.
После оказания доврачебной помощи необходимо безотлагательно доставить больного в медицинское учреждение или вызвать карету скорой помощи.
Правильно и своевременно оказанная первая помощь увеличивает шансы на выздоровление человека даже при незначительном контакте с токсином.
Лечение
Мероприятия, оказываемые в лечебном учреждении, направлены на выведение из организма токсинов и восстановление пораженных органов и систем. Для этого медицинским персоналом выполняются следующие действия:
- очищение желудка и кишечника, форсированный диурез и гемодиализ;
- введение глюкозы внутривенно;
- применение антидотов, к которым относятся диазепам, изонитрозин;
- введение атропин сульфата в качестве противоядия ;
- проведение мероприятий, направленных на устранение нарушений ритмов сердца, сердечной и дыхательной недостаточности, паралича дыхания;
- симптоматическая противошоковая терапия;
- введение препаратов для борьбы с судорожным состоянием;
- назначение аденозинтрифосфата и витаминных комплексов для профилактики поражений центральной нервной системы.
Во время лечения отравления ФОС в рационе больного должна присутствовать жирная и молочная пища , способствующая быстрому распределению фосфора.
Профилактика
Во избежание отравления ФОС при работе с ними важно придерживаться следующих правил:
- носить закрытую одежду во избежание контакта ядовитых веществ с кожей;
- при попадании токсинов на одежду нужно немедленно снять ее, волосы и ногти – состричь;
- при работе с фосфорорганическими веществами необходимо соблюдать меры предосторожности: использовать респиратор, не курить и не обедать на рабочем месте;
- в быту препараты с ФОС необходимо хранить в недоступных для детей местах.
Отравление фосфором в ряде случаев приводит к тяжелым поражениям нервной системы и остальных органов человека . При первых признаках обнаружения интоксикации фосфорорганическими соединениями необходимо срочно обратиться в клинику. Это может спасти жизнь и не допустить хронических заболеваний, связанных с отравлением.
В начале XX века было установлено, что фосфорорганические со-
единения играют большую роль в жизни живых организмов. В 30-е годы XX века были синтезированы органические соединения фосфора, характеризуемые высоким токсическим действием. Именно в это время были синтезированы такие отравляющие вещества, как табун, зарин, зоман и др. Фосфорорганические соединения находят разнообразное применение в народном хозяйстве. Многие из них используют в производстве термостойких пластмасс (диалиловый эфир хлорметилфосфорной и фенилфосфоновой кислот используется в производстве оргстекла специального назначения: высокопрозрачное, термостойкое, химически инертное). Отдельные фосфорорганические соединения
применяют для обработки натуральных и синтетических волокон для придания им негорючести. Некоторые эфиры фосфоновых и фосфиновых кислот используют для получения химически стойких лаков, пленок, клеев. Третичные фосфины и другие соединения фосфора используют в качестве катализаторов.
В нефтехимической промышленности фосфорорганические соединения применяют как присадки к маслам и бензинам для улучшения их качества. Соединения типа триарилфосфатов используют как огнестойкие гидрав-
лические жидкости.
Моно- и диалкилфосфиты с восемью и десятью атомами углерода нашли применение в качестве поверхностно-активных веществ в текстильной промышленности. Диалкилдитиофосфаты применяют как флотореагенты
для разделения металлов руд. Особенно широко их применяют для разделения металлических руд золота, серебра, меди, цинка и т. д., а также в технологии получения урана из руд и для его очистки.
Фосфорорганические соединения по характеру связи фосфора с углеродом можно классифицировать на две группы:
1) Р-С соединения, в которых атом фосфора непосредственно связан с одним, или несколькими атомами углерода;
2) Р-О-С соединения, в которых атом фосфора связан с атомом углерода через кислород.
В свою очередь Р-С соединения подразделяются на следующие
подгруппы:
1) фосфины, производные РН 3 ; первичные R-РН 2 ,
вторичные R 2 РН и третичные R 3 P;
2) производные фосфонистой кислоты R -Р(ОН) 2 ;
3) производные фосфинистой кислоты R 3 -Р(ОН);
4) производные фосфиновой кислоты R 2 -Р ОН
5) производные фосфоновой кислоты
6) фосфораны R Х РГу (х + у = 5).
Р-О-С соединения подразделяются на ряд подгрупп, в которых атом фосфора является пятивалентным:
1) производные фосфорной кислоты
2) производные пирофосфорной кислоты
3) полимерные соединения (полиэфиры)
Кроме перечисленных известны и другие органические соединения фосфора: тиосоединения, металлорганические соединения, циклические фосфорсодержащие и др.
Несмотря на большое разнообразие соединений фосфора и широкое их применение в народном хозяйстве пожарная опасность их изучена далеко не полно. Остановимся на характеристике пожарной опасности отдельных
видов этих соединений.
Фосфины можно рассматривать как производные фосфористого водорода РН 3 , атомы водорода которого замещены углеводородными радикалами. Различают фосфины первичные RРН 2 , вторичные R 2 PН и третичные R 3 Р. Первичные и вторичные фосфины получают взаимодейcтвием фосфористого водорода с галогеналкилами.
Третичные фосфины получают взаимодействием треххлористого фосфора с магнийгалогеналкилами.
Первичные, вторичные и третичные фосфины, содержащие низшие алкильные радикалы, являются жидкими веществами с отвратительным запахом. Лишь метилфосфин СН 3 РН 2 является бесцветным газом. Фосфины не растворимы в воде. Легко окисляются под действием окислителей с выделением тепла, что может привести к самовозгоранию. На воздухе жадно поглощают кислород. Поэтому низшие фосфины на воздухе самовоспламеняются.
Третичные фосфины, содержащие в радикале четыре и более атомов углерода, являются твердыми веществами; в воде не растворяются. На воздухе окисляются медленно и имеют сравнительно невысокую температуру самовоспламенения. Например, трибутилфосфин (С 4 Н 9) 3 Р имеет температуру самовоспламенения 200 °С.
Все фосфины характеризуются высокой токсичностью, так как легко взаимодействуют с ферментами живого организма и парализуют нервную систему.
С увеличением длины углеродной цепи радикалов повышается температура кипения и самовоспламенения фосфинов. Первичные фосфины имеют более низкую температуру кипения, чем вторичные; вторичные фосфины имеют более низкую температуру кипения, чем третичные. Так, триамилфосфин (С 5 Н 11) 3 Р имеет температуру плавления 29 °С, а высшие гомологи - более 50 °С.
Фенилфосфин (С 6 Н 6)РН 2 и дифенилфосфин (С 6 Н 5) 2 РН являются бесцветными жидкостями, а трифенилфосфин (С 6 Н 5) 3 Р представляет собой твердое вещество с температурой плавления 80 °С. Жидкие фосфины не ассоциированы и поэтому легко испаряются.
Энергия разрыва связи Р-R довольно велика. Так,
энергия связи фенильного радикала составляет 293-314 кДж/моль, а алкильного радикала 276 кДж/моль. Поэтому при нагревании в атмосфере водорода или инертного газа фосфины начинают разлагаться при температуре более 300°С.
С галогенидами металлов фосфины легко образуют комплексные соединения, которые используются как катализаторы в органическом синтезе. С ненасыщенными соединениями фосфины вступают в реакцию присоединения, образуя вещества с характерными окрасками.
Третичные фосфины легко присоединяют и другие вещества: галогены, серу, сероводород, галоидные алкилы и т. д.
Под действием азотной кислоты первичные и вторичные
фосфины переходят в фосфорсодержащие кислоты, а третичные - в оксиды фосфинов.
Все эти вещества горючи. Производные этих кислот представляют собой либо жидкости, либо твердые вещества. При нагревании плавятся и, не разлагаясь, переходят в жидкость. На воздухе в жидком состоянии устойчивы, но при нагревании до температуры кипения разлагаются. Температура вспышки большинства этих соединений превышает 97 о С. Смеси их паров с воздухом являются взрывоопасными; нижний концентрационный предел воспламенения 0,5 - 0,8% (об.). Однако смеси взрывоопасных концентраций могут образовываться лишь при высоких температурах (выше 100 °С). Горят они ярким пламенем с выделением СО 2 , Н 2 О и Р 2 0 5 .
Производные фосфорсодержащих кислот находят применение в качестве пестицидов, а также в качестве пластификаторов и термостойких присадок в производстве пластмасс. Все эти производные являются весьма
ядовитыми веществами. К этой группе соединений относятся отравляющие вещества: табун, зорин, V-газ.
Производные фосфорсодержащих кислот можно успешно тушить водой, воздушно-механической пеной, диоксидом углерода или азотом.
Диэтилэтилфосфонат (диэтиловый эфир этилфосфоновой
кислоты) представляет собой бесцветную горячую жидкость с неприятным запахом; ядовит, в воде не растворяемся, тяжелее воды, плотность 1025 кг/м 3 при 25°С; при нагревании до 250°С разлагается; температура вспышки 105°С; хорошо тушится водой, воздушно-механической пеной.
Поскольку производные фосфорсодержащих кислот при нагревании до высокой температуры разлагаются с выделением различных веществ, состав которых зависит от температуры и условий процесса разложения, температура самовоспламенения этих веществ изменяется в
определенных пределах и лежит выше 400°С.
Фосфорорганические соединения типа Р-О-С нашли широкое практическое применение как инсектициды, фотореагенты, поверхностно-активные вещества и растворители. Наиболее широко применяют производные фосфористой кислоты Р(ОН) 3 - фосфиты и производные фосфорной кислоты Н 3 Р0 4 - фосфаты.
Неполные фосфиты (диметилфосфит, диэтилфосфит, дипропилфосфит, дибутилфосфит) интенсивно взаимодействуют с окислителями и самовозгораются. Вата, тряпки, стружка и другие подобные материалы, пропитанные этими соединениями, на воздухе самовозгораются.
Хлорпроизводные фосфитов при слабом нагревании разлагаются на галоидные алкилы и оксиды фосфора, энергично взаимодействуют с окислителями. Большинство фосфитов характеризуются как ГЖ. Наиболее опасными являются триметилфосфит, трихлорэтилфосфит. Триметилфосфит -бесцветная легкоподвижная летучая жидкость, с неприятным запахом, не растворимая в воде; при нормальном давлении температура кипения составляет 112°С. В этих условиях кипение не сопровождается разложением. Пары в смеси с воздухом образуют взрывоопасные концентрации. Температура вспышки 54°С. При нагревании до температуры выше 150°С разлагается на этан и оксиды фосфора.
Производные фосфорной кислоты Н 3 РО 4 представляют собой, главным образом, бесцветные с неприятным запахом токсичные жидкости. Температура вспышки выше 100°С. Низшие члены гомологического ряда фосфатов кипят при температуре выше 200 °С без разложения при нормальном давлении. Высшие члены гомологического ряда имеют температуру кипения, превышающую 300°С, причем кипение сопровождается их разложением. Продуктами разложения являются углеводороды и оксиды фосфора.
Температура самовоспламенения фосфатов 350 °С. Фосфаты не растворимы в воде; некоторые из них под действием воды разлагаются, например тригексилфосфат. Горение фосфатов как и других фосфорорганических соединений сопровождается образованием яркого пламени. Самовозгораются они под действием сильных окислителей. Хорошо тушатся водой, воздушно-механической пеной и инертными газами.
Пирофосфаты по степени пожарной опасности характеризуются также, как и фосфаты.
Тиофосфаты - производные тиофосфорной кислоты; представляют собой горючие вещества (жидкие или кристаллические); растворимы в воде; на воздухе устойчивы; могут самовозгораться под действием сильных окислителей; горение сопровождается образованием яркого пламени и выделением оксидов фосфора и серы; такие соединения, как тиофос, фосфомид, применяют в качестве инсектицидов.
Основой для синтеза негорючих термостойких пенопластов служат непредельные фосфонаты. Они легко полимеризуются, образуя фосфорорганические полимеры, которые придают термостойкость текстильным изделиям; используются также в качестве катионообменных смол.
Общие сведения Впервые синтез ФОС был осуществлен при помощи реакции этерифи- кации спиртов фосфорными кислотами в 1820 г. Уже в 1847 г. Французским ученым Тенардом были синтезированы многие фосфины.Однако интенсивному развитию исследований по химии ФОС послужили работы Михаэлиса и А.Е. Арбузова.
В 1903 и 1915 г.г. Михаэлис опубликовал фундаментальные работы по синтезу амидированных производных фосфорной, фосфиновой и тиофосфор- ной кислот. Открытая реакция Михаэлиса-Беккера дала возможность получать эфиры алкилфосфоновых кислот из галоидалкилов и диалкилфосфитов.
А.Е. Арбузов открыл новый путь получения соединений пятивалентного фосфора из эфиров кислот трехвалентного фосфора, который получил название «перегруппировки Арбузова». Способ синтеза эфиров фосфорной кислоты был опубликован А.Е. Арбузовым в 1906 г. Это легло в основу химии органических соединений и послужило широкому синтезу многих высокоактивных ингибиторов ХЭ, которые нашли широкое применение в качестве пластификаторов для пластмасс и резины, экстрагирующих веществ, антиоксидантов для смазочных масел, флотоагентов в горнорудной промышленности, лекарственных средств. Наибольшее применение органические соединения фосфора различной структуры находят в сельском хозяйстве в качестве инсектицидов, акарицидов, фунгицидов и регуляторов роста растений.
Изучение механизма действия ФОС начато в Германии с 1938 г. Параллельно аналогичные исследования проводились в Англии Эдрианом, Фельдбергом, Килби и др., в Советском Союзе - А.Г. Генецинским.
Поскольку первые созданные ФОС оказались чрезвычайно токсичными и опасными для теплокровных животных и человека, это побудило к изысканию новых соединений с избирательной токсичностью и исследованию их механизма токсического и селективного действия, метаболизма, изысканию средств антидотной терапии.
Из многих тысяч синтезированных в последнее время ФОС большая часть синтезирована в Советском Союзе в лабораториях А.Е. Арбузова и Б.В. Арбузова (октаметил, дитио, хлорофос и др.), М.И. Кабачника (М-74, М-81,
Р-2 и др.), Н.Н. Мельникова (меркаптофос, метилмеркаптофос, тиофос, ме- тафос, карбофос, фосфамид и др.). Существенный вклад в изучение механизма биологической активности ФОС, закономерностей антихолинэстеразной активности внесен М.И. Кабачником и его сотрудниками. Систематическое и плодотворное изучение вопросов токсикологии и механизма токсического действия ФОС проводится в лабораториях М.Я. Михельсона, К.С. Шадурско- го, С.Н. Голикова, В.И. Розенгарта, Ю.С. Кагана, Ю.И. Кундиева и др.
Химическое строение большинства ФОС может быть выражено общей схематической формулой:
R1 O(S)
\ //
P / \
R2 X
где R1 и R2 - одинаковые или различные алкильные, алкоксильные, алкила- минные, арильные или арилокси группы.
По химическому строению ФОП можно разделить на 5 групп: производные фосфорной, тиофосфорной, дитиофосфорной, пирофосфорной и фосфоновых кислот.
В зависимости от различия в фосфорной группе ФОП выделяют 3 основные группы соединений: фосфаты (без атома серы), фосфоротиоаты (с одним атомом серы) и фосфородитиоаты (с двумя атомами серы).
В настоящее время известны десятки тысяч отдельных ФОС, их число возрастает с каждым днем и дать их полный перечень не представляется возможным.
ФОС могут находиться в различном агрегатном состоянии. Большинство из них представляют собой маслянистую жидкость или кристаллический порошок, нерастворимы либо плохо растворимы в воде и хорошо растворимы в органических растворителях. Многие из них имеют неприятный специфический запах. Плотность ФОС находится в пределах 1,1-1,7.
Среди ФОС имеются вещества с различной степенью летучести. К веществам, обладающим очень высокой летучестью (насыщающая концентра-
ция больше 10 мг/м), относятся димефокс, ДДВФ, фосдрин, тионовый изомер метилмеркаптофоса, тимет, зарин, ронелл и др. Летучесть в данном ряду
о
ФОС составляет 925; 145; 27; 23,3; 12,4; 12; 11 мг/м соответственно. К веществам с относительно высокой летучестью (1-10 мг/м) относятся зоман, октаметил, табун, тиоловый изомер меркаптофоса, препарат М-81, меркапто- фос, ТЭПФ, карбофос, диазинон и др. Летучесть их составляет 10; 9,5; 6; 4,5; 4; 3,67; 2,5; 2,26; 1,39 мг/м соответственно. ФОС со средней летучестью (0,1 мг/м3) являются метилнитрофос, байтекс, параоксон, фосфамидон, мета- фос, хлорофос, фосфамид и др., их летучесть составляет 0,82; 0,46; 0,41; 0,18; 14; 0,11; 0,11 мг/м соответственно. Низкой степенью летучести (менее 0,1
о
мг/м) обладают паратион, хлортион, дикаптон, тритион, гузатион, фенкап- тон и др., их летучесть - 0,09; 0,07; 0,05; 0,0057; 0,0042; 0,00085 мг/м3 соответственно. Следует отметить, что с возрастанием температуры летучесть ФОС значительно увеличивается.
ФОС достаточно стабильны при нейтральной pH, легко гидролизуются в щелочных растворах (pH 8,0 и выше), в меньшей степени в кислых растворах (при pH 2,0 и ниже). Фосфороамидаты гидролизуются в ходе катализируемой кислотой реакции даже при pH 4,0-5,0 и после образования кислоты разложение ускоряется из-за автокатализа. На скорость гидролиза оказывают влияние такие факторы, как характер заместителей в молекуле ФОС, катализаторы (азотсодержащие соединения, гидроксамовые кислоты, хлор, медь и др.), растворители, изменение температуры и pH.
При хранении, нагревании и перегонке некоторые ФОС способны к изомеризации. В результате изомеризации образуются продукты, которые более токсичны, чем исходное вещество. Токсикодинамика ФОС Механизм взаимодействия антихолинэстеразных соединений детально изучен. ФОС проявляют свое токсическое действие в результате того, что
имеют определенное сходство в строении с естественным субстратом ХЭ - АХ (как стериохимически, так и по реакционной способности). При достижении активного участка ХЭ их взаимодействие с ферментом сводится к фосфорилированию (или карбамилированию) гидроксила серина.
В общем виде реакцию АХ под действием АХЭ можно представить в виде последовательного процесса: активный фермент обратимо реагирует с АХ, в результате чего образует комплекс субстрат - фермент. В этом комплексе связь между ферментом и субстратом осуществляется не только за счет взаимодействия эстеразного центра с углеродом карбамильной группы АХ, но также за счет притяжения катионной головки АХ к анионному центру и взаимодействия неполярных групп субстрата с гидрофобными участками активного центра. Распад комплекса фермент - субстрат с образование продуктов реакции происходит в два этапа. На первом этапе ацетильный остаток субстрата присоединяется к ферменту, замещая содержащийся в нем протон, а остаток холина отщепляется в виде свободного холина. Далее следует де- ацетилирование эстеразного участка фермента с восстановлением его первоначальной структуры и образованием уксусной кислоты. Схематически это выглядит следующим образом:
O O
HE + RO - C - CH3 ^ E - C - CH3 + ROH
Фермент АХ Ацетилированный
холин - фермент
Различие во взаимодействии ХЭ с АХ и ФОС заключается в том, что в первом случае образуется ацетилированный фермент - весьма непрочное соединение, быстро подвергающееся гидролизу, в результате чего активные центры ХЭ освобождаются для новых реакций с АХ. При взаимодействии ФОС с ХЭ, эстеразный центр прочно связывается с остатком фосфорной кислоты, что приводит к образованию чрезвычайно устойчивого к гидролизу фосфорилиро- ванного фермента, неспособного реагировать с молекулами АХ и потому утратившему свою основную каталитическую функцию. Блокирование
ХЭ ФОС осуществляется в две фазы. В первой фазе подавление фермента обратимо. И только через определенный промежуток времени наступает вторая фаза. Первая фаза начинается сразу после контакта ингибитора с ферментом. Переход от обратимого ингибирования к необратимому происходит постепенно и зависит от температуры, строения и концентрации ингибитора.
Фосфорилирующая способность ФОС зависит от прочности эфирной связи фосфора с кислотным остатком и от дефицита электронов вокруг атома фосфора. Важное значение имеют стерические факторы и гидрофобные взаимодействия. Гидролиз фосфорилированной ХЭ происходит очень медленно. При этом устойчивость фосфорилированной ХЭ к гидролизу зависит от характера алкоксигрупп, связанных с фосфором. Легче всего происходит гидролиз в случае угнетения ХЭ диметиловыми эфирами кислот фосфора, значительно труднее - после воздействия диэтиловых, которые практически необратимо угнетают ХЭ диизопропиловые эфиры.
В связи с тем что ХЭ и ХР имеют в своем строении много общего, в механизме действия антихолинэстеразных соединений определенное значение может иметь их взаимодействие не только с ферментом, но и с ХР. При этом некоторые ФОС (фосфакол, ДФФ, паратион, армии и др.) могут проявлять как возбуждающее, так и блокирующее действие на ХР.
Для взаимодействия ФОС с ХР необязательно наличие в них катионной группы, определяющей возможность реакции с анионным пунктом рецептора. Блокирующее действие на ХР таких веществ, как диизопропилфторфос- фат, армии, фосфакол, связанно, по-видимому, с их взаимодействием с эсте- рофильным участком ХР. Влияние на Н-холинореактивные системы проявляется главным образом в случае введения больших доз этих препаратов.
Взаимодействие ФОС с ХЭ представляет собой реакцию фосфорилиро- вания, которую можно изобразить схематически:
EH + (RO^P(O)X^ (RO)2P(O)E + XH, где
EH - активная холинэстераза (механизм взаимодействия ХЭ и ФОС описан выше).
Сопоставление данных об антихолинэстеразной активности ФОС in vitro с их токсичностью и антихолинэстеразными свойствами in vivo показывает, что между этими свойствами не всегда имеется прямая зависимость. Это касается в первую очередь тиофосфатов (фосфоротиоатов). Например, такие тиофосфаты, как тиофос, карбофос, ЭПН, не вызывают угнетение холинэсте- разы in vitro, однако эти соединения отличаются выраженными антихолинэстеразными свойствами in vivo и высокой токсичностью.
Относительная токсичность всех исследуемых препаратов была выше, чем следовало бы предположить на основании данных об антихолинэстеразной активности in vitro и in vivo. Отсутствие строгой зависимости между ан- тихолинэстеразным действием in vitro и токсичностью свидетельствует о том, что в организме они превращаются в более активные антихолинэстераз- ные вещества.
При дермальном пути поступления ФОС, как и при пероральном, максимальное снижение активности ХЭ проявляется в первые сутки. Однако угнетение фермента нарастает медленнее, а активность энзима начинает восстанавливаться и достигает нормы несколько позже, чем при пероральном поступлении. Наблюдаемое более продолжительное изменение активности ХЭ при дермальном пути поступления связано с депонированием вещества в липоидах кожи и постепенным высвобождением из «депо».
Однако для некоторых соединений, например дифоса (абат), токсическое действие препарата больше выражено при дермальном пути поступления, чем пероральном. Это связано с тем, что дифос легко всасывается через неповрежденную кожу.
В большинстве случаев токсичность при ингаляционном поступлении ФОП в организм выше, чем при введении этой же дозы перорально.
Несмотря на количественные различия эффектов ингаляционного и пе- рорального действия, часто наблюдается их качественная однонаправленность, выражающаяся в сходстве изменений органов и биохимических показателей подопытных животных.
На высоких уровнях воздействия любая зависимость доза - эффект может быть представлена экспоненциальной кривой. В динамике эффективных доз более низкого уровня наблюдаются различные вариации, которые, однако, всегда сводятся к S-образным либо экспоненциальным кривым.
При пероральном поступлении ФОС более обоснованной является S- образная зависимость «доза - эффект», так как форма этой кривой отражает эффективную детоксикацию токсина в печени при воздействии малых доз. При ингаляционном пути поступления более оправданной будет экспоненциальная зависимость, так как препарат попадает непосредственно в кровь, поэтому даже малые дозы вызывают заметное угнетение ХЭ и АХЭ.
При однократном воздействии независимо от пути поступления в организм существует зависимость доза - эффект. Чем выше доза антихолинэсте- разного вещества, тем больше степень ингибирования АХЭ нервной ткани и выраженности интоксикации. Ингибирование АХЭ эритроцитов при воздействии одной и той же дозы вещества может существенно изменяться от ингибирования АХЭ нервной ткани. Влияние на ХЭ плазмы и внутренних органов (печень, почки, селезенка, сердце, мышцы) также зависит от дозы. Однако между степенью ингибирования активности холинэстеразы в различных биосубстратах существует диспропорция, в некоторых случаях значительная. Для отдельных веществ ХЭ плазмы более чувствительна к ингибированию, чем АХЭ эритроцитов, однако чаще наблюдается обратная зависимость.
Степень ингибирования активности ХЭ плазмы не всегда соотносится с тяжестью интоксикации. Типичная холинергическая интоксикация отмечается только при значительном ингибировании АХЭ нервной ткани.
Некоторые фосфорорганические инсектициды оказывают ингибирующее действие на карбоксилэстеразы тканей (например, малатион) в дозах, которые ниже уровней, влияющих на АХЭ и ХЭ. В связи с этим первичное ингибирование карбоксиэстераз может потенцировать токсичность веществ для теплокровных животных, детоксикация которых обычно осуществляется эс- теразами тканей.
Признаки интоксикации ФОС могут развиваться сразу или спустя несколько часов после воздействия. Для более липофильных соединений, которые требуют метаболической активации, симптомы интоксикации развиваются медленно и могут сохраняться несколько суток. Клиника острой интоксикации ФОС включает мускариноподобные и никотиноподобные нарушения, изменения со стороны центральной нервной системы и дыхания.
В зависимости от структуры вещества, скорости и направленности метаболизма может изменяться выраженность тех либо других нарушений центральной нервной системы.
Первые признаки холинергических симптомов в большинстве случаев появляются тогда, когда активность АХЭ в крови снижается до 50%. Общепризнано, что ингибирование активности АХЭ и ХЭ крови на 75% является индикатором опасности и требует принятия срочных мер по устранению воздействия вещества. Ингибирование активности АХЭ на 25-30% является пороговым эффектом, при котором отсутствуют какие-либо вредные последствия для здоровья. Активность ХЭ крови восстанавливается медленно и зависит от величины дозы и пути поступления. Однако такая зависимость между степенью ингибирования АХЭ и клиническими симптомами интоксикации наблюдается не всегда.
Общим в действии многих ФОС как в остром, так и хроническом опытах является зависимость доза - эффект.
С увеличением дозы вводимого вещества усиливается эффект независимого от пути поступления в организм. С нарастанием эффекта в антихоли- нэстеразные механизмы вовлекается все большее количество
физиологических систем. Степень выраженности ингибирования при введении одних и тех же доз зависит от видовой чувствительности животных. Вещества с большим антихолинэстеразным эффектом in vitro проявляют токсическое действие в первые часы после введения вещества. Для веществ с менее выраженными антихолинэстеразными свойствами in vitro, а также веществ, требующих предварительной активации (тионофосфаты), токсическое действие и антихолинэстеразный эффект проявляются в более поздние сроки.
При субхроническом и хроническом действии ФОС зависимость между степенью ингибирования активности ХЭ крови и тяжестью интоксикации может не сохраняться.
В некоторых случаях при повторном воздействии ФОС активность АХЭ эритроцитов угнетена почти на 100% без появления признаков интоксикации или без какой-либо связи с имеющимися симптомами, возникшими после облучения первой дозы вещества. Одной из причин такой реакции АХЭ эритроцитов на повторное воздействие ингибитора ХЭ является чрезвычайно низкая скорость восстановления ее активности.
При хроническом воздействии многих ФОС не отмечается корреляции между уровнем ХЭ крови и тканей. В различных тканях может наблюдаться разнонаправленный эффект (снижение или повышение активности ХЭ). В некоторых случаях наблюдаются фазовые изменения активности ХЭ крови и тканей. В восстановительном периоде иногда активность ХЭ в исследуемых биосубстратах подопытных животных выше, чем в контроле.
В условиях применения ФОС в сельском хозяйстве характерен прерывистый режим воздействия их на организм рабочих. Выяснение особенностей антихолинэстеразного действия ряда ФОС (афоса, циклофоса, рицида-П, ге- терофоса и др.) при мотонном и прерывистом режимах воздействия показало, что при прерывистом влиянии независимо от пути поступления в организм исследованные препараты оказывают менее выраженный антихолинэстеразный эффект, чем при монотонном.
Гистоморфологические и патобиохимические изменения во внутренних органах и головном мозге были выражены в меньшей степени, а восстановление активности холинэстеразы и нарушенных физиологических функций организма происходило быстрее при прерывистом воздействии, чем при монотонном.
Фосфор (Phosphorus), P – в чистом виде в природе не встречается, из соединений фосфора наибольшее значение имеет фосфат кальция - Ca 3 (PO 4) 2 , главная составная часть апатитов и фосфоритов.
Фосфор входит в состав животного организма – фосфат кальция – основа костной ткани, фосфор в виде различных соединений содержится в крови и лимфе. Фосфор необходим для жизни животных и растений.
Наибольшее значение имеет белый и красный фосфор.
Белый фосфор - мягкий, с запахом чеснока, неустойчив, огнеопасен, очень ядовит
Красный фосфор - твердый порошок темно-малинового цвета. Не ядовит, менее химически активен, не огнеопасен.
Физико-химические свойства соединений фосфора
Неорганические соединения фосфора.
Фосфорид цинка Zn 3 P 2 – порошок серовато-черного цвета, с запахом чеснока, не растворим в воде, спирте, хорошо во всех кислотах
Содержит 14 % фосфора, 70-80% цинка. Применяют как зооцид
Фосфаты – соли фосфорной кислоты. Значение имеет фосфат кальция – хорошо растворимая соль- примен.удобрение – суперфосфат.
Органические соединения фосфора
Большое количество фосфорорганических соединений сложного состава с различными техническими названиями. Их называют просто –ФОС . Они широко применяются в медицине, ветеринарии и сельском хозяйстве и промышленности
Химическое строение ФОС ов выражена следующей химической формулой:
R 1 и R 2 - различные или одинаковые алкилы, алкооксилы, алкиламины. Х – остаток неорганической или органической кислоты. Именно данная часть определяет физиологическую активность всего соединения (фтор, галогены, CN, и иные группы).
Органические соединения можно классифицировать по характеру инсектицидных свойств. Один из них обладают контактным действием (метафос, карбофос), другие- системным.
Эти соединения адсорбируются соком растений и сохраняют активность в отношении вредителей
Фосфорорганические соединения (ФОС) - это высокомолекулярные эфиры кислот фосфора (фосфорной, пирофосфорной, фосфористой, фосфоновой, фос финовой, тио- и дитиофосфорной, тиофосфористой) и их сернистых и азотистых производных.
В растениеводстве и животноводстве применяются более 25 ФОС, которые подразделяются на:
1.препараты контактного действия, вызывающие быструю гибель насекомых и клещей в момент контакта с ними,
2. препараты системного действия, всасывающиеся через листья и корневую систему и длительно циркулирующее вместе с соками растений, которые становятся токсичными для сосущих и грызущих насекомых в течение до 2 мес без вредного влияния на сами растения.
К препаратам контактного действия относятся: хлорофос, ДДВФ, метафос, дифос, этафос, циодрин, карбофос, диазинон, дурсбан, трихлорметафос и др.
К препаратам системного действия относятся: гардона, селекрон, токутион, фозалон, бутифос; к препаратам контактно-системного действия: антио, фосфапид, фталофос и гетерофос.
Патогенез. Фосфорорганические соединения - высоколипидотропные вещества. Они быстро всасываются через слизистые оболочки органов пищеварения, органов дыхания, через кожные покровы, накапливаются преимущественно в печени, головном мозге, сердечной и скелетныx мышцах, почках, внутренней жировой ткани, выделяется с молоком, мочой, фекалиями.
В оснсве биохимического механизма токсического, действия ФОС на организм животных лежит избирательная блокада фермента нервной ткани - ацетилхолинэстеразы, в результате чего в холинергических синапсах скапливается медиатор ацетилхолин, который, являясь что ведет к деполяризации мембран нервных клеток, падению потенциала покоя и резкому возрастанию процесса возбуждения центральной нервной системы.
Фосфорорганические пестициды в токсикологическом отношении представляют собой нервно-паралитические яды, в действии которых различают:
мускариноподобные,
никотиноподобные
курареподобные явления.
Мускариноподобные явления включают: миоз, бронхоспазм, слюнотечение, повышенное потоотделение, усиление перистальтики кишечника, понос.
Никотиноподобные - тремор скелетной мускулатуры, судороги конечностей, повышение кровяного давления, возбуждение и паралич центральной нервной системы.
Курарепо д обн ы е - ослабление тонуса скелетной мускулатуры, особенно шейных мышц, ослабление тонуса и паралич мускулатуры грудной клетки.
Крупный рогатый скот, овцы и козы более чувствительны к токсическому действию ФОС, чем свиньи, куры, утки и лошади. Молодые животные более чувствительны, чем взрослые.
Сим п томы. Отравление животных ФОС может протекать:
молниеносно,
хронически.
Мол н иеносное отравления возникали через 15-20 мин после обработки, особенно у животных, которые облизывали обработанные участки кожи у себя или у других животных. Проявлялись они вначале резким двигательным возбуждением, падением животных; нередко возникала характерная поза «молельщика», развивались гиперсаливация, гиперкинез и параличи языка, миоз, затрудненное дыхание. Возникали судороги конечностей и параличи, частые дефекация и мочеиспускание. Животные погибают через 1 -1,5 ч в коматозном состоянии при явлениях асфиксии и паралича мускулатуры конечностей и грудной клетки.
О с трое отравление в тяжелой степени у животных отмечаются беспокойство, пугливость, обострение реакции на звуковые и световые раздражения, которое сменяется угасанием зрительных и слуховых рефлексов и болевой чувствительности кожи; возникает разлитой тремор скелетной мускулатуры, нарушается координация движения, отмечается шаткость, животные зачастую падают. Выражены судороги конечностей клониче-ского и тонического характера.
Средней степени тяжести у животных наблюдают кратковременное слюнотечение, тремор скелетной мускулатуры, периодические приступы судорог, временами нарушение координации движения, понижение тонуса скелетной мускулатуры, явления бронхоспазма, частые дефекации и мочеиспускание. Через 1-2 сут эти явления исчезают, и животные выздоравливают клинически через 5-6 сут.
Легкой степени отравления у животных наблюдают периодическое незначительное слюнотечение кашель, приступы затруднения дыхания, понижение тонуса скелетной мускулатуры, усиление перистальтика кишечника. Эти явления через сутки полностью исчезают.
Хронической интоксикации у животных понижается активность приема корма, возникают общее угнетение, малая подвижность, ослабление мышечного тонуса, снижается масса тела, отмечается прогрессирующее исхудание. Помимо этого, у животных возникают сужение зрачков, частое мочеиспускание, разжижение фекалий. Чере; 6-7 мес у овец развиваются парезы мускулатуры конечностей и асимметрия тонуса шейных мышц, что ведет к искривлению шеи у овец и склонению головы у кротиков. Нередко отмечают тремор скелетных мышц и приступы клонико-тонических судорог. Смерть животных наступает при значительном исхудании и понижении температуры тела.
Па т о л огоанато м ичес к ие изменения. У животных при отравлении ФОС, резко выражены гемодинамические расстройства жизненно важных органов, застойные явления, периваскулярные отеки и диапедезные кровоизлияния в печени, почках, легких, сердечной мышце, в щитовидной и поджелудочной железах, дистрофические и некротические изменения в ганглиозных клетках головного мозга.
Диагностика отравления ФОС осуществляется на основании:
а) характерного комплекса нервно-паралитических клинических симптомов (миоз, слезотечение, слюнотечение, явления бронхоспазма, нарушение координации, угасание рефлексов, тремор и судороги скелетных мышц, диарея, парезы и параличи конечностей, асфиксия);
б) результатов патологоанатомического вскрытия павших животных;
в) химико-аналитического обнаружения остатков ФОС в содержимом желудочно-кишечного тракта, в жировой ткани, головном мозге, печени и почках, а также в кормах и воде с учетом анамнестических данных о применении ФОС в хозяйствах и условиях заболевания животных.
Лечение животных при отравлении ФОС основано на комплексном применении холинолитических препаратов в сочетании с реактиваторами холинэстеразы. К холинолитическим препаратам относятся атропина сульфат, тропацгна сульфат, фосфолитин (атропиноподобный препарат).
В качестве реактиваторов холинэстеразы известны дипироксим (ТМБ-4) , токсогонин и диэтиксим. Антидотный эффект атропина, тропацина и дипироксима основан на антидеполяризующем их действии на различные ФОС.
Наиболее широко испытаны на всех видах животных при экспериментальной интоксикации различными ФОС, атропин - холинолитик периферического действия,
тропацин - холинолитик центрального действия и
реактиватор холинэстеразы - дипироксим, путем внутримышечного введения в одном комплексном водном растворе.
В практических условиях можно заранее приготовить антидотную смесь указанных препаратов следующим образом. Вначале готовят 10 %-ный водный раствор тропацина и 20 %-ный водный раствор дипироксима, а затем по мере необходимости их смешивают в равных объемах. В смесь этих растворов добавляют атропина сульфат из расчета получения 1,5 %-ного раствора.
Антидтную смесь указанных препаратов применяют внутримышечно, согласно расчету в таблице 6, в следующих однократных дозах:
В практике готовят смесь:
10% раствор тропацина
20% раствор дипироксима
1,5% раствор атропина
в/м, однократно:
молодняк 1-2
молодняк 10
овцы, козы 4
молодняк 2
свиньи 5-10
молодняк 3
собаки 1,5
кролики - 1,0
Профилактика отравлений животных ФОС должна включать следующие мероприятия:
1.строгое соблюдение утвержденных санитарных правил и инструкций по технике безопасности при хранении, транспортировке и применению пестицидов в сельском хозяйстве;
2.скармливание зеленых кормов и растений не ранее 6 сут после обработки препаратами контактного действия и не ранее 45 дней после обработки препаратами системного действия;
3.содержание остаточных количеств ФОС в кормах (мг/кг) не должно превышать: для антио 2, бутифоса 3, дурсбана 0,2, карбофоса 2 для молочного скота и яйценоских птиц и 5 для откормочных животных; метафоса в кормах для молочного скота и яйценоской птицы не допускается, а для откормочных животных не должно превышать 0,5; метилмеркаптофоса 1; метилнитрофоса 1 для молочного скота и 2 для откормочных животных; фосфамяда 2; фталофоса 1 для молочного скота и 2 для откормочных животных; хлорофоса 1 для молочного скота и 3 для откормочного скота.
5.нельзя допускать промывание опрыскивающей аппаратуры! водоемах для водопоя животных, содержания водоплавающей птицы и разведения рыб.
Ветеринарно-санитарная экспертиза сырых животных продуктов.
Убой животных, в том числе птиц на мясо, может быть разрешен не ранее чем через 25 дней после перенесенного отравления фосфорорганическими пестицидами.
В случае вынужденного убоя животных при отравлении ФОС необходимо обязательно провести химико-аналитические исследования остаточных количеств ФОС и руководствоваться безопасными максимально допустимыми уровнями (МДУ) содержания пестицидов в пищевых продуктах, утвержденными Минздравом СССР 28 июля 1983 г.
Согласно указанному перечню МДУ пестицидов, допускается содержание абата (дифоса) в мясе и яйцах в количестве 1 мг/кг, амидофоса (руэлена) в мясе и мясных продуктах 0,3, байтекса 0,2, дурсбана 0,1, тролена 0,3 мг/кг; наличие ДДВФ и хлорофоса в этих продуктах не допускается.
Следует подчеркнуть, что остаточные количества фосфорорганических пестицидов в мясе при варке в течение 2-5,5 ч не разрушаются и оказывают токсическое действие на лабораторных животных при многократном скармливании.
В связи с этим мясо и мясопродукты, содержащие остаточные количества фосфорорганических пестицидов сверх допустимых нормативов, подлежат технической утилизации.
Поражение ФОС людей возможно при авариях на объектах по их производству, при применении в качестве ОВ или диверсионных агентов. ФОС – производные кислот пятивалентного фосфора.
Все ФОС при взаимодействии с водой подвергаются гидролизу с образованием нетоксичных продуктов. Скорость гидролиза ФОС, растворенных в воде, различна (например, зарин гидролизуется быстрее, чем зоман, а зоман – быстрее, чем V-газы).
ФОВ образуют зоны стойкого химическиого заражения.
Прибывающие из зоны заражения, пораженные ФОВ представляют реальную опасность для окружающих.
Токсикокинетика
Отравление происходит при вдыхании паров и аэрозолей, всасывании ядов в жидком и аэрозольном состоянии через кожу, слизистую глаз, с зараженной водой или пищей – через слизистую желудочно-кишечного тракта.
ФОВ не обладают раздражающим действием на месте аппликации (слизистые оболочки верхних дыхательных путей и желудочно-кишечного тракта, конъюнктива глаз, кожа) и проникают в организм практически незаметно. Мало токсичные ФОС способны к относитльно продолжительному персистированию (карбофос – сутки и более). Наиболее токсичные представители, как правило, быстро гидролизуются, окисляются. Период полуэлиминации зарина и зомана составляют около 5 минут, Vх несколько больше. Метаболизм ФОС происходит во всех органах и тканях.
Из организма выделяются только нетоксичные метаболиты веществ и потому выдыхаемый воздух, моча, кал не опасны для окружающих.
Основные проявления интоксикации
Симптомы интоксикации ФОС при ингаляционном поражении развиваются значительно быстрее, чем при поступлении через рот или кожу.
При ингаляции ФОВ смерть может наступить в течение 1-10 минут после воздействия.
В случае поступления ОВТВ с зараженной пищей, симптомы интоксикации развиваются в течение 0,5 часа. Резорбция с поверхности кожи действующей дозы высоко токсичных веществ происходит в течение 1 — 10 минут, однако скрытый период может продолжаться в течение 0,5 — 2 часов.
ФОС оказывают местное и резорбтивное действие. Подавляющее большинство развивающихся эффектов является следствием перевозбуждения мускарин- и никотинчувствительных холинэргических синапсов центральной нервной системы и периферии.
Местное действие проявляется функциональными изменениями органов на месте аппликации: возникновением миоза и гиперемии конъюнктивы при контакте яда со слизистой глаза; гиперемией слизистой оболочки носа и ринорреей – при проникновении ФОС ингаляционным путем; тошнотой, рвотой, спастическими болями в области живота – при попадании ядов внутрь; фибрилляцией подлежащих мышечных групп, пилоэрекцией и выделением капелек пота на зараженном участке кожи.
Однако все явления непродолжительны и в конечном итоге не определяют тяжести интоксикации.
Резорбтивное действие ФОС всегда сопровождается нарушениями со стороны ЦНС, жизненно важных органов и систем: дыхательной, сердечно-сосудистой, а также желудочно-кишечного тракта и др.
Продолжительность этих нарушений и степень их выраженности зависят от количества яда, попавшего в организм, и в известной степени, – от путей проникновения.
Интоксикации могут быть легкими, средней степени тяжести и тяжелыми.
При отравлении легкой степени обычно наблюдается возбуждение, бессонница, головные боли, галлюцинации, чувство страха, апатия, депрессия, легкий тремор.
Зрачки сужены (при поражении незащищенного человека ФОС в парообразной или аэрозольной форме). При этом нарушается зрение, особенно в темноте. Появляется головная боль, затруднение при дыхании, тошнота и другие диспептические явления. При отравлении средней степени тяжести возникают приступы удушья, напоминающие тяжелые приступы бронхиальной астмы. Поэтому такие формы отравления определяются как бронхоспастические.
Приступы, как правило, возобновляются через каждые 10-15 мин, но и в промежутках между ними дыхание остается затрудненным. Отмечается усиленная секреция бронхиальных, слюнных и потовых желез. Отчетливо выражено повышение артериального давления. Отравление нередко сопровождается рвотой, поносом и схваткообразными болями в области живота. Наблюдаются фибриллярные подергивания мышц, в особенности жевательных. Чаще сознание сохранено, но чувство страха, возбуждение, эмоциональная лабильность — нарушают критическое восприятие окружающей обстановки.
Зрачки резко сужены. Симптомы интоксикации отмечаются в течение 2-3 суток и более. При тяжелых поражениях развивается судорожный синдром. Если отравление не заканчивается летальным исходом от остановки дыхания впервые 10-30 минут, развивается кома. Кожа бледная, влажная, с резко выраженным акроцианозом. Наблюдается непрекращающаяся фибрилляция всех групп мышц, тремор. Дыхание дезорганизовано из-за периодически возникающих приступов удушья.
Также отмечаются гипотензия и брадикардия. Зрачки сужены (однако миоз может сменяться мидриазом), реакция зрачков на свет отсутствует. Изо рта и носа выделяется пенистая жидкость. Наблюдается непроизвольное мочеиспускание и дефекация, а в особо тяжелых случаях – развивается полная арефлексия. Смерть может наступить в течение ближайших часов или первых суток после начала отравления, от остановки дыхания, реже — сердечной деятельности.
При благоприятном исходе на протяжении длительного времени (1,5-2 месяца и более) у таких пораженных сохраняется общая слабость, астенизация, повышенная раздражительность, нарушение сна, устрашающие сновидения, головокружение, головная боль и другие невротические расстройства, составляющие астенический симптомокомплекс.
Нередко, особенно при поражении зоманом или длительно персистирующими в организме отравленного ФОС, в периоде выздоровления у пострадавших развиваются признаки нейропатий (нарушения кожной чувствительности, мышечная слабость, как правило, дистальных групп мышц). Кроме того, могут возникать пневмония, острая сердечно-сосудистая недостаточность (причина поздней гибели), нарушение функции желудочно-кишечного тракта (тошнота, расстройство стула, боли в эпигастральной области), печени и почек.
Механизм токсического действия
В основе гиперактивации холинэргических механизмов передачи нервного импульса в ЦНС и на периферии лежит:
Антихолинэстеразное действие ФОС (угнетение активности ацетилхолинэстеразы):
ФОС являются ингибиторами АХЭ, практически необратимо взаимодействующими с ее активным центром. В результате их действия угнетается процесс разрушения АХ в синапсах.
Медиатор накапливается в синаптической щели и вызывает стойкое перевозбуждение постсинаптических холинэргических рецепторов (непрямое холиномиметическое действие ФОС). Перевозбуждение холинорецепторов избытком ацетилхолина приводит к стойкой деполяризации постсинаптических мембран, иннервируемых клеток. Таким образом, отравление ФОС, по сути, — отравление эндогенным ацетилхолином, накапливающимся в крови и тканях, вследствие прекращения его разрушения ферментом ацетилхолинэстеразой.
Способность ФОС взаимодействовать с активным центром энзима объясняют структурным сходством молекул ядов с молекулой ацетилхолина.
Взаимодействие ФОС с активным центром ацетилхолинэстеразы приводит к образованию прочной ковалентной связи атома фосфора с гидроксильным радикалом серина, входящего в структуру эстеразного участка активного центра холинэстеразы, вызывая его фосфорилирование.
Взаимодействие ФОС и АХЭ проходит в две фазы и может быть представлено следующим образом:
Процесс превращения образовавшейся в первой фазе обратимо фосфорилированной холинэстеразы в необратимо связанную форму называется “старение” фосфорилхолинэстеразы.
Скорость “старения”, зависит от структуры ФОС, а именно от строения алкильных радикалов при атоме фосфора. Чем “тяжелее” радикалы, тем ниже скорость “спонтанной реактивации” и выше скорость “старения”. Поэтому АХЭ, ингибированная VX (R -OC2H5), стареет чрезвычайно медленно, зарином (R -OCН(СH3)2) — в течение нескольких часов, зоманом (R -OCНСН3С(СH3)3) — в считанные минуты.
В основе “старения” лежит процесс отщепления от атома фосфора, связанного с активным центром энзима, алкильных радикалов. При этом одновременно изменяется конформация белковой части энзима.
2. Холиносенсибилизирующее действие ФОС(непосредственное взаимодействие с холинорецепторами, сопровождающееся прямым холиномиметическим эффектом, повышением чувствительности холинорецепторов к ацетилхолину и холиномиметикам). Действие на холинорецепторы. Из возможных неантихолинэстеразных механизмов наиболее важным является действие ФОС на холинорецепторы.
Поскольку и холинорецепторы, и холинэстераза адаптированы к одному и тому же нейромедиатору, ингибиторы холинэстеразы могут проявить активность и по отношению к холинорецепторам.
По-видимому, блокада проведения нервно-мышечного сигнала, развивающаяся при смертельной интоксикации ФОС, связана не только со стойким деполяризующим действием избыточного количества ацетилхолина, но и с прямым действием ФОС на нервно-мышечные синапсы (по типу действия деполяризующих миорелаксантов).
Так, в эксперименте на изолированном нервно-мышечном препарате млекопитающего, при внесении в инкубационную среду достаточной дозы ФОС, наблюдается полное прекращение передачи нервного импульса с нервного волокна на мышцу.
Однако через некоторое время на фоне практически “тотального” угнетения активности холинэстеразы отмечается восстановление нервно-мышечной проводимости в синапсах.
Повторно блок можно вызвать, вновь добавив ФОС в инкубационную среду.
Сенсибилизирующее действие на холинорецептор зарина, ДФФ и других ФОС, проявляется, в частности, существенным повышении чувствительности отравленных экспериментальных животных к холиномиметикам, негидролизуемым ацетилхолинэстеразой (никотину, ареколину и т.д.). Установлено, что сенсибилизация к М-холиномиметикам (ареколину) сохраняется значительно дольше, чем к Н-холиномиметикам (никотину).
Причины различия, вероятно, обусловлены особенностями проведения нервных импульсов в М- и Н-холинэргических синапсах (см. выше).
Восстановление нормального проведения нервного импульса у лиц, перенесших интоксикацию ФОС, осуществляется за счет медленно протекающих процессов дэфосфорилирования АХЭ (“спонтанная реактивация”), синтеза АХЭ в перикарионе нервных клеток de novo и транспорта ее в нервные окончания, снижения содержания ацетилхолина в синаптической щели, десенситизации холинорецепторов (понижение чувствительности к ацетилхолину).
Нехолинэргические механизмы токсического действия. Помимо действия на холинореактивные структуры, ФОС, в высоких дозах, обладают прямым повреждающим действием на клетки различных органов и тканей (нервной системы, печени, почек, системы крови и т.д.), в основе которого лежат общие механизмы цитотоксичности: нарушение энергетического обмена клетки; нарушение гомеостаза внутриклеточного кальция; активация свободнорадикальных процессов в клетке; повреждение клеточных мембран.
Чем менее токсично ФОС, тем значимее роль указанных механизмов в развитии проявлений тяжелого поражения данным токсикантом. Существуют ФОС полностью лишенные антихолинэстеразной активности, токсичность которых обусловлена исключительно их цитотоксическим действием (три-о-крезилфосфат). Клиника отравления такими веществами полностью отличается от описанной выше.
В основе клиники лежат общие механизмы цитотоксичности:
— нарушение энергетического обмена клетки;
— нарушение гомеостаза внутриклеточного кальция;
— активация свободнорадикальных процессов в клетке;
— повреждение клеточных мембран.
Фосфорорганические соединения
Фосфорорганические соединения нашли применение как инсектициды (хлорофос, карбофос, фосдрин, лептофос и др.), лекарственные препараты (фосфакол, армин и т.д.), наиболее токсичные представители группы приняты на вооружение армий целого ряда стран в качестве боевых отравляющих веществ (зарин, зоман, табун, Vx).
Поражение ФОС людей возможно при авариях на объектах по их производству, при применении в качестве ОВ или диверсионных агентов.
Впервые ФОС были синтезированы Тенаром в 1846 г.
В нашей стране основоположником химии ФОС был А.Е. Арбузов, предложивший в 1905 г. новый метод их синтеза. На токсические свойства этих соединений внимание было обращено только в 1932 г., когда Ланге и Крюгер впервые описали симптомы отравления диметил- и диэтилфторфосфатом, синтезированных в процессе поиска новых инсектицидов. Бесспорная практическая значимость таких средств явилась причиной масштабных исследований, направленных на всестороннее изучение нового класса биологически активных веществ.
Так, за короткий промежуток времени только в Германии, в лаборатории Шрадера, с целью изыскания все новых средств борьбы с вредными насекомыми было синтезировано и изучено более 2000 ФОС, среди которых многие обладали высокой токсичностью и для млекопитающих. Это послужило поводом для создания на их основе новых образцов химического оружия. К началу второй мировой войны химиками Германии были синтезированы такие высокотоксичные отравляющие вещества, как табун, зарин, несколько позже – зоман.
Одновременно были определены перспективы изыскания еще более токсичных для человека соединений, что на практике было реализовано Таммелином (1955), синтезировавшим метилфторфосфорилхолин, явившийся прообразом новой группы ФОВ, обозначаемых как V-газы (Vх).
В 70 — 80х годах 20 столетия была разработана технология применение ФОВ в так называемых бинарных боеприпасах. При этом два относительно мало ядовитые химические соединения хранятся, транспортируются и размещаются в боеприпасах раздельно.
Компоненты смешиваются лишь после выстрела и образуют на пути к цели, в ходе химической реакции, высокоядовитое ОВ. Чрезвычайно высокая токсичность и особенности физико-химических свойств, позволяющие быстро создавать обширные очаги химического заражения, до недавнего времени делали ФОВ (зарин, зоман, V-газы) наиболее опасными из всех известных ОВ. В соответствии с международными договоренностями, запасы ФОВ в большинстве стран мира подлежат уничтожению.
В настоящее время исследования в области создания все новых биологически активных веществ на основе ФОС продолжаются.
Сейчас это, как и в начале 30х годов 20 века, в основном, поиск инсектицидов, которых на сегодняшний день известны сотни наименований.
Физико-химические свойства.
Симптомы и первая помощь при отравлении ФОС
Токсичность
ФОС – производные кислот пятивалентного фосфора. Все токсичные соединения фосфорной (1), алкилфосфоновой (2) и диалкилфосфиновой (3) кислот имеют структуру:

Фосфор с помощью двойной связи соединен с атомом кислорода или серы; двумя связями — с алкил-, алкокси- арил-, моно- или диалкиламиногруппами и т.д.
(R1, R2); пятая (Х) — насыщена группой, относительно легко отщепляющейся от атома фосфора (F-, CN-, -ОR, -SR и т.д.).
За счет высвобождающейся при этом валентности, ФОС и взаимодействует с активными центрами ряда энзимов.
Структурные формулы некоторых ФОС представлены на рисунке 46.

Рисунок 46.
Структура некоторых фосфорорганических соединений
Биологическая активность ФОС, в том числе и токсичность, зависит от их строения (табл.
Таблица 43.
Токсичность (ЛД50) некоторых ФОС для белых мышей
| Название вещества | Способ введения | Токсичность, мг/кг |
| О,О-Диметил-S-(1,2-дикарбоэтоксиэтил)дитиофосфат (карбафос, малатион) | через рот | 400 — 930 |
| О,О-Диметил-О-(2,2-дихлорвинил)фосфат (ДДВФ, дихлорофос) | через рот | 75 — 175 |
| Диэтил-(4-нитрофенил)-тиофосфат (паратион) | через рот внутрибрюшинно | 25,0 5,5 |
| Диэтил-(4-нитрофенил)-фосфат (фосфакол, параоксон) | подкожно | 0,8 |
| Диизопропилфторфосфат (ДФФ) | через рот подкожно внутривенно | 36,8 0,4 |
| N,N-диметиламидо-О-этилцианфосфат (табун) | подкожно внутрибрюшинно внутривенно | 0,6 0,6 0,15 |
| О-изопропилметилфторфосфонат (зарин) | подкожно внутрибрюшинно | 0,2 0,2 |
| О-диметилизобутилметилфторфосфонат (зоман) | подкожно | 0,06 |
| О,О-диэтоксифосфорилтиохолин | подкожно внутрибрюшинно | 0,26 0,14 |
| Метилфторфосфорилгомохолин | внутрибрюшинно внутривенно | 0,05 0,006 |
Все ФОС обладают высокой реакционной способностью.
Особое значение придают реакциям фосфорилирования, гидролиза и окисления, поскольку именно эти реакции определяют стойкость токсикантов в окружающей среде, имеют отношение к метаболизму и механизму токсического действия ядов в организме, на них основаны некоторые принципы дегазации, обнаружения, антидотной профилактики и терапии интоксикаций.
ФОС легко отдают электроны, активно вступают в реакции с электрофильными группами других соединений и за счет этого фосфорилируют многие вещества (аминокислоты, полифенолы, гидроксиламин, гидроксамовые кислоты и др.).
В качестве примера приводим реакцию фосфорилирования зарином гидроксиламина:

Все ФОС при взаимодействии с водой подвергаются гидролизу с образованием нетоксичных продуктов.
Скорость гидролиза ФОС, растворенных в воде, различна (например, зарин гидролизуется быстрее, чем зоман, а зоман – быстрее, чем V-газы).
В общей форме реакция гидролиза может быть представлена следующим образом:

Реакция гидролиза ФОС с разрывом ангидридной связи происходит и в организме, как спонтанно, так и при участии энзимов.
В результате реакции окисления, ФОС также разрушаются, однако в ряде случаев (при окислении фосфотионатов до фосфатов) некоторые вещества даже повышают свою активность.
Это иллюстрируется примером

Токсичность параоксона для млекопитающих и человека выше, чем паратиона.
Важнейшие свойства фосфорорганических отравляющих веществ представлены в таблицах 44-46.
Таблица 44.
Основные свойства зарина
| Зарин | GВ |
| Химическое название | изопропил метилфосфонофторид |
| Агрегатное состояние | бесцветная жидкость, пары бесцветны |
| Молекулярный вес | 140,10 |
| Плотность пара (по воздуху) | 4,86 |
| Плотность жидкости | 1,089 |
| Точка кипения | 1580С |
| 11300 (при 200С) | |
| Температура разрушения | полное разрушение в течение 2,5 часов при 1500 |
| Растворимость в воде (%) | |
| Скорость гидролиза | зависит от рН.
Период полураспада при рН 1,8: 7,5 часов; в незабуференной среде — 30 часов; быстрый гидролиз в щелочной среде. |
| Продукт гидролиза | в кислой среде НF; в щелочной среде изопропиловый спирт и полимеры |
| Растворимость в липидах | хорошая |
| Стабильность при хранении | стабилен в стальных контейнерах при 650.
Чем чище вещество, тем стабильнее |
| Действие на металлы | легкое коррозийное |
| Запах | Отсутствует |
| 100 мг.мин/м3- в состоянии покоя; 35 мг.мин/м3 — при физической нагрузке | |
| Средненепереносимая токсодоза (ингаляционно) | 75 мг.мин/м3 — в покое; 35 мг.мин/м3 — при физической нагрузке |
| Скорость детоксикации | быстро детоксицируется; |
| Кожные эффекты (жидкость) среднесмертельная доза | 1,7 г/человека.
Жидкость не повреждающая кожу, но легко пенетрирующая во внутренние среды. Необходима немедленная деконтаминация кожных покровов. Пары также проникают через неповрежденную кожу. |
| Среднесмертельная токсодоза (пара через кожу, при защищенных органах дыхания) | 12000 мг.мин/м3 для обнаженного человека, 15000 мг.мин/м3, для человека, находящегося в обычном обмундировании |
| Средненепереносимая токсодоза (пара через кожу) | 8000 мг.мин/м3 для человека в обычном обмундировании |
| Стойкость | Зависит от средств доставки и погодных условий (в среднем — до 5 суток) |
Таблица 45.
Основные свойства зомана
| Зоман | GD |
| Химическое название | пинаколиловый эфир метилфторфосфоновой кислоты |
| Агрегатное состояние | бесцветная жидкость; бесцветный пар |
| Молекулярный вес | 182,2 |
| Плотность пара (по воздуху) | 6,33 |
| Концентрация пара в воздухе (мг/м3) | 3000 (при 200С) |
| Плотность жидкости | 1,02 |
| Температура кипения | 1980 |
| Температура разрушения | нестабилизированное вещество разрушается при 1300 в течение 4 часов, стабилизированное — 200 часов |
| Растворимость в воде (%) | 1,5 |
| Скорость гидролиза | зависит от рН; в присутствии NaOH(5%) полное разрушение в течение 5 минут; период полуразрушения при рН 6,65 и 250 — 45 часов |
| Продукт гидролиза | НF |
| Растворимость в липидах | Высокая |
| Стабильность при хранении | менее стабилен, чем GB |
| Запах | фруктовый; при наличии примеси — камфорный |
| Среднесмертельная токсодоза (ингаляционно) | 70-100 мг.мин/м3 |
| Кожные эффекты | чрезвычайно токсичен при действии через кожу.
Кожу не повреждает, но быстро абсорбируется. |
| Средненепереносимая доза через кожу (жидкая форма) | 0,35 г/человека |
| Необходимость защиты | противогаз, защита кожных покровов. Обычное обмундирование задерживает пары в течение 30 минут после контакта. Перед снятием противогаза необходимо удалять обмундирование, зараженное капельно-жидким ОВ |
| Стойкость | зависит от способа применения и погодных условий.
Крупные проливы персистируют на местности в течение 1-2 недель при обычной погоде |
Таблица 46.
Не нашли то, что искали?
Воспользуйтесь поиском гугл на сайте:
ФОСФОРОРГАНЙЧЕСКИЕ СОЕДИНЕНИЯ - органические соединения, содержащие в своем составе фосфор, связанный с молекулой органического соединения либо фос-фор-углеродной связью, либо через гетероатом - кислород, азот, серу. Ф. с., являющиеся неполными эфирами фосфорных кислот (см.), играют чрезвычайно важную биол. роль; к таким соединениям принадлежат нуклеиновые кислоты (см.), фосфолипиды (см.
Фосфатиды), фосфопротеиды (см.) и др. Некоторые Ф. с. применяют в качестве лекарственных средств. Особый интерес представляют синтетические физиологически активные соединения, являющиеся полными эфирами или амидами фосфорных к-т, с общей формулой RiR2P (О или S)X, где Ri и R2 - алкильные или алкокс ильные радикалы, замещенные амиды, X - кислотная группа (фтор, нитрофенолы, меркаптаны, ангидридные группы).
Биол. активность Ф. с. этой группы связана с тем, что они выступают в качестве ингибиторов (см.) холинэстераз (см. Антихолинэстеразные средства). В основе классификации и общепринятой номенклатуры таких Ф. с. лежат фосфорные к-ты, производными к-рых они являются. Так, хим. название армина (см.), производного этил-фосфоновой к-ты, - О-этил-О-м-нит-рофеяилэтилфосфояат.
Характеристики отдельных представителей Ф. с. смотри в статьях Антихолинэстеразные средства, Ар-мин, Нибуфин, Нервно-паралитические отравляющие вещества, Пи-рофос, Фосфакол, Хлорофос.
Механизм в з а и м о д е fi-ст в и я ф о с ф о р о р г а н и ч е-с к и х соединений с холин-э с т e р а з а м и.
Эстеразный центр активной поверхности холинэстераз (см.) включает по крайней мере две функционально важные группировки - имидазол остатка гистидина (см.) и гидроксильную группу остатка серина (см.). При сорбции Ф. с. на каталитической поверхности холинэстеразы (ХЭ) между фос-форильным кислородом Ф.
Отравление фосфорорганическими соединениями
с., ими-дазолом гистидина и гидроксильной группой серина через систему водородных связей образуется циклический фермент-ингибиторный комплекс, аналогичный по структуре фермент-субстратному комплексу Михаэлиса (см. Ферменты). Перераспределение электронов приводит к отщеплению кислотной группы Н X и образованию фосфорилирован-ной по гидроксильной группе серина ХЭ, причем такое промежуточное соединение в отличие от ацилирован-ной ХЭ (при ее реакции с субстратом) практически неспособно к гидролитическому отщеплению фосфо-рильной группы и восстановлению активности фермента (см.
Фосфорилирование). Это определяет необратимый характер угнетения ХЭ под действием Ф. с., однако гидролиз фосфорилированной ХЭ может произойти под действием нуклеофильных реагентов - реактиваторов. Количественной мерой анти-ферментного действия Ф. с. служит бимолекулярная константа скорости реакции ки (М-1* сек»1- или М»1* мин-1). Ранее такой мерой служила величина концентрации Ф. с., вызывающая угнетение ХЭ на 50% (I50, М).
При развитии острой интоксикации Ф. с. ведущую роль играет их антихолинэстеразный эффект. Предполагают, что определенное значение имеет неантихолинэстеразное действие Ф. с. непосредственно на холинорецептор.
Метаболизм фосфорор-г а н и ч е с к и х соединений.
По гипотезе В. И. Розенгарта, все метаболические превращения Ф. с. приводят к образованию более полярных продуктов, что облегчает их выведение из организма, и в основном протекают под действием определенных групп ферментов, относящихся к классам гидролаз (см.), трансфераз (см.), оксидоредуктаз (см.). В организме Ф. с. подвергаются и неферментативным превращениям, напр, отщеплению молекулы соляной к-ты в процессе метаболизма хлорофоса, тионтиольной изомеризации.
Метаболические превращения Ф. с. в организме могут приводить как к инактивации (детоксикации) фосфорорганических соединений, так и к их активации.
Практическое применение фосфорорган и чески х соединений. Основное практическое использование Ф. с. в качестве акарицидов (см.) и инсектицидов (см.) связано гл. обр. с их высокой биол. эффективностью и с быстрой детоксикацией (по сравнению, напр., с хлорорганическими соединениями). К серьезным недостаткам Ф. с. относится их определенная токсичность в отношении человека и домашних животных и легко возникающая резистентность к ним у членистоногих (см. Гербициды, Дезинсицирующие средства, Ларвициды, Пестициды).
Чрезвычайно важную роль сыграли Ф. с. в исследованиях свойств ХЭ, полученных из различных источников. С помощью большой группы специально синтезированных Ф. с., имеющих неполярные углеводородные радикалы, на каталитической поверхности молекул ХЭ были обнаружены гидрофобные участки, имеющие большое значение в проявлении этими ферментами субстратной специфичности.
Ф. с. в качестве лекарственных средств применяют при лечении глаукомы, для предупреждения и лечения послеоперационной атонии желудка и кишечника, а также при травмах и воспалительных заболеваниях органов жел.-киш. тракта (см. Антихолинэстеразные средства, Армин, Нибуфин).
Библиогр.: О’Брайн Р. Токсические эфиры кислот фосфора, пер. с англ., М., 1964, библиогр.; Розен гарт В. И. и Шерстобитов О. Е. Избирательная токсичность фосфорорганических инсектоакарицидов, Л., 1978; Сады-
С. и др. Холинэстеразы, Активный центр и механизм действия, Ташкент, 1976; Химия и применение фосфор^ органических соединений, Труды Первой конференции, под ред. А. Е. Арбузова, М., 1957; Е to М. Organophosphorus
pesticides, Organic and biological chemistry, Clevelend, 1976, bibliogr. E. В. Розенгарт.
1 2 3 4 5 6 7 8 9 … 26
М-, Н-холиномиметики
Разберем группу средств, относящихся к М-, Н-холиномиметикам. К средствам, прямо стимулирующим М- и Н-холинорецепторы (М-, Н-холиномиметикам) относятся ацетилхолин и его аналоги (карбахолин). Ацетилхолин, является медиатором в холинергических синапсах, представляет собой сложный эфир холина и уксусной кислоты и относится к моночетвертичным аммониевым соединениям.
В качестве лекарственного средства его практически не применяют, так как он действует резко, быстро, практически молниеносно, очень кратковременно (минуты).
При приеме внутрь неэффективен, так как гидролизуется. В виде хлорида ацетилхолин используют в экспериментальной физиологии и фармакологии.
Ацетилхолин оказывает прямое стимулирующее влияние на М- и Н- холинорецепторы. При системном действии ацетилхолина (в/в введение недопустимо, так как резко понижается АД) преобладают М-холиномиметические эффекты: брадикардия, расширение сосудов, повышение тонуса и сократительной активности мышц бронхов, ЖКТ.
Перечисленные эффекты аналогичны тому, что наблюдаются при раздражении соответствующих холинергических (парасимпатических) нервов. Стимулирующее влияние ацетилхолина на Н-холинорецепторы вегетативных ганглиев также имеет место, но оно маскируется М-холиномиметическим действием. Ацетилхлин вызывает стимулирующий эффект и на Н-холинорецепторы скелетных мышц.
В связи со сказанным, в дальнейшем основное внимание уделим антихолинэстеразным средствам.
Антихолинэстеразные средства (АХЭ)
Антихолинэстеразные средства (АХЭ) — это лекарственные средства, оказывающие свое действие путем ингибирования, блокирования ацетилхолинэстеразы.
Ингибирование фермента сопровождается накоплением медиатора ацетилхолина в области синапса, т. е. в области холинореактивных рецепторов. Под влиянием антихолинэстеразных средств замедляется скорость разрушения ацетилхолина, который и проявляет более длительное действие на М- и Н-холинорецепторы. Таким образом, эти препараты действуют аналогично М, Н-холиномиметикам, но эффект антихолинэстеразных средств опосредован через эндогенный (собственный) ацетилхолин.
В этом заключается основной механзим действия антихолинэстеразных средств. Следует добавить, что данные средства обладают также некоторым и прямым возбуждающим действием на М, Н-холинорецепторы.
Исходя из стойкости взаимодействия антихолинэстеразных препаратов с ацетилхолнэстеразой, их подразделяют на 2 группы:
- АХЭ средства обратимого действия. Их действие длится 2-10 часов. К ним относятся: физостигмин, прозерин, галантамин и другие.
- АХЭ средства необратимого типа действия.
Эти средства очень мощно связываются с ацетилхолинэстеразой на много дней, даже месяцев. Однако постепенно, примерно через 2 недели активность энзима может восстанавливаться.
К данным средствам относятся: армин, фосфакол и другие антихолинэстеразные средства из группы фосфорорганических соединений (инсектициды, фунгициды, гербициды, БОВ).
Эталонным средством группы обратимо действующих АХЭ средств является ФИЗОСТИГМИН(3-4 часа) (его длительное время использовали как оружие и как средство правосудия, так как согласно поверию, от яда погибает лишь истинно виновный человека), являющийся природным алкалоидом из калабарских бобов, т.е.
высушенных зрелых семян западно-африканского вьющегося дерева Physotigma venenosum. В нашей стране чаще используется ПРОЗЕРИН (таблетки по 0,015; ампулы по 1 мл 0,05%, в глазной практике — 0,5%; Proserinum), являющийся, как и другие средства этой группы (галантамин, оксазил, эдрофоний и др.), синтетическим соединением. Прозерин по химическому строению представляет собой упрощенный аналог физостигмина, содержащий четвертичную аммониевую группу. Это отличает его от физостигмина.
В связи с однонаправленностью действия всех перечисленных препаратов у них будут практически общие эффекты.
Значительный практический интерес представляет влияние АХЭ средств как природных, так и синтетических на некоторые функции:
- глаза;
- тонус и моторику ЖКТ;
- нервно-мышечную передачу;
- мочевого пузыря;
Прежде всего, разберем эффекты прозерина, связанные с его воздействием на М-холинорецепторы.
Антихолинэстразные средства, в частности прозерин, влияют на глаз следующим образом:
- вызывают сужение зрачка (миоз — от греческого — myosis — закрывание), что связано с опосредованным возбуждением М-холинорецепторов круговой мышцы радужки (m.sphincter puрillae) и сокращением этой мышцы;
- снижают внутриглазное давление, что является результатом миоза. Радужка при этом становится тоньше, в большей степени раскрываются углы передней камеры глаза и в связи с этим улучшается отток (реабсорбция) внутриглазной жидкости через Фонтановы пространства и Шлеммов канал.
- прозерин, как все АХЭ, вызывает спазм аккомодации (приспособления).
В этом случае, средства опосредованно стимулируют М -холинорецепторы ресничной мышцы (m.ciliaris), имеющей только холинергическую иннервацию. Сокращение указанной мышцы расслабляет Циннову связку и, соответственно, увеличивает кривизну хрусталика. Хрусталик становится более выпуклым, а глаз устанавливается на ближнюю точку видения (вдаль плохо видит).
Исходя из сказанного, становится понятным, почему прозерин иногда используется в офтальмологической практике. В этом плане прозерин показан при открытоугольной форме глаукомы (0,5% р-р 1-2 капли 1- 4 раза в день)-для купирования приступа.
Прозерин оказывает стимулирующее влияние на тонус и двигательную активность (перистальтику) ЖКТ, за счет чего улучшается продвижение содержимого, усиливает тонус бронхов (вызывает бронхоспазм), а также тонус и сократительную активность мочеточников.
Одним словом, АХЭ, в частности прозерин, усиливают тонус всех гладкомышечных органов. Кроме того, прозерин усиливает секреторную активность желез внешней секреции (слюнных, бронхиальных, кишечника, потовых) за счет ацетилхолина.
СЕРДЕЧНО-СОСУДИСТАЯ СИСТЕМА.
Прозерин обычно снижает частоту сокращений сердца и обладает тенденцией к снижению АД.
Использование прозерина в клинической практике связано с перечисленными его фармакологическими эффектами. Благодаря тонизирующему его влиянию на тонус и сократительную активность кишечника и мочевого пузыря препарат используется для устранения послеоперационных атонии кишечника и мочевого пузыря. На значают в виде таблеток или инъекции под кожу.
ЭФФЕКТЫ ПРОЗЕРИНА (АХЭ) ПРИ ДЕЙСТВИИ НА Н-ХОЛИНОРЕЦЕПТОРЫ (НИКОТИНОПОДОБНЫЕ ЭФФЕКТЫ).
Никотиноподобные эффекты прозерина проявляются в облегчении:
- нервно-мышечной передачи
- передачи возбуждения в вегетативных ганглиях.
В результате этого прозерин вызывает значительные повышение силы сокращения скелетных мышц, а благодаря этому показан к применению у больных с миастенией. Miasthenia gravis — нервно мышечное заболевание с двумя характерными, протекающими параллельно процессами:
а) поражение мышечной ткани по типу полимиозита (аутоиммунные нарушения);
б) поражение синаптической проводимости, синаптический блок (синтез Ацетилхолина меньше, затруднение его освобождения, недостаточная чувствительность рецепторов).
Клиника: мышечная слабость и резкая утомляемость. Кроме того, препарат используется в неврологической практике при параличах, парезах, возникающих после механических травм, после перенесенного полиомиелита (остаточные явления), энцефалита, неврита зрительного нерва, при невритах. В связи с тем, что прозерин облегчает передачу возбуждения в вегетативных ганглиях, он показан при отравлениях ганглиоблокаторами. Кроме того, прозерин эффективен при передозировке миорелаксантов (мышечная слабость, угнетение дыхания) антидеполяризующего действия (в/в до 10-12 мл 0,05% р-ра) например d-тубокурарином.
Иногда прозерин назначают при слабости родовой деятельности (раньше чаще, сейчас очень редко). Как видно, у препарата широкий спектр деятельности, в связи с этим есть и побочные реакции.
Побочные эффекты: эффект однократно введенной дозы прозерина проявляется через 10 минут и продолжается до 3-4 часов.
При передозировке или повышенной чувствительности могут быть такие нежелательные реакции как усиление тонуса кишечника (вплоть до поноса), брадикардия, бронхоспазм (особенно у лиц, склонных к этому).
Выбор препаратов АХЭ средств определяется их активностью, способностью проникать через тканевые барьеры, длительностью действия, наличием раздражающих свойств, токсичностью. При глаукоме используют прозерин, физостигмин, фосфакол.
Следует подчеркнуть, что галантамин с этой целью не используют, так как он оказывает раздражающее действие и вызывает отек коньюнктивы.
ГАЛАНТАМИН — алкалоид подснежника кавказкого — имеет практически те же показания к применению, что и прозерин. В связи с тем, что он лучше проникает через ГЭБ (третичный амин, а не четвертичный, как прозерин), он более показан при лечении остаточных явлений после полиомиелита.Действует 6-8 часов.
Для резорбтивного действия назначают (т.
е. действия после всасывания) ПИРИДОСТИГМИН и ОКСАЗИЛ, влияниеие которых более продолжительно, чем прозерина. Противопоказания: эпилепсия, гиперкинезн, бронхиальная астма, стенокардия, атеросклероз, у больных с нарушением глотания и дыхания.
ВТОРАЯ ГРУППА АХЭ СРЕДСТВ — АХЭ средства «необратимого» типа действия. Здесь, по-существу, одно лекарство, фосфорорганическое соединение — органический эфир фосфорной кислоты — ФОСФАКОЛ.
Phosphacolum — флаконы по 10 мл 0,013% и 0,02% растворов. Высочайшая токсичность свойственна препарату, поэтому используется только местно в отфальмологической практике. Отсюда и показания к применению:
- острая и хроническая глаукома;
- при прободении роговицы; выпадении хрусталика (искусственный хрусталик, нужен длительный миоз).
Фармакологические эффекты те же, что и у прозерина в отношении глаза. Следует сказать, что в офтальмологии растворы прозерина и фосфакола в настоящее время используются редко.
Второй препарат — армин (Arminum) – эфир этилфосфоновой кислоты, ФОС входит в группу сильнодействующих, длительно действующих препаратов. Обладает высокой токсичностью (гиперактивация центральных и периферических холинергических систем).
В малых концентрациях используется как местный миотический и противоглаукоматозный препарат. Выпускается в виде глазных капель (0,01% раствора по 1- 2 капли- 2-3 раза в день).
Значительный интерес представляют для врача другие ФОС, такие как инсектициды, фунгициды, гербициды, так как существенно увеличилось число отравлений данными веществами.
Фармакологические эффекты органических соединений фосфора обусловлены накоплением эндогенного (общего) ацетилхолина в тканях вследствие стойкого ингибирования ацетилхолинэстеразы. Острые отравления ФОС требуют безотлагательной помощи.
ПРИЗНАКИ ОТРАВЛЕНИЯ ФОС И АХЭ ВЕЩЕСТВАМИ ВООБЩЕ.
Отравления ФОС имеют очень характерную клиническую картину.
Отравление фосфорорганическими соединениями: симптомы, антидоты и неотложная помощь
Состояние больного обычно тяжелое. Отмечаются эффекты мускаринового и никотинового типа. Прежде всего у больного обнаруживается:
- спазм зрачка (миоз);
- сильнейший спазм ЖКТ (тенезмы, боли в животе, диарея, рвота, тошнота);
- тяжелый спазм бронхов, удушье;
- гиперсекреция всех желез (слюнотечение, отек легких — булькание, хрипы, чувство стеснения за грудиной, одышка);
- кожа мокрая, холодная, липкая.
Все перечисленные эффекты связаны с возбуждением М-холинорецепторов (мускариновые эффекты) и соответствуют клинике при отравлении грибами (мухоморами), содержащими мускарин.
Никотиновые эффекты проявляются судорогами, подергиваниями мышечных волокон, сокращениями отдельных групп мышц, общей слабостью и параличом вследствии деполяризации.
Со стороны сердца может отмечаться как тахикардия, так и (чаще) брадикардия.
Центральные эффекты отравлений ФОС реализуются головокружением, возбуждением, спутанностью сознания, гипотензией, угнетением дыхания, комой. Смерть обычно наступает вследствие недостаточности дыхательной функции.
Что делать? Какие меры и в какой последовательности проводить? В соответствии с рекомендациями ВОЗ, «лечение должно быть начато незамедлительно». При этом меры помощи должны быть полными и всесторонними.
Прежде всего, следует удалить ФОС с места введения.
С кожных покровов и слизистых ФОС следует смыть 3-5% раствором НАТРИЯ ГИДРОКАРБОНАТА или просто водою с мылом. При интоксикации вследствие попадания веществ внутрь, необходимо промывание желудка, назначение адсорбирующих и слабительных средств, используют высокие сифонные клизмы. Эти мероприятия проводят многократно. Если ФОС попало в кровь, ускоряют его выведение с мочой (форсированный диурез).
Эффективно применение ГЕМОСОРБЦИИ, гемодиализа и перитонеального диализа.
Важнейшим компонентом лечения острых отравлений ФОС является медикаментозная терапия. Если при отравлении ФОС наблюдается перевозбуждение М-холинорецепторов, то логично использование антагонистов — М-холиноблокаторов.
Прежде всего, следует в/ в ввести АТРОПИН в больших дозах (10-20-30 мл суммарно). Дозы атропина увеличивают в зависимости от степени интоксикации. Следят за проходимостью дыхательных путей и, если необходимо, проводят интубацию и искусственное дыхание.
Руководством к дополнительному введению атропина являются состояние дыхания, судорожная реакция, АД, частота пульса, саливация (слюнотечение). Описано в литературе введение атропина в дозе нескольких сот миллиграммов в сутки.
При этом частота пульса не должна превышать 120 ударов в 1 минуту.Вводят до появления сухости во рту и расширения зрачка.
Кроме того, при отравлениях ФОС необходимо применение специфических противоядий — реактиваторов ацетилхолинэстеразы.
К последним относят ряд соединений, содержащих в молекуле ОКСИМНУЮ группу (-NOH): дипироксим — четвертичный амин, а также изонитрозин — третичный амин; (aмпp., 15% — 1 мл). Реакция идет по схеме: АХЭ — Р = NOH. Дипироксим взаимодействует с остатками ФОС, связанными с ацетилхолинэстеразой, высвобождая фермент. Атом фосфора в АХЭ соеднинениях прочно связан, но связь Р = NOH, т. е. фосфора с оксимной группой, еще более прочная. Таким путем фермент высвобождается и восстанавливает свою физиологическую активность.
Но действие реактиваторов холинэстеразы развивается недостаточно быстро, поэтому наиболее целесообразно применение реактиваторов АХЭ вкупе с М-холиноблокаторами. Дипироксин назначают парентерально (по 1-3 мл п/к и только в особо тяжелых случаях в/в).
1 2 3 4 5 6 7 8 9 …
Фосфорорганические отравляющие вещества (ФОВ)
В арсенале химического оружия капиталистических стран имеются яды, относящиеся к наиболее токсичным веществам из известных человечеству. Это отравляющие вещества (ОВ) из группы фосфорорганических соединений. Кроме них, следует назвать ОВ кожно-нарывного действия, ОВ общеядовитого действия, ОВ удушающего действия, раздражающие и слезоточивые ОВ, а также психотомиметики.
Последние три группы ядов не относятся к веществам смертельного действия, однако способны в очень низких концентрациях и дозах вызывать выраженные нарушения со стороны целого ряда физиологических систем и органов, что полностью выводит человека из строя.
Все высокотоксичные фосфорорганические вещества являются производными кислот пятивалентного фосфора.
Наиболее известные яды этого типа - ДФФ (диизо-пропилфторфосфат), табун, зарин, зоман, Y-газы.
Типичным представителем Y-газов (фосфорорганические вещества типа Y) является вещество Yx (Lohs, 1975).
Указанные яды представляют собой жидкости. Они хорошо растворимы в органических растворителях и легко впитываются в окрашенные и пористые поверхности, а также в резинотехнические изделия.
Зарин достаточно летуч: при 20° С его максимальная концентрация паров в воздухе составляет 12 мг/л.
Зоман менее летуч: максимальная концентрация его паров при 20° С составляет 3 мг/л. Плотность паров зарина и зомана по воздуху соответственно равны 4,8 и 6,3. Вещества типа Y малолетучи.
ФОВ могут поражать незащищенного человека при любом способе контакта с ним. Они легко проникают в организм через легкие, слизистые оболочки глаз и органов пищеварения а также через кожные покровы.
«Неотложная помощь при острых отравлениях», С.Н.Голиков
Эту группу ядов подразделяют на ОВ, избирательно поражающие верхние дыхательные пути (стерниты) - дифенилхлорарсин, дифенилцианарсин, адамсит.
Слезоточивые ОВ (лакриматоры) - хлорацетофенон, бромбензилцианид, хлорпикрин (в низких концентрациях). ОВ смешанного действия - вещество CS.
Ниже приводится краткая характеристика этих соединений. Дифенилхлорарсин - кристаллическое вещество, температура кипения 333° С, температура плавления 38-40° С. Максимальная концентрация при температуре 20°С…
Вещества психогенного действия, галлюциногены. К психотомиметикам относят вещества, способные в сравнительно малых дозах расстраивать психическую деятельность человека. По своей химической природе психотомиметики принадлежат в основном к следующим группам: производные индола: производные лизергиновой кислоты - диэти- ламид, этиламид, морфолид; производные триптамина - N, N-диметилтриптамин, буфотенин, псилоцин и псилоцибии; разные - гармин, гармалин, ибогамин и др.
производные…
По токсичности ФОВ превосходят почти все известные яды, за исключением ботулотоксина и немногих токсинов природного происхождения.
Токсичность нарастает в ряду соединений ДФФ, табун, зарин, зоман, вещество Yx во много раз. Смертельная доза зарина для человека при внутримышечном введении 0,03 мг/кг. Капля зарина массой 3 мг при попадании в глаз представляет смертельную опасность.
Отравление ФОС
Концентрация зарина в…
Психотомиметики могут использоваться как ОВ на поле боя, так и в качестве диверсионных ядов (Franke, 1973). Они могут проникать в организм человека ингаляционным путем или же эптерально с зараженной пищей и водой. По механизму токсического действия производные лизергиновой кислоты отличаются от производных бензиловой и гликолевой кислот (антихолинергических веществ). У последних в основе психогенного действия лежит…
Острая интоксикация ФОВ проявляется разнообразными симптомами, которые в зависимости от их происхождения удобно делить на три группы: симптомы возбуждения мускариночувствительных холинореактивных систем, симптомы возбуждения никотиночувствительных холинореактивных систем, симптомы поражения центральной нервной системы.
К первой группе относятся следующие симптомы: слезотечение, слюнотечение, рино- и бронхорея, повышенное потоотделение, миоз, бронхоспазм и ларингоспазм, спастические сокращения кишечника, брадикардия, гипотония, тошнота,…