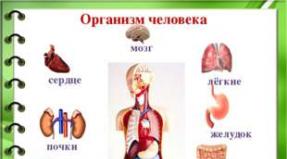
Методы получения изолированных колоний аэробов. Принципы и методы выделения чистых культур. Ферменты бактерий, их идентификация. Внутривидовая идентификация (эпидемиологическое маркирование). Выделение чистой культуры по способу Дригальского
«Получение аммиака» - Обеспечить оптимальное протекание химических реакций. Создании альтернативного способа производства аммиака. Создать производство, основанное на современных принципах. При увеличении температуры равновесие смещается в сторону эндотермической реакции. Химизм. Аппарат для получения аммиака. Принципиальная схема производства.
«Метод проектов» - Давать определение понятиям. Видеть проблемы. Осуществление деятельности. На долю учителя остается трудная задача выбора проблем для проектов. Метод учебных проектов. Оформление проектной папки. Классифицировать. «От идеи до реализации». Задавать вопросы. Распределяют роли в группе. Скажи мне - и я забуду.
«Методы психологии» - Выполните задание. Почему знание социальной психологии способствуют более эффективному взаимодействию людей? Место психологии в системе наук. Зачем нужно изучать психологию? Задачи психологии. Тест «Какой вы психолог?». Психология - наука, изучающая факты, закономерности и механизмы психики. Методы изучения человека.
«Основание греческих колоний» - Как изменились права демоса? А существует ли сегодня в нашем государстве демократия? Почему Солон был вынужден покинуть свое государство на длительный срок? Сделай вывод. Урок на тему: «Основание греческих колоний». Основные причины переселений: Основание греческих колоний. Назовите места колонизации на Средиземном море.
«Получение радиоактивных изотопов» - Получение радиоактивных изотопов. Йод интенсивно отлагается в щитовидной железе, особенно при базедовой болезни. Радиоактивные изотопы широко применяются в науке, медицине и технике. Меченые атомы. С помощью ядерных реакций можно получить изотопы всех химических элементов. Для постановки диагноза, так и для терапевтических целей.
«Метод проектов в литературе» - Метод проектов на уроках литературы. Целеустремленность. Все члены команды равны. Презентация. Такой урок включает в себя приемы и методы различных форм обучения. Каждый должен получать удовольствие от чувства уверенности в себе. Цель нетрадиционных уроков: Все должны проявлять активность и вносить свой вклад в общее дело.
Выделение чистых культур аэробов занимает, как правило, три дня и производится по следующей схеме:
1-й день - микроскопия мазка из исследуемого материала, окрашенного (обычно по Граму) - для предварительного ознакомления с микрофлорой, что может быть полезным в выборе питательной среды для посева. Затем посев материала на поверхность застывшего питательного агара для получения изолированных колоний. Рассев можно произвести по методу Дригальского на три чашки Петри с питательной средой. Каплю материала наносят на первую чашку и распределяют шпателем по всей чашке. Затем этим же шпателем распределяют оставшуюся на нем культуру на второй чашке и таким же образом - на третьей. Наибольшее количество колоний вырастет на первой чашке, наименьшее - на третьей. В зависимости от того, сколько было микробных клеток в исследуемом материале, на одной из чашек вырастут изолированные колонии.
Такого же результата можно достигнуть, произведя рассев на одной чашке. Для этого делят чашку на четыре сектора. Исследуемый материал засевают бактериологической петлей штрихами на первом секторе, затем, прокалив и остудив петлю, распределяют посев из первого сектора во второй и таким же образом последовательно в третий и четвертый сектор. Из отдельных микробных клеток после суточного инкубирования в термостате образуются изолированные колонии.
2-й день - изучение колоний, выросших на чашках, описание их. Колонии могут быть прозрачными, полупрозрачными или непрозрачными, они имеют различные размеры, округлые правильные или неправильные очертания, выпуклую или плоскую форму, гладкую или шероховатую поверхность, ровные или волнистые, изрезанные края. Они могут быть бесцветными или иметь белый, золотистый, красный, желтый цвет. На основании изучения этих характеристик выросшие колонии разделяются на группы. Затем из исследуемой группы отбирают изолированную колонию, готовят мазок для микроскопического исследования с целью проверки однородности микробов в колонии. Из этой же колонии производят посев в пробирку со скошенным питательным агаром.
3-й день - проверка чистоты культуры, выросшей на скошенном агаре путем микроскопии мазка. При однородности исследуемых бактерий выделение чистой культуры можно считать законченным.
Для идентификации выделенных бактерий изучаются культуральные признаки, то есть характер роста на жидких и плотных питательных средах. Например, стрептококки на сахарном бульоне образуют придонный и пристеночный осадок, на кровяном агаре - мелкие, точечные колонии; холерный вибрион образует пленку на поверхности щелочной пептонной воды, а на щелочном агаре - прозрачные колонии; палочка чумы на питательном агаре образует колонии в виде «кружевных платочков» с плотным центром и тонкими волнистыми краями, а в жидкой питательной среде - пленку на поверхности, а затем -нити, отходящие от нее в виде «сталактитов».
Выделение чистых культур анаэробных бактерий:
Химические методы заключаются в том, что чашки с посевами анаэробов ставят в герметически закрытый эксикатор, куда помещают химические вещества, например, пирогаллол и щелочь, реакция между которыми идет с поглощением кислорода.
Биологический метод основан на одновременном выращивании анаэробов и аэробов на плотных питательных средах в чашках Петри, герметически закрытых после посева. Вначале кислород поглощается растущими аэробами, а затем начинается рост анаэробов.
Выделение чистой культуры анаэробов начинают с накопления анаэробных бактерий путем посева на среду Китта-Тароцци. В дальнейшем получают изолированные колонии одним из двух способов.
Метод Пастера (метод предельных разведений). Заключается в том, что из исследуемого материала делают ряд последовательных разведений в жидкой питательной среде. Для этого каплю посевного материала вносят в пробирку со стерильной жидкой средой, из нее каплю переносят в следующую пробирку и так засевают до 8…10 пробирок. С каждым разведением количество микробных клеток, попадающих в среду, будет уменьшаться и можно получить такое разведение, в котором во всей пробирке со средой будет находиться только одна микробная клетка, из которой разовьется чистая культура микроорганизма. Так как в жидких средах микробы растут диффузно, т.е. легко распределяются во всей среде, то изолировать одну микробную клетку от другой трудно. Таким образом, метод Пастера не всегда обеспечивает получение чистой культуры. Поэтому в настоящее время этот метод используется, главным образом, для предварительного уменьшения концентрации микроорганизмов в материале перед посевом его в плотную среду для получения изолированных колоний.
Методы механического разделения микроорганизмов с использованием плотных питательных сред. К таким методам относятся метод Коха и метод Дригальского.
Метод Коха (метод глубинного посева). Исследуемый материал вносят бактериологической петлей или пастеровской пипеткой в пробирку с расплавленной плотной питательной средой. Равномерно размешивают содержимое пробирки, вращая ее между ладонями. Каплю разведенного материала переносят во вторую пробирку, из второй – в третью и т.д. Содержимое каждой пробирки, начиная с первой, выливают в стерильные чашки Петри. После застывания среды в чашках, их помещают в термостат для культивирования.
Для выделения анаэробных микроорганизмов по методу Коха необходимо ограничить доступ кислорода к культуре. С этой целью поверхность глубинного посева в чашке Петри заливают стерильной смесью парафина и вазелина (1:1). Можно также оставлять посевной материал, тщательно перемешанный с агаризованной средой, непосредственно в пробирке. Ватную пробку при этом заменяют резиновой или заливают поверхность агара смесью парафина и вазелинового масла. Чтобы извлечь выросшие колонии анаэробных микроорганизмов, пробирки слегка нагревают, быстро вращая над пламенем горелки. Агар, прилегающий к стенкам, расплавляется, и столбик легко выскальзывает в подготовленную чашку Петри. Далее столбик с агаром разрезают стерильным скальпелем, колонии извлекают стерильной петлей или стерильной капиллярной рубкой и переносят в жидкую среду.
Метод Дригальского основан на механическом разделении микробных клеток на поверхности плотной питательной среды в чашках Петри. Каждая микробная клетка, фиксируясь в определенном месте, начинает размножаться, образуя колонию.
Для посева по методу Дригальского используют несколько чашек Петри, залитых плотной питательной средой. На поверхность среды вносят каплю исследуемого материала. Затем с помощью стерильного шпателя эту каплю распределяют по всей питательной среде (посев газоном).
Посев также можно проводить штрихом, используя бактериологическую петлю. Этим же шпателем или петлей осуществляют посев во вторую, третью и т.д. чашки. Как правило, в первой чашке после культивирования посева появляется рост микробов в виде сплошного налета, в последующих чашках содержание микроорганизмов снижается и образуются изолированные колонии, из которых отсевом можно легко выделить чистую культуру.
Таким образом, в первых секторах получается сплошной рост, а вдоль последующих штрихов вырастут обособленные колонии, представляющие собой потомство одной клетки.
В целях экономии сред и посуды можно пользоваться одной чашкой, разделив ее на сектора, и последовательно засевать их штрихом (метод истощающего штриха). Для этого материал берут петлей и проводят ею ряд параллельных штрихов сначала по поверхности первого сектора, а затем последовательно оставшимися на петле клетками засевают все другие сектора. При каждом последующем штрихе происходит уменьшение количества засеваемых клеток.
Метод выделения чистых культур с помощью химических веществ используется при изолировании культур микроорганизмов, устойчивых к определенным химическим веществам. Например, с помощью этого метода можно выделить чистую культуру туберкулезных микобактерий, устойчивых к действию кислот, щелочей и спирта. В этом случае исследуемый материал перед посевом заливают 15 % раствором кислоты или антиформином и выдерживают в термостате в течение 3…4 часов. После воздействия кислоты или щелочи клетки туберкулезной палочки остаются живыми, а все другие микроорганизмы, содержащиеся в исследуемом материале, погибают. После нейтрализации кислоты или щелочи обработанный материал высевают на плотную среду и получают изолированные колонии возбудителя туберкулеза.
Питательные среды для культивирования бактерий
Для выделения чистых культур патогенных бактерий применяют оптимальные для их роста питательные среды с фиксированным рН. Большинство бактерий способно расти на различных питательных средах; исключение составляют хламидии и риккетсии, не растущие in vitro вне клеточных культур. Используемая среда должна содержать
Вещества, утилизируемые бактериями для различных биосинтетических процессов.
Универсальные источники азота и углерода -- бел- ковые гидролизаты (содержат полный набор аминокис- лот), пептиды и пептоны. Универсальные источники витаминов и микроэлементов -- экстракты белков жи- вотного или растительного происхождения и белковые гидролизаты.
рН среды. В некоторых случаях жизнедеятельность бактерий сопровождается сдвигом рН в кислую или щелочную сторону, что требует внесения в среды раз-- личных буферных систем (обычно применяют фосфат-- ный буфер). Сбалансированные среды отличают высо-- кая буферность и стабильный оптимум рН. Важно так- же создание оптимальной концентрации О 2 и СО 2 .
Посев и культивирование
При достаточном содержании патогенных бактерий в образце проводят посев на плотные пита-тельные среды (для получения изолированных колоний). Если в исследуемом материале бактерий мало, то посев проводят на жидкие среды обогащения. На практике выделение относительно неприхотливых бактерий обычно проводят на простых средах (например, на КА, агаре Плоскирева, тиогликолевом бульоне, агаре Сабуро и т.д.). Для выделения прихотливых видов в среды вносят питательные вещества (кровь, сыворотку, дрожжевой экстракт и др.), а такжепогло-тители токсических метаболитов, образующихся при росте бактерий (например, дре-весный уголь). Для посевов применяют микробиологические петли, реже иглы и шпатели.
Получение изолированных колоний
Для получения изолированных колоний на практике наиболее часто используют модифика-цию рассева по Дригальски. Для этого материал наносят на поверхность плотной питательной среды ближе к краю и делают «бляшку». Затем из неё материал распределяют по четырём квадратам, проводя петлёй штрихи, как показано на рис. 1-12, обжигая петлю после засева каждого квадрата. Подобный метод позволяет получить изолированные колонии и изучать их. Исключение составляет техника посева при бактериологическом исследовании мочи (техника штрихового засева показана на рис.1-13). Указанные методы пригодны для посева аэробных и факультативно анаэробных бактерий, а также нестрогих анаэробов.
Температура культивирования
Патогенные бактерии вариабельны в отношении температур, оптимальных для их роста, но большинство из них неплохо развивается при 35-37 °С. Исключение составляют некоторые атипичные микобактерии, возбудитель чумы, листерии и лептоспиры (температурный оптимум 20-30 °С), а также Campylobacter jejuni (температурный оптимум 42 °С).
Бактерии чётко разделяют по отношению к содержанию кислорода в атмосфере культиви-рования.
Аэробы. Посевы аэробных бактерий культивируют в простых термостатах. Некоторые факуль-тативно анаэробные виды также можно культивировать при атмосферном воздухе, но более оптимально помещение посевов в термостаты с дозированной подачей кислорода. На практи-ке их чаще помещают в эксикаторы, куда вносят горящую свечу; после её выгорания в атмо-сфере снижается содержание кислорода и повышается содержание СО 2 .
Анаэробы. Посевы анаэробных бактерий в жидких средах заливают вазелиновым или другим маслом. При использовании плотных сред посевы культивируют в специальных устройствах -- анаэростатах (откуда откачивают воздух) либо заливают посевы тонким слоем агара. Анаэ-робные условия можно создать химическим путём, поместив посевы в эксикаторы, на дно которых заливают щелочной раствор пирогаллола, поглощающего кислород. Также можно использовать методы Фортнера, Цейсслера и Вейнберга.
Метод Фортнера. Посевы проводят на чашку Петри с толстым слоем среды, разделённым пополам узкой канавкой, вырезанной в агаре. На одну половину засевают культуру аэроб-ных бактерий, на другую -- анаэробных. Края чашки заливают парафином и инкубируют в термостате. Первоначально наблюдают рост аэробов, а затем (после поглощения кислоро-да) -- рост анаэробов.
Метод Цейсслера используют для выделения чистых культур спорообразующих анаэробов. Для этого проводят посев на среду Китта-Тароцци, прогревают 15 мин при 80 °С (для унич-тожения вегетативных форм), заливают вазелиновым маслом и инкубируют 24 ч. Затем про-водят посев на сахарно-кровяной агар для получения чистых культур. После 24-часового культивирования подозрительные колонии изучают и отсевают на среду Китта-Тароцци (с последующим контролем чистоты выделенной культуры).
Метод Вейнберга используют для получения чистых культур строгих анаэробов. Культуры, выращенные на среде Китта-Тароцци, вносят в сахарный бульон. Затем пастеровской пи-петкой с запаянным концом материал переносят в узкие пробирки (трубки Виньяля) с сахарным МПА, погружая пастерку до дна пробирки. Засеянные пробирки быстро охлаждают холодной водой, что позволяет зафиксировать отдельные бактериальные клетки в толще затвердевшего агара. Пробирки инкубируют, и изучают выросшие колонии. При обнаружении подозрительной колонии на её месте делают распил, колонию быстро отбирают и засеивают на среду Китта-Тароцци (с последующим контролем чистоты выделенной культуры).
Методы культивирования
При выращивании бактерий применяют стационарный способ, способ глубинного культивирования с аэрацией и метод проточных питательных сред. В соответствии со способами выращивания бактериальные культуры разделяют на периодические (при стационарном и глубинном культивировании) инепрерывные (при проточном культивировании).
Стационарный способ -- наиболее часто используемый на практике. Состав сред остаётся постоянным, с ними не проводят никаких дополнительных манипуляций.
Способ глубинного культивирования применяют при промышленном выращивании бактериальной биомассы, для чего используют специальные котлы-реакторы. Они снабжены систе-мами поддержания температуры, подачи в бульон различных питательных веществ, переме-шивания биомассы и постоянной подачи кислорода. Создание аэробных условий по всей толще среды способствует протеканию энергетических процессов по аэробному пути, что способствует максимальной утилизации энергетического потенциала глюкозы и, следователь-но, максимальному выходу биомассы.
Метод проточных сред (промышленный способ культивирования) позволяет постоянно под-держивать бактериальную культуру в экспоненциальной фазе роста, что достигают постоянным внесением питательных веществ и удалением определённого числа бактериальных клеток. Пре-бывание бактерий в экспоненциальной стадии роста обеспечивает максимальный выход различ-ных БАВ (витамины, антибиотики и др.).
Первичная идентификация бактерий
В большинстве случаев изучение особенностей роста для первичной идентификации возбу-дителей проводят на колониях, выросших в течение 18-24 ч. Характер роста бактерий на раз-личных средах может дать много полезной информации. На практике используют сравнительно небольшой набор критериев. В жидких средах обычно учитывают характер поверхностного (образование плёнки) или придонного роста (вид осадка) и общее помутнение среды. На твёр-дых средах бактерии формируют колонии --изолированные структуры, образующиеся в результате роста и накопления бактерий. Колонии возникают как следствие роста и размноже-ния одной или нескольких клеток. Таким образом,пересев из колонии в дальнейшем даёт возможность оперировать с чистой культурой возбудителя. Рост бактерий на плотных сре-дах имеет больше характерных особенностей.
Размеры и форма колоний
Важные признаки колоний -- их размеры и форма. Колонии могут быть большими или мелкими. Величина колоний -- признак, позволяющий различать различные виды, роды и даже типы бактерий.
В большинстве случаев ко-лонии грамположительных бактерий мель-че колоний грамотрицательных бактерий. Колонии бактерий могут быть плоскими, приподнятыми, выпуклыми, иметь вдавлен-ный или приподнятый центр. Другой важный признак --форма краёв колоний. При изучении фор-мы колоний учитывают характер её поверх-ности: матовый, блестящий, гладкий или ше-роховатый. Края колоний могут быть ров-ными, волнистыми, дольчатыми (глубоко изрезанными), зубчатыми, эрозированными, бахромчатыми и т.д. Размеры и формы ко-лоний часто могут изменяться. Подобные изменения известны какдиссоциации. Наиболее часто обнаруживают S- и R-ducсоциации. S-колонии круглые, гладкие и выпуклые, с ровными краями и блестящей поверхностью. R-колонии -- неправильной формы, шероховатые, с зубчатыми краями.
Цвет колоний
При просмотре посевов также обращают внимание на цвет колоний. Чаще они бесцветные, белые, голубоватые, жёлтые или бежевые; реже -- красные, фиолетовые, зелёные или чёрные. Иногда колонии ирризируют, то есть переливаются всеми цветами радуги [от греч. iris, радуга]. Окрашивание возникает в результате способности бактерий к пигментообразованию. На специ-альных дифференцирующих средах, включающих специальные ингредиенты или красители, ко-лонии могут приобретать разнообразную окраску (чёрную, синюю и др.) за счёт включения красителей либо их восстановления из бесцветной формы. В данном случае их окраска не связана с образованием каких-либо пигментов.
Запах
Запах -- менее важный признак колоний, поскольку вызываемые им ассоциации носят субъективный характер. В частности, культуры синегнойной палочки имеют запах карамели, культуры листерий -- молочной сыворотки, протеев -- гнилостный запах, нокардий -- свежевскопанной земли.
Для выделения бактерий в виде чистых культур известно сравнительно мало методов. Чаще всего это делают путем изолирования отдельных клеток на твердой питательной среде, используя метод посева штрихом или разлива по чашкам небольшого количества жидкой культуры (метод предельных разведений ). Однако получение отдельной колонии не всегда гарантирует чистоту культуры, поскольку колонии могут вырасти не только из отдельных клеток, но и из их скоплений. Если микроорганизмы образуют слизь, то часто к ней прикрепляются посторонние формы. Для очистки предпочтительно использовать неселективную среду (МПА), поскольку на ней лучше растут контаминирующие микроорганизмы и их легче обнаружить.
Получение изолированных колоний на твердой питательной среде достигается либо путем рассева взвеси микроорганизмов шпателем (метод Коха ), либо с помощью бактериологической петли (метод истощающего штриха ). В результате механического разобщения клеток микроорганизмов каждая из них может дать начало изолированной колонии одного вида микробов.
Рассев шпателем (метод Коха) производят в следующей последовательности:
1) на поверхность питательной среды в чашке № 1 наносят стерильной пипеткой каплю накопительной культуры и распределяют ее стерильным шпателем;
2) шпатель достают, чашку быстро закрывают и переносят шпатель в чашку № 2, не стерилизуя его. Имитируют распределение культуры по всей поверхности среды, прикасаясь к ее поверхности той же стороной шпателя, которой ранее распределяли пробу;
3) точно те же действия проводят и в чашке № 3, после чего шпатель стерилизуют;
4) засеянные чашки помещают в термостат и инкубируют при оптимальной температуре.
Через определенное время чашки достают из термостата и изучают рост микроорганизмов. Обычно в чашке № 1 наблюдают сплошной рост бактерий, в последующих чашках отмечают колонии.
Рассев петлей (метод истощающего штриха) предполагает высев бактериологической петлей из накопительной культуры на поверхность агаризованной среды в чашках Петри. На первом этапе петлей с культурой наносят ряд параллельных штрихов на агаризованной среде (рисунок 4.2, А ). Петлю стерилизуют, остужают о незасеянную часть агаризованной среды и проводят серию штрихов в направлении, перпендикулярном первым (рисунок 4.2, Б ). Затем петлю вновь стерилизуют, остужают и штрихи наносят в направлении В (рисунок 4.2), а после очередной стерилизации – в направлении Г (рисунок 4.2). Чашки помещают в термостат и через определенное время учитывают результаты. Обычно на штрихах А и Б вырастает большое число колоний (иногда сплошной рост), тогда как на штрихах В и Г формируются изолированные колонии.
Рисунок 4.2 – Схема рассева бактерий штрихами для получения изолированных колоний
Последовательные разведения в твердой среде – самый простой способ посева по чашкам, который заключается в том, что после инокуляции пробы в пробирку со стерильным расплавленным и охлажденным агаром, среду перемешивают, выливают в чашку Петри и дают ей застыть. Для получения хорошо изолированных колоний готовят ряд последовательных десятикратных разведений и по 1 мл проб вносят сразу в чашку, добавляют 15–20 мл расплавленной агаризованной среды и смешивают, покачивая чашку. Иногда отдельные колонии оказываются погруженными в агар и извлечь их можно только механически. Плохо и то, что бактерии некоторое время находятся в среде при температуре расплавленного агара.