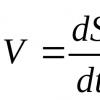Диффузионный потенциал и его физическая природа. Контактный и диффузионный потенциалы. Выход вещества по току
Как уже указывалось, концентрационные цепи имеют большое практическое значение, так как с их помощью можно определять такие важные величины как коэффициент активности и активность ионов, растворимость малорастворимых солей, числа переноса и т.д. Такие цепи практически легко осуществимы и соотношения, связывающие ЭДС концентрационной цепи с активностями ионов, так же проще, чем для других цепей. Напомним, что электрохимическая цепь, содержащая границу двух растворов, называется цепью с переносом и схема ее изображается следующим образом:
Ме 1 ½раствор (I) раствор (II)½Ме 2 ½Ме 1 ,
где пунктирная вертикальная черта указывает на существование между двумя растворами диффузионного потенциала, который является гальвани – потенциалом между точками, находящимися в разных по химическому составу фазах, а потому его нельзя точно измерить. Величина диффузионного потенциала входит в сумму для расчета ЭДС цепи:
![]()
Малая величина ЭДС концентрационной цепи и необходимость точного ее измерения делают особенно важным либо полное устранение, либо точный расчет диффузионного потенциала, который возникает на границе двух растворов в такой цепи. Рассмотрим концентрационную цепь
Ме½Ме z+ ½Ме z+ ½Me
Напишем уравнение Нернста для каждого из электродов этой цепи:
для левого 
для правого 
Допустим, что активность ионов металла у правого электрода больше, чем у левого, т.е.
Тогда очевидно, что j 2 положительнее, чем j 1 и ЭДС концентрационной цепи (Е к) (без диффузионного потенциала) равна разности потенциалов j 2 – j 1 .
Следовательно, 
 , (7.84)
, (7.84)
тогда при Т = 25 0 С  , (7.85)
, (7.85)
где и – моляльные концентрации ионов Ме z + ; g 1 и g 2 – коэффициенты активности ионов Ме z + соответственно у левого (1) и правого (2) электродов.
а) Определение средних ионных коэффициентов активности электролитов в растворах
Для наиболее точного определения коэффициента активности необходимо измерить ЭДС концентрационной цепи без переноса, т.е. когда отсутствует диффузионный потенциал.
Рассмотрим элемент, состоящий из хлорсеребряного электрода, погруженного в раствор HCl (моляльностью C m) и водородного электрода:
(–) Pt, H 2 ½HCl½AgCl, Ag (+)
Процессы, происходящие на электродах:
(–) H 2 ® 2H + + 2
(+) 2AgCl + 2 ® 2Ag + 2Cl –
токообразующая реакция H 2 + 2AgCl ® 2H + + 2Ag + 2Cl –
Уравнение Нернста
для водородного электрода:  ( = 1атм)
( = 1атм)
для хлорсеребряного: 
Известно, что
=  (7.86)
(7.86)
Учитывая, что средняя ионная активность для HClравна
![]() и
и ![]() ,
,
где С m – моляльная концентрация электролита;
g ± – средний ионный коэффициент активности электролита,
получаем  (7.87)
(7.87)
Для расчета g ± по данным измерения ЭДС необходимо знать стандартный потенциал хлорсеребряного электрода, который в данном случае будет и стандартным значением ЭДС (Е 0), т.к. стандартный потенциал водородного электрода равен 0.
После преобразования уравнения (7.6.10) получим
 (7.88)
(7.88)
Уравнение (7.6.88) содержит две неизвестные величины j 0 и g ± .
По теории Дебая – Хюккеля для разбавленных растворов 1-1 электролитов
lng ± = –A ,
где А – коэффициент предельного закона Дебая и согласно справочным данным для этого случая А = 0,51.
Поэтому, последнее уравнение (7.88) можно переписать в следующем виде:
 (7.89)
(7.89)
Для определения строят график зависимости  от и проводят экстраполяцию к С m = 0 (рис. 7.19).
от и проводят экстраполяцию к С m = 0 (рис. 7.19).

Рис. 7.19. График для определения Е 0 при вычислении g ± р-ра НСl
Отрезок, отсекаемый от оси ординат, будет величиной j 0 хлорсеребряного электрода. Зная , можно по экспериментальным величинам Е и известной моляльности для раствора HCl (C m), используя уравнение (7.6.88), найти g ±:
 (7.90)
(7.90)
б) Определение произведения растворимости
Знание стандартных потенциалов позволяет легко рассчитать произведение растворимости труднорастворимой соли или оксида.
Для примера рассмотрим AgCl: ПР = L AgCl = a Ag + . a Cl –
Выразим L AgCl через стандартные потенциалы, согласно электродной реакции
AgCl – AgCl+ ,
идущей на электроде IIрода
Cl – / AgCl, Ag
И реакции Ag + + Ag,
идущей на электроде Iрода с токообразующей реакцией
Cl – + Ag + ®AgCl
 ;
;  ,
,
т.к. j 1 = j 2 (электрод один и тот же) после преобразования:
 (7.91)
(7.91)
![]() = ПР
= ПР
Значения стандартных потенциалов берутся из справочника, тогда легко рассчитать ПР.
в) Диффузионный потенциал концентрационной цепи. Определение чисел переноса
Рассмотрим обычную концентрационную цепь с использованием солевого мостика с целью исключения диффузионного потенциала
(–) Ag½AgNO 3 ½AgNO 3 ½Ag (+)
ЭДС такой цепи без учета диффузионного потенциала равна:
 (7.92)
(7.92)
Рассмотрим эту же цепь без солевого мостика:
(–) Ag½AgNO 3 AgNO 3 ½Ag (+)
ЭДС концентрационной цепи с учетом диффузионного потенциала:
Е КД = Е К + j Д (7.93)
Пусть через раствор пройдет 1 фарадей электричества. Каждый вид ионов переносит часть от этого количества электричества, равную его числу переноса (t + или t –). Количество электричества, которое перенесут катионы и анионы, будет равно t + . F и t – . F соответственно. На границе соприкосновения двух растворов AgNO 3 разной активности возникает диффузионный потенциал (j Д). Катионы и анионы, преодолевая (j Д), совершают электрическую работу.
В расчете на 1 моль:
DG = –W эл = – zFj Д = – Fj д (7.94)
При отсутствии диффузионного потенциала ионы при пересечении границы раствора совершают только химическую работу. При этом изменяется изобарный потенциал системы:
![]()
Аналогично для второго раствора:
|
![]()
Тогда по уравнению (7.6.18)
 (7.99)
(7.99)
Преобразуем выражение (7.99), с учетом выражения (7.94):
 (7.100)
(7.100)
 (7.101)
(7.101)
Числа переноса (t + и t –) могут быть выражены через ионные проводимости:
 ;
; 
Тогда  (7.102)
(7.102)
Если l – > l + , то j д > 0 (диффузионный потенциал помогает движению ионов).
Если l + > l – , то j д < 0 (диффузионный потенциал препятствует движению ионов, уменьшает ЭДС). Если l + = l – , то j д = 0.
Если в уравнение (7.99) подставим значение j д из уравнения (7.101), то получим
Е КД = Е К + Е К (t – – t +), (7.103)
после преобразования:
Е КД = Е К + (1 + t – – t +) (7.104)
Известно, что t + + t – = 1; тогда t + = 1 – t – и выражение
 (7.105)
(7.105)
Если выразить Е КД через проводимости, то получим:
Е КД =  (7.106)
(7.106)
Измеряя Е КД экспериментально, можно определить числа переноса ионов, их подвижности и ионные проводимости. Этот метод значительно проще и удобнее, чем метод Гитторфа.
Таким образом, с помощью экспериментального определения различных физико-химических величин можно провести количественные расчеты по определению ЭДС системы.
Используя концентрационные цепи, можно определить раствори-мость малорастворимых солей в растворах электролитов, коэффициент активности и диффузионный потенциал.
Электрохимическая кинетика
Если электрохимическая термодинамика занимается исследованием равновесий на границе электрод – раствор, то измерение скоростей процессов на этой границе и выяснение закономерностей, которым они подчиняются, является объектом изучения кинетики электродных процессов или электрохимической кинетики.
Электролиз
Законы Фарадея
Поскольку прохождение электрического тока через электро-химические системы связано с химическим превращением, то должна существовать определенная зависимость между количеством электри-чества и количеством прореагировавших веществ. Эта зависимость была открыта Фарадеем (1833-1834 гг.) и получила отражение в первых количественных законах электрохимии, названных законами Фарадея .
Электролиз – возникновение химических превращений в электрохимической системе при пропускании через нее электрического тока от внешнего источника. Путем электролиза удается провести процессы, самопроизвольное протекание которых невозможно согласно законам термодинамики. Например, разложение HСl (1M) на элементы сопровождается возрастанием энергии Гиббса 131,26 кДж/моль. Однако под действием электрического тока этот процесс легко может быть осуществлен.
Первый закон Фарадея.
Количество прореагировавшего на электродах вещества пропорционально силе тока, прошедшего через систему, и времени его прохождения.
Математически выражается:
Dm = kэI t = kэq, (7.107)
где Dm – количество прореагировавшего вещества;
kэ – некоторый коэффициент пропорциональности;
q – количество электричества, равное произведению силы
тока I на время t.
Если q = It = 1, тоDm = k э, т.е. коэффициент k э представляет собой количество вещества, реагирующее при протекании единицы количества электричества. Коэффициент пропорциональности k э называется электро-химическим эквивалентом . Так как в качестве единицы количества электричества могут быть выбраны различные величины (1 Кл= 1А. с; 1F = 26,8 А. ч = 96500 К), то для одной и той же реакции следует различать электрохимические эквиваленты, относящиеся к этим трем единицам: А. с k э, А. ч k э и F k э.
Второй закон Фарадея .
При электрохимическом разложении различных электролитов одним и тем же количеством электричества содержание полученных на электродах продуктов электрохимической реакции пропорционально их химическим эквивалентам.
По второму закону Фарадея при постоянном количестве прошедшего электричества массы прореагировавших веществ относятся между собой как их химические эквиваленты А .
 . (7.108)
. (7.108)
Если за единицу количества электричества выбрать фарадей, то
Dm 1 = F k э 1 ; Dm 2 = F k э 2 и Dm 3 = F k э 3 , (7.109)
 (7.110)
(7.110)
Последнее уравнение позволяет объединить оба закона Фарадея в виде одного общего закона, по которому количество электричества, равное одному фарадею (1F или 96500 Кл, или 26,8 А. ч), всегда изменяет электрохимически один грамм-эквивалент любого вещества, независимо от его природы.
Законы Фарадея применимы не только к водным и неводным растворам солей при обычной температуре, но справедливы и в случае высокотемпературного электролиза расплавленных солей.
Выход вещества по току
Законы Фарадея являются наиболее общими и точными количественными законами электрохимии. Однако в большинстве случаев электрохимическому изменению подвергается меньшее количество данного вещества, чем рассчитанное на основании законов Фарадея. Так, например, если пропускать ток через подкисленный раствор сульфата цинка, то при прохождении 1F электричества выделяется обычно не 1 г-экв цинка, а примерно 0,6 г-экв. Если подвергать электролизу растворы хлоридов, то в результате пропускания 1F электричества образуется не один, а немногим более 0,8 г-экв газообразного хлора. Подобные отклонения от законов Фарадея связаны с протеканием побочных электрохимических процессов. В первом из разобранных примеров на катоде протекает фактически две реакции:
реакция осаждения цинка
Zn 2+ + 2 = Zn
и реакция образования газообразного водорода
2Н + + 2 = Н 2
Результаты, полученные при выделении хлора, также не будут противоречить законам Фарадея, если учесть, что часть тока расходуется на образование кислорода и, кроме того, выделенный на аноде хлор может частично снова переходить в раствор вследствие вторичных химических реакций, например по уравнению
Cl 2 + H 2 O = HCl + HСlO
Чтобы учесть влияние параллельных, побочных и вторичных реакций, было введено понятие выхода по току Р . Выход по току – это часть количества протекшего электричества, которая приходится на долю данной электродной реакции
Р = (7.111)
или в процентах
Р = . 100 %, (7.112)
где q i – количество электричества, расходуемое на данную реакцию;
Sq i – общее количество прошедшего электричества.
Так, в первом из примеров выход по току цинка составляет 60 %, а водорода – 40 %. Часто выражение для выхода по току записывается в другой форме:
Р = . 100 %, (7.113)
где q p и q p – количество электричества, соответственно рассчитанное по закону Фарадея и пошедшее фактически на электрохимическое превращение данного количества вещества.
Можно также определить выход по току как отношение количества измененного вещества Dm p к тому, которое должно было бы прореагировать, если бы весь ток расходовался только на данную реакцию Dm р:
Р = . 100 %. (7.114)
Если из нескольких возможных процессов желателен только один, то необходимо, чтобы его выход по току был как можно выше. Имеются системы, в которых весь ток расходуется лишь на одну электрохимическую реакцию. Такие электрохимические системы используются для измерения количества прошедшего электричества и называются кулонометрами, или кулометрами.
Внешняя клеточная мембрана – плазмалемма – в своей основе представляет липидный слой, который является диэлектриком. Поскольку с обеих сторон мембраны располагается проводящая среда, то вся эта система с точки зрения электротехники представляет собой конденсатор . Таким образом, переменный ток по живой ткани может проходить как по активным сопротивлениям, так и через электрические ёмкости, образованные многочисленными мембранами. Соответственно сопротивление прохождению переменного тока через живую ткань будут оказывать две составляющих: активная R - сопротивление движению зарядов по раствору, и реактивная X - сопротивление току электрической ёмкости на мембранных структурах. Реактивное опротивление имеет поляризационную природу, и его величина связана с величиной электрической ёмкости формулой:
где С – электрическая ёмкость, w - круговая частота, f – частота тока.
Эти два элемента могут быть соединены последовательно и параллельно.
Эквивалентная электрическая схема живой ткани – это соединение элементов электрической цепи, каждый из которых соответствует определённому элементу структуры изучаемой ткани.
Если мы учтём основные структуры ткани, то мы получим следующую схему:
Рисунок 2 - Эквивалентная электрическая схема живой ткани
R ц - сопротивление цитоплазмы, R мж - сопротивление межклетников, С м - электрическая ёмкость мембраны.
Понятие импеданса .
Импеданс – суммарное комплексное сопротивление активной и реактивной составляющих электрической цепи. Его величина связана с обеими составляющими формулой:
где Z - импеданс, R – активное сопротивление, X – реактивное сопротивление.
Величина импеданса при последовательном соединении реактивного и активного сопротивления выражается формулой:

Величина импеданса при параллельном соединении реактивного и активного сопротивления записывается в виде:
![]()
Если мы проанализируем как изменяется величина импеданса при изменении R и C, то придём к выводу, что и при последовательном и параллельном соединении этих элементов при увеличении активного сопротивления R импеданс увеличивается, а при увеличении С – уменьшается и наоборот.
Импеданс живой ткани – лабильная величина, которая зависит, во-первых, от свойств измеряемой ткани, а именно:
1) от структуры ткани (мелкие или крупные клетки, плотные или рыхлые межклетники, степень одревеснения клеточных оболочек);
2) оводнённости ткани;
4) состояния мембран.
Во-вторых, на импеданс влияют условия измерения:
1) температура;
2) частота тестируемого тока;
3) схема электрической цепи.
При разрушении мембран различными экстремальными факторами будет наблюдаться уменьшение сопротивления плазмалеммы, а также апопласта за счёт выхода клеточных электролитов в межклеточное пространство.
Постоянный ток пойдёт главным образом по межклетникам и его величина будет зависеть от сопротивления межклеточного пространства.
| С, нФ |
| f, Гц |
| 10 4 |
| 10 6 |
| образец нативный |
| образец проморож. |
| Z, Ом |
| f, Гц |
| 10 4 |
| 10 6 |
| образец нативный |
| образец промороженный |
Рисунок 3 - Измененение ёмкости (C) и сопротивления (R) ткани при изменении частоты переменного тока (f)
Преимущественный путь переменного тока зависит от частоты прикладываемого напряжения: с увеличением частоты всё большая доля тока будет идти через клетки (через мембраны), и комплексное сопротивление будет уменьшаться. Это явление – уменьшение импеданса при возрастании частоты тестирующего тока – называется дисперсией электропроводности .
Крутизна дисперсии характеризуется коэффициентом поляризации. Дисперсия электропроводности живых тканей является результатом поляризации при низких частотах, как и при постоянном токе. Электропроводность связана с поляризацией – по мере увеличения частоты поляризационные явления сказываются меньше. Дисперсия электропроводности, как и способность к поляризации присуща только живым тканям.
Если посмотреть, как изменяется коэффициент поляризации при отмирании ткани, то в первые часы он уменьшается довольно сильно, затем его падение замедляется.
Печень млекопитающих имеет коэффициент поляризации 9-10, печень лягушки 2-3: чем выше уровень метаболизма, тем выше коэффициент поляризации.
Практическое значение.
1. Определение морозоустойчивости.
2. Определение водообеспеченности.
3. Определение психоэмоционального состояния человека (прибор «Тонус»)
4. Компонент детектора лжи – полиграфа.
Мембранный диффузионный потенциал
Диффузионный потенциал – электрический потенциал, возникающий вследствие микроскопического разделения зарядов из-за разностей в скорости движения различных ионов. А разная скорость движения через мембрану связана с разной избирательной проницаемости.
Для его возникновения необходим контакт электролитов с различной концентрацией и различной подвижностью анионов и катионов. Например, ионов водорода и хлора (рис. 1.). Граница раздела одинаково проницаема для обоих ионов. Переход ионов H + и Cl - будет осуществляться в сторону меньшей концентрации. Подвижность Н + при перемещении через мембрану намного выше Cl - , в силу этого, будет создаваться большая концентрация ионов с правой стороны от границы раздела электролитов, возникнет разность потенциалов.
Возникающий потенциал (поляризация мембраны) тормозит дальнейший перенос ионов, так что, в конце концов, суммарный ток через мембрану прекратится.
В растительных клетках главные потоки ионов – это потоки К + , Na + , Cl - ; они в значительных количествах содержаться внутри и снаружи клетки.
Учитывая концентрации этих трёх ионов, их коэффициенты проницаемости, можно рассчитать величину мембранного потенциала, обусловленного неравномерным распределением этих ионов. Это уравнение получило название уравнение Гольдмана, или уравнение постоянного поля:
где φ M - разность потенциалов, В;
R - газовая постоянная, T - температура; F - число Фарадея;
P - проницаемость иона;
0 - концентрация иона снаружи клетки;
I - концентрация иона внутри клетки;
Диффузионный потенциал - это разность потенциалов, возникающая на границе раздела между двумя неодинаковыми растворами электролита. Он обусловлен диффузией ионов через границу раздела и вызывает торможение более быстро диффундирующих ионов и ускорение более медленно диффундирующих ионов, будь то катионы или анионы. Таким образом, вскоре устанавливается равновесней потенциал на границе раздела достигает постоянной величины , которая зависит от числа переноса ионов, величины их заряда и концентрации электролита.
Э. д. с. концентрационной цепи (см.)
выражаемая уравнением

есть сумма двух электродных потенциалов и диффузионного потенциала Алгебраическая сумма двух электродных потенциалов теоретически равна
![]()
следовательно,
Предположим, что , тогда
или в общем случае для электрода, обратимого по отношению к катиону,

и для электрода, обратимого по отношению к аниону,

Для электродов, обратимых по отношению к катиону, когда если то величина положительная и добавляется к сумме электродных потенциалов; если то величина отрицательная и э. д. с. элемента в этом случае меньше, чем сумма электродных потенциалов. Предпринимались попытки исключить диффузионный потенциал введением солевого мостика, содержащего концентрированный раствор и других солей, для которых . В таком случае, поскольку раствор концентрированный, диффузия обусловлена электролитом самого солевого мостика и вместо диффузионного потенциала ячейки имеем два диффузионных потенциала, действующих в противоположных направлениях и имеющих близкую к нулю величину. Таким путем удается уменьшить диффузионные потенциалы, но полностью их исключить практически невозможно.
Диффузионные потенциалы возникают на границе соприкосновения двух растворов. Причем это могут быть как растворы разных веществ, так и растворы одного и того же вещества, только в последнем случае они обязательно должны отличаться друг от друга своими концентрациями.
При соприкосновении двух растворов происходит взаимопроникновение в них частиц (ионов) растворенных веществ вследствие процесса диффузии.
Причина возникновения при этом диффузионного потенциала заключается в неодинаковой подвижности ионов растворенных веществ. Если ионы электролита обладают разной скоростью диффузии, то более быстрые ионы постепенно оказываются впереди менее подвижных. Образуются как бы две волны разнозаряженных частиц.
Если смешиваются растворы одного и того же вещества, но с разной концентрацией, то более разбавленный раствор приобретает заряд, совпадающий по знаку с зарядом более подвижных ионов, а менее разбавленный – заряд, совпадающий по знаку с зарядом менее подвижных ионов (рис. 90).
Рис. 90. Возникновение диффузионного потенциала вcледствие разной скорости ионов: I
– «быстрые» ионы, заряженные отрицательно;
II
– «медленные» ионы, заряженные положительно
На границе раздела растворов возникает так называемый диффузионный потенциал. Он усредняет скорости движения ионов (тормозит более «быстрые» и ускоряет более «медленные»).
Постепенно, с завершением процесса диффузии данный потенциал снижается до нуля (обычно в течение 1-2 часов).
Диффузионные потенциалы могут возникать и в биологических объектах при повреждении оболочек клеток. При этом нарушается их проницаемость и электролиты могут диффундировать из клетки в тканевую жидкость или наоборот в зависимости от разности концентрации по обе стороны мембраны.
В результате диффузии электролитов возникает так называемый потенциал повреждения, который может достигать величин порядка 30-40 мV. Причем поврежденная ткань чаще всего заряжается отрицательно по отношению к неповрежденной.
Диффузионный потенциал возникает в гальванических элементах на границе соприкосновения двух растворов. Поэтому при точных вычислениях э.д.с. гальванических цепей обязательно должна вводиться поправка на его величину. Для устранения влияния диффузионного потенциала электроды в гальванических элементах часто соединяют друг с другом «солевым мостиком», представляющим собой насыщенный раствор KCl.
Ионы калия и хлора имеют почти одинаковые подвижности, поэтому их применение позволяет в значительной степени уменьшить влияние диффузионного потенциала на величину э.д.с.
Диффузионный потенциал может сильно возрасти, если растворы электролитов разного состава или разных концентраций разделить мембраной, проницаемой только для ионов определенного знака заряда или вида. Такие потенциалы будут гораздо более стойкими и могут сохраняться в течение более длительного времени – они называются иначе мембранными потенциалами . Мембранные потенциалы возникают при неравномерном распределении ионов по обе стороны мембраны, зависящем от её избирательной проницаемости, или в результате обмена ионами между самой мембраной и раствором.
На возникновении мембранного потенциала основан принцип работы так называемого ион-селективного или мембранного электрода.
Основой такого электрода является определенным образом полученная полупроницаемая мембрана, обладающая селективной ионной проводимостью. Особенностью мембранного потенциала является то, что в соответствующей ему электродной реакции не участвуют электроны. Здесь имеет место обмен ионами между мембраной и раствором.
Мембранные электроды с твердой мембраной содержат тонкую мембрану, по обе стороны которой находятся разные растворы, содержащие одни и те же определяемые ионы, но с неодинаковой концентрацией. С внутренней стороны мембрану омывает стандартный раствор с точно известной концентрацией определяемых ионов, с внешней стороны – анализируемый раствор с неизвестной концентрацией определяемых ионов.
Вследствие различной концентрации растворов по обе стороны мембраны ионы обмениваются с внутренней и внешней сторонами мембраны неодинаковым образом. Это приводит к тому, что на разных сторонах мембраны образуется разный электрический заряд и как результат этого, возникает мембранная разность потенциалов.
Диффузионный потенциал
В электрохимических цепях на границах раздела между неодинаковыми растворами электролитов возникают скачки потенциала. Для двух растворов с одинаковым растворителем такой скачок потенциала называется диффузионным потенциалом. В месте контакта двух растворов электролита КА, отличающихся друг от друга концентрацией, происходит диффузия ионов из раствора 1, более концентрированного, в раствор 2, более разбавленный. Обычно скорости диффузии катионов и анионов различны. Допустим, что скорость диффузии катионов больше скорости диффузии анионов. За некоторый промежуток времени из первого раствора во второй перейдет больше катионов, чем анионов. В результате этого раствор 2 получит избыток положительных зарядов, а раствор 1 -- отрицательных. Поскольку растворы приобретают электрические заряды, то скорость диффузии катионов уменьшается, анионов увеличивается, и с течением времени эти скорости становятся одинаковыми. В стационарном состоянии электролит диффундирует как единое целое. При этом каждый раствор имеет заряд, и разность потенциалов, установившаяся между растворами, соответствует диффузионному потенциалу. Расчет диффузионного потенциала в общем случае затруднителен. С учетом некоторых допущений Планком и Гендерсоном выведены формулы для расчета цд. Так, например, при контакте двух растворов одного и того же электролита с различной активностью (б1б2)
где и -- предельные молярные электрические проводимости ионов. Величина цд мала и в большинстве случаев не превышает нескольких десятков милливольт.
ЭДС электрохимической цепи с учетом диффузионного потенциала
……………………………….(29)
Уравнение (29) используется для расчета (или) по результатам измерения Е, если известны (или) и. Поскольку определение диффузионного потенциала связано с существенными экспериментальными трудностями, то при измерениях ЭДС удобно устранить с помощью солевого мостика. Последний содержит концентрированный раствор электролита, молярные электрические проводимости ионов которого приблизительно одинаковы (KCl, KNO3). Солевой мостик, в котором содержится, например, КС1, располагают между растворами электрохимической цени, и вместо одной жидкостной границы в системе возникают две. Так как концентрация ионов в растворе КС1 значительно выше, чем в соединяемых им растворах, то практически только ионы K+ и С1- диффундируют через жидкостные границы, на которых возникают очень малые и обратные по знаку диффузионные потенциалы. Их суммой можно пренебречь.,
Строение двойного электрического слоя
Переход заряженных частиц через границу раствор -- металл сопровождается возникновением на этой границе двойного электрического слоя (д.э.с) и скачка потенциала. Двойной электрический слой создается электрическими зарядами, находящимися на металле, и ионами противоположного заряда (противоионами), ориентированными в растворе у поверхности электрода.
В формировании ионной обкладки д.э.с. принимают участие как электростатические силы, под влиянием которых противоионы подходят к поверхности электрода, так и силы теплового (молекулярного) движения, в результате действия которых д.э.с. приобретает размытое, диффузное строение. Кроме того, в создании двойного электрического слоя на границе металл -- раствор существенную роль играет эффект специфической адсорбции поверхностно-активных ионов и молекул, которые могут содержаться в электролите.
Строение двойного электрического слоя в отсутствие специфической адсорбции. Под строением д.э.с. понимают распределение зарядов в его ионной обкладке. Упрощенно ионную обкладку можно условно разделить на две части: 1) плотную, или гельмгольцевскую, образованную ионами, практически вплотную подошедшими к металлу; 2) диффузную, созданную ионами, находящимися на расстояниях от металла, превышающих радиус сольватированного иона (рис. 1). Толщина плотной части порядка 10-8 см, диффузной -- 10-7--10-3 см. Согласно закону электронейтральности
……………………………..(30)
где, - плотность заряда со стороны металла, со стороны раствора, в плотной диффузионной части д.э.с. соответственно.

Рис.1. Строение двойного электрического слоя на границе раствор - металл.: аб - плотная часть;бв - диффузная часть
Распределение потенциала в ионной обкладке двойного электрического слоя, отражающее его строение, представлено на рис.2. Величина скачка потенциала ц на границе раствор -- металл соответствует сумме величин падения потенциала в плотной части д.э.с и -- в диффузной. Строение д.э.с. определяется общей концентрацией раствора, С ее ростом диффузия противоиоиов от поверхности металла в массу раствора ослабляется, в результате чего сокращаются размеры диффузной части. Это приводит к изменению -потенциала. В концентрированных растворах диффузная часть практически отсутствует, и двойной.электрический слой подобен плоскому конденсатору, что соответствует модели Гельмгольца, впервые предложившего теорию строения д.э.с..

Рис.1. Распределение потенциала в ионной обкладке при различной концентрации раствора: аб - плотная часть; бв - диффузная часть; ц - разность потенциалов между раствором и металлом; ш,ш1 - падение потенциала в плотной и диффузной частях д.э.с.
Строение двойного электрического слоя в условиях специфической адсорбции. Адсорбция - концентрирование вещества из объема фаз на поверхности раздела между ними - может быть вызвана как электростатическими силами, так и силами межмолекулярного взаимодействия и химическими. Адсорбцию, вызванную силами неэлектростатического происхождения, принято называть специфической. Вещества, способные адсорбироваться на границе раздела фаз, называются поверхностно-активными (ПАВ). К ним относятся большинство анионов, некоторые катионы и многие молекулярные соединения. Специфическая адсорбция ПАВ, содержащегося в электролите, влияет на структуру двойного слоя и величину -потенциала (рис.3). Кривая 1 соответствует распределению потенциала в двойном электрическом слое в отсутствие ПАВ в растворе. Если раствор содержит вещества, дающие при диссоциации поверхностно-активные катионы, то за счет специфической адсорбции поверхностью металла катионы будут входить в плотную часть двойного слоя, увеличивая ее положительный заряд (кривая 2). В условиях, способствующих усилению адсорбции (например, увеличение концентрации адсорбата), в плотной части может оказаться избыточное количество положительных зарядов по сравнению с отрицательным зарядом металла (кривая 3). По кривым распределения потенциала в двойном слое видно, что -потенциал изменяется при адсорбции катионов и может иметь знак, противоположный знаку потенциала электрода.

Рис.3.
Эффект специфической адсорбции наблюдается и на незаряженной поверхности металла, т.е. в тех условиях, когда обмен ионами между металлом и раствором отсутствует. Адсорбированные ионы и соответствующие противоионы образуют двойной электрический слой, расположенный в непосредственной близости к металлу со стороны раствора. Ориентированные около поверхности металла адсорбированные полярные молекулы (ПАВ, растворителя) также создают двойной электрический слой. Скачок потенциала, отвечающий двойному электрическому слою при незаряженной поверхности металла, называется потенциалом нулевою заряда (ц.н.з.).,,
Потенциал нулевого заряда определяется природой металла и составом электролита. При адсорбции катионов п.н.з. становится более положительным, анионов -- более отрицательным. Потенциал нулевого заряда является важной электрохимической характеристикой электродов. При потенциалах, близких к п.н.э., некоторые свойства металлов достигают предельных значений: велика адсорбция ПАВ, максимальна твердость, минимальна смачиваемость растворами электролитов и др.
Результаты исследований в области теории двойного электрического слоя позволили более широко рассмотреть вопрос о природе скачка потенциала на границе раствор -- металл. Этот скачок обусловлен следующими причинами: переходом заряженных частиц через границу раздела (), специфической адсорбцией ионов () и полярных молекул (). Гальвани-потенциал на границе раствор -- металл можно рассматривать как сумму трех потенциалов:
……………………………..(31)
В условиях, при которых обмен заряженными частицами между раствором и металлом, а также адсорбция ионов не происходят, все же остается скачок потенциала, вызванный адсорбцией молекул растворителя, -- . Гальвани-потенциал может быть равен нулю только тогда, когда, и компенсируют друг друга.
В настоящее время нет прямых экспериментальных и расчетных методов определения величин отдельных скачков потенциала на границе раздела раствор -- металл. Поэтому вопрос об условиях, при которых скачок потенциала обращается в нуль (так называемый абсолютный нуль потенциала), остается пока открытым. Однако для решения большинства электрохимических задач знание отдельных скачков потенциалов не обязательно. Достаточно пользоваться значениями электродных потенциалов, выраженными в условной, например водородной, шкале.
Строение двойного электрического слоя не отражается на термодинамических свойствах равновесных электродных систем. Но при протекании электрохимических реакций в неравновесных условиях ионы испытывают влияние электрического поля двойного слоя, что приводит к изменению скорости электродного процесса.